Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
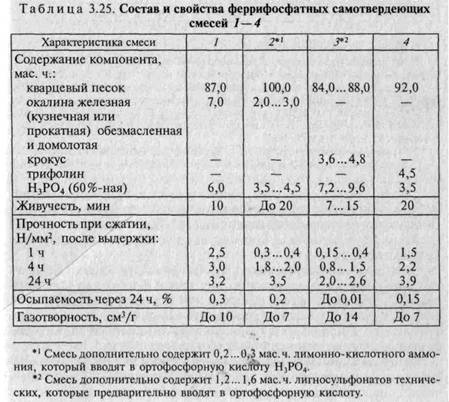
Примерный состав металлофосфатной смеси ⇐ ПредыдущаяСтр 3 из 3 MgO1,5-2% Формовочного песка 98-98.5% Ортофосфорная кислота сверх 100% добавляется 2% Добавки: - лимонная кислота как замедлитель твердения - фосфат аммония для модифицирования продуктов твердения. Фосфаты могут добавляться в ПГС и жидкостекольные смеси. Состав и свойства фосфатных самотвердеющих смесей приведены в табл. 3.25 и 3.26. Феррифосфатные самотвердеющие смеси (см. табл. 3.25) интенсивно разрушаются при нагреве (после прогрева до 800... 1000 °С остаточная прочность при сжатии составляет 0,03...0,08 Н/мм2). Этим обеспечивается облегченная выбиваемость отливок. Из-за недостаточных термостойкости, огнеупорности и по причине склонности к пригарообразованию их можно рекомендовать только для отливок из чугуна и цветных сплавов. Смеси являются экологически чистыми и практически не выделяют вредных веществ в воздушную среду. Областью применения магнийфосфатных самотвердеющих смесей являются преимущественно стержни и формы для стальных отливок, что обусловлено достаточной термостойкостью, огнеупорностью и податливостью указанных смесей (см. табл.). При этом смесь 7 используется при получении крупных массивных стальных отливок с толщиной стенок свыше 300 мм.
Алюмофосфатные материалы Довольно часто сейчас интересуются клеями-цементами, основанными на фосфорной кислоте, а также ее производных. Издавна известно, что фосфорная кислота обладает вяжущими свойствами. В этой области фосфорная кислота, поначалу использовалась для того, чтобы получить цинкофосфатные зубные цементы, которые схватываются буквально за пару минут. Кислые соли также не обделены вяжущими свойствами – это одно- и двузамещенные фосфаты. Наилучшими свойствами обладают кислые фосфаты алюминия, «связками» называют их водные растворы. В процессе взаимодействия гидроокиси алюминия (может быть и трехзамещенный фосфат алюминия) с ортофосфорной кислотой образуются кислые фосфаты алюминия. Их вязкость, также как и вяжущие свойства находятся в прямой зависимости от соотношения воды, окиси фосфора и окиси алюминия.  Алюмофосфатные клеи с высокой теплостойкостью и механической прочностью разрабатываются на основе алюмофосфатных связок. Характерная особенность данных клеев – сохранение механической прочности даже после нагревания. Ещё одним положительным свойством алюмофосфатных клеев является то, что они не выделяют газообразных продуктов при термической обработке. Благодаря этому, эти клеи используют и для крепления внутренних деталей установок и вакуумных приборов. Для того чтобы приготовить алюмофосфатную связку, при нагревании растворяют в ортофосфорной кислоте (плотность = 1,70 г/см3) гидроокись алюминия в соотношении 5:1. Если брать во внимание исходное состояние, то соотношение гидроокиси алюминия, воды и фосфорной кислоты в связке равно 1:2:3. Когда связка готова к употреблению, ее состав немного изменяется (здесь все зависит от объема испарившейся воды). Связки – это вязкие прозрачные продукты, плотность которых составляет 1,7-1,8 г/см3. Срок их годности – 3 суток, после чего они начинают мутнеть и становятся слишком вязкими. Процесс изготовления алюмофосфатных клеев заключается в смешивании алюмофосфатных связок с наполнителями. Лишь от назначения клея зависит то, какой из них выбрать. Таким образом, мелкодисперсную окись алюминия, или алунд, трехзамещенный фосфат алюминия, каолин (1:2:12) используют для получения клея, обладающего неплохими электроизоляционными свойствами. Сначала порошки прокаливают в муфельной печи на протяжении 2 часов при температуре 950-1000 градусов Цельсия для того, чтобы удалить летучие примеси (и обезводить), после чего порошок измельчают на валковой мельнице. Алюмофосфатный клей может состоять из 3 вес. ч. ортофосфорной кислоты, 4 вес. ч. связки и 10 вес. ч. смеси наполнителей. Многое зависит от назначения клея, в частности возможность изменения количества фосфорной кислоты и смеси наполнителей. Например, в роли наполнителей для производства токопроводящих клеев применяют металлические порошки. Чтобы склеить мелкие детали (это может быть проволока, диаметр которой равен 10-20 мкм) используют клей с большим содержанием связки (до 50 %). В данном случае применяются порошки наполнителей с более тонким помолом. Если предназначение клея – работа в глубоком вакууме, то каолин полностью исключается из смеси наполнителей. Уже при комнатной температуре алюмофосфатные клеи становятся твердыми, но, чтобы отверждение произошло полностью, клеевой шов нагревают при температуре 270-300 градусов на протяжении 2-6 часов (все зависит от толщины шва). После того, как клей высушат при более низких температурах, он начинает поглощать влагу из воздуха, набухая при этом и становясь мягким, после чего теряется его механическая прочность. Повышение температуры во время сушки клея должно осуществляться со скоростью не более 2 градусов в минуту в интервале температур от 20 до 10 и от 200 до 280 градусов Цельсия, а также не более 1,5 градуса в минуту в интервале температур 100-200 градусов. Если температуру в процессе сушки поднимать быстрее, то клеевой шов станет пористым из-за интенсивного испарения воды, прочность снижается. Клей можно сушить как на воздухе, так и в вакууме, атмосфере азота, водорода. Все зависит от свойств склеиваемых материалов. Таким образом, если металлы легко окисляются и их нужно склеить, сушка клея производится в вакууме или в атмосфере водорода. Если же взять во внимание материалы, которые не окисляются на воздухе (керамика), то склеивание их будет одинаково прочным в любой среде. Фосфат - хром Фосфат хрома относится к труднорастворимым соединениям Наилучшие растворители - хлорная и соляная кислоты. Нами выбрана соляная кислота, потому что присутствие ClOj как было-проверено экспериментально, значительно влияет на положение-прямой lg t а Ъ lg С, уменьшая угол наклона к оси абсцисс, что свидетельствует о понижении чувствительности. [1] Фосфат хрома СгРО4 - пН2О - порошок светло-зеленого цвета, представляет собой кристаллогидрат средней соли ортофосфорной кислоты. Фосфат хрома кристаллизуется с шестью молекулами воды, при нагревании до 105 С теряет 2 5 - 3 моль воды. Как правило, в качестве антикоррозионного пигмента используется продукт кристаллизации с тремя молекулами воды. [2] Фосфат хрома легко растворим в минеральных кислотах, в холодной уксусной кислоте и в щелочах. [3] Фосфат хрома частично растворим в уксусной кислоте на холоду и нерастворим в ней при кипячении. [4] Фосфат хрома СгРО4 образуется при действии Na2HPO4 на раствор соли хрома. Образующийся осадок СгРО4 серо-зеленого ( иногда фиолетового цвета) растворим в кислотах ( минеральной, уксусной) и в щелочах. [5] Фосфат хрома нетоксичен и по защитным свойствам превосходит тетраоксихромат цинка. [6] Фосфат хрома кристаллизуется с 6 моль воды, при нагревании до 105 С теряет 2 5 - 3 моль. Как правило, в качестве антикоррозионного пигмента используется продукт с 3 моль воды. Фосфат хрома не токсичен, практически не растворим в воде и органических растворителях, стоек к кислотам и щелочам, средний размер частиц 0 6 мкм. [7] Фосфат хрома получают восстановлением шестивалентных соединений хрома до трехвалентного в присутствии ортофосфорной кислоты. В качестве восстановителей применяют сульфит натрия и тиосульфат натрия. [8] Фосфат хрома, синтезируемый из водных растворов, кристаллизуется с 6 молекулами воды, но легко теряет кристаллизационную воду. Воздушно-сухой пигмент состава СгР04 - 6Н2О при нагревании до 105 - 110 С теряет до 3 молекул воды. [9] Фосфат хрома получают при восстановлении солей хрома ( VI) в присутствии ортофосфорной кислоты. [10] Получаютфосфат хрома восстановлением шестивалентного хрома до трехвалентного в присутствии фосфорной кислоты. [11] Препаратыфосфата хрома представляют собой сине-зеленые порошки с удельной активностью от 3 до 30 мкюри. [12] Получаемые осадкифосфата хрома отфильтровываются, промываются дистиллированной водой и высушиваются при температуре 100 С. [13] Процесс полученияфосфата хрома состоит в восстановлении шестивалентного хрома до трехвалентного в присутствии ортофосфорной кислоты. [14] Метод полученияфосфата хрома состоит из приготовления хромовой смеси ( Ка2Сг2От Н3РО4) и приготовления раствора сульфита натрия ( N SOs-THaO) при40 С. [15] Полагают, чтофосфат хрома представляет собой как бы готовый хромофосфатный комплекс и реагирует в грунтовках с поли-винилбутиралем, что сопровождается выделением фосфорной кислоты, вступающей во взаимодействие с металлом. Для большей эффективности фосфат хрома должен иметь высокую степень дисперсности. [16] Сырьем для полученияфосфата хрома могут служить хромат натрия и тиосульфат натрия, ортофосфорная кислота и серная кислота. [17] При организации производствафосфата хрома на заводах хромовых соединений, где раствор хромата натрия является полупродуктом, а раствор тиосульфата натрия - отходом производства Сг2Оз, удобно пользоваться методом восстановления тиосульфатом натрия. В этом случае процесс получения фосфата отличается от описанного выше тем, что рН хромовой смеси в процессе восстановления доводят от 11 - 12 до 1 8 - 2 0 добавлением сначала фосфорной, а затем серной кислоты. Процесс протекает при 70 - 80 С. [18] При дегидратации гексагидратафосфата хрома СгРО4 - 6Н2О обнаружены [35] а - и р-формы СгРО4; р - СгРО4 - метастабильная модификация, наблюдаемая при 1000 - 1100 С; а - СгРО4 стоек до температуры 1800 С, при которой происходит его плавление. [19] В грунтовки, содержащиефосфат хрома, при нанесении их по алюминиевым сплавам необходимо вводить дополнительно некоторое количество хромата цинка и свободной фосфорной кислоты. [20] Зелень Динглера - смесьфосфата хрома и фосфата кальция, менее красивая, чем зелень Арнодона. [21] Реакции получения карбоната ифосфата хрома проводят аналогично реакциям получения карбоната и фосфата алюминия. [22] Обратимые пленки состоят изфосфатов хрома или хроматов в смеси с гидратом окиси алюминия; они образуются при обработке изделий погружением или распылением растворов, содержащих хром ( VI), фосфаты, фториды и ускорители. Вначале фосфатные пленки на алюминии аморфны, имеют гелеобразную структуру и в первые часы после образования гидрофильны и довольно легко выщелачиваются горячей водой и растворяются разбавленным раствором азотной кислоты. После нагревания выше 65 С фосфатные пленки становятся гидрофобными и не растворимыми в разбавленной азотной кислоте. [23] При анализе растворов, содержащихфосфат хрома ( зеленый), разделение при обычных условиях протекает не полностью. Для анализа растворов, содержащих комплексные ацетаты и формиаты хрома, метод ионного обмена также неприменим. [24]
Гидрофосфат натрия выделяет зеленый осадокфосфата хрома СгРО4, растворимого в едких щелочах и кислотах, в том числе и в уксусной кислоте. При кипячении уксуснокислого раствора фосфата выпадает осадок основного фосфата. [27] Определение фосфат-ионов и натрия вфосфате хрома весовым методом очень длительно и трудоемко, а определение малых количеств натрия в присутствии большого количества хрома, кроме того, недостаточно надежно. [29] По приготовленным эталонам были проанализированы пробыфосфата хрома и искусственные смеси. Натрий определяли методом градуировочного графика, а фосфат-ионы - методом ограничивающих растворов. [30] Предложенный метод проверен на ряде пробфосфата хрома. Для сравнения принят весовой метод. Результаты приведены в таблице. [31] С использованием в качестве противокоррозионного пигментафосфата хрома была разработана [69 ] однокомпонентная грунтовка ВЛ-05, которая представляет собой суспензию пигментов ( фосфата хрома и смеси его с хроматом) в растворе поливинилбутираля с добавкой фосфорной кислот. [32] Однокомпонентный грунт ВЛ-05 содержит в качестве пигментафосфат хрома, который позволяет сохранять стабильность грунта в течение длительного времени - не менее года. [33] Представляет интерес применение для приготовления одно-компонентных грунтовокфосфата хрома. Полагают, что фосфат хрома представляет собой как бы готовый хромофосфатный комплекс и реагирует в грунтовках с поливинилбутиралем, что сопровождается выделением фосфорной кислоты, вступающей во взаимодействие с металлом. Для большей эффективности фосфат хрома должен иметь высокую степень дисперсности. [34] Перспективными в этом отношении являются фосфатные пигменты: фосфат хрома и фосфат цинка. Они практически нетоксичны, но значительно уступают хроматам по защитному действию. Известно, что сам по себе фосфат хрома не обеспечивает пассивирования металлической поверхности. Продукты его гидролиза, взаимодействуя с неорганическими ионами или карбоксильными группами пленкообразующих, могут образовывать защитные слои. [35] Катион Сг3 с гидрофосфатом натрия Na2HPO4 образует осадокфосфата хрома СгРО4 зеленого цвета, растворимый в кислотах и щелочах; с арсенитами и арсенатами дает малорастворимые осадки арсенита CrAsO3 и арсената CrAsO4 соответственно. [36]
В вытяжке, полученной из смеси тетраоксихромата цинка ифосфата хрома ( 30 и 70 %), сталь сильно пассивируется даже при незначительной плотности тока. [38]
Проведенные исследования дают основание полагать, что при смешениифосфата хрома с тетраоксихроматом цинка происходит взаимодействие этих пигментов, приводящее к образованию фосфата цинка и новых хроматных соединений, лучше растворяющихся в воде, чем исходные соединения. При проведении испытаний в дистиллированной воде, камере Г-4 и 3 % - ном растворе хлорида натрия было установлено, что покрытия, пигментированные смесью фосфата хрома и тетраоксихромата цинка, имеют лучшие защитные свойства, чем покрытия, пигментированные каждым из этих пигментов в отдельности. Оптимальным соотношением тетраоксихромата и фосфата хрома-является 30: 70, что ранее было устанорлено при исследовании водных вытяжек. Это позволило втрое уменьшить в грунтовках содержание токсичного хроматного пигмента, заменив его нетоксичным фосфатом хрома. [40] Предложен пламеннофотометрический метод определения содержания натрия и фосфат-ионов вфосфате хрома. Для определения содержания фосфат-ионов использован принцип понижения интенсивности излучения кальция в присутствии фосфат-ионов. [41] Данные по определению сульфат-ионов ( в %) вфосфате хрома хронофотомет. [42] Наверху образуется зона фосфата железа, ниже располагается серо-голубая зонафосфата хрома, затем - розово-фиолетовая зона фосфата кобальта. [43] Для целей терапии разработаны методы получения радиоактивных коллоидов золота, фосфатов хрома, цирконила. Для стабилизации радиоактивных коллоидных систем следует применять желатину, устойчивую к действию излучения. [44] Наверху образуется зона фосфата железа, ниже располагается серо-голубая зонафосфата хрома, затем - розово-фиолетовая зона фосфата кобальта. [45] На основании проведенных исследований предложен хронофотометрический метод определения сульфат-ионов вфосфате хрома. [46]
Все это указывает на то, что, хотя водные вытяжкифосфата хрома образуют на поверхности стали пленки, обладающие изолирующими свойствами, сами по себе они не способны защитить сталь от коррозии, но в присутствии ионов CrCV облегчается оксидная пассивация, что способствует образованию защитных слоев, полностью защищающих металл от коррозии. [48] Повышение температуры термической обработки АХФС приводит к кристаллизации фосфатов алюминия ифосфатов хрома. Уже при 400 С в стекле установлена зачаточная субмикроскопическая кристаллизация, которая может быть отнесена к началу образования алюмо-фосфатов. [49] К пигментам этой группы относятся оксид и гидроксид хрома, а такжефосфат хрома; последний применяется в качестве противокоррозионного пигмента. [50] При получении алюмохром-фосфатной связки ( АХФС) используют взаимодействие фосфата алюминия сфосфатом хрома или нейтрализацию кислотой трехвалентного хрома и алюминия. Расчеты удобно вести на такие смешанные фосфаты. [51] Другой пример - повышение полноты осаждения катионов хрома ( Ш) Сг3 видефосфата хрома ( Ш) СгРО4, из растворов при одновременном выделении осадка фосфата железа ( Ш) FePO4, чем пользуются в аммиачно-фосфатном методе качественного анализа катионов. [52]
|
||||||||||||||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 885. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |