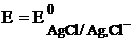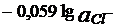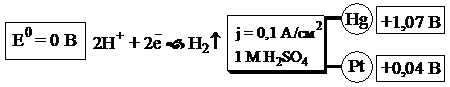Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Эксклюзионная хроматографияВ эксклюзионной хроматографии (гель-хроматографии) разделение основано на различиях в размерах и форме молекул. В качестве твёрдого носителя в гель-хроматографии используют различные сетчатые полимеры («гели»). Неподвижной фазой является элюент, находящийся в порах зёрен твёрдого носителя, подвижной фазой - этот же элюент, протекающий вдоль слоя частиц полимера. В процессе хроматографирования более мелкие молекулы проникают в поры геля и задерживаются в находящейся в них неподвижной фазе. Более крупные молекулы не проникают в поры и поэтому движутся быстрее. Таким образом, выход компонентов смеси из колонки происходит в порядке уменьшения их молекулярных масс (рис 24.10). Величина коэффициента распределения (D) в эксклюзионной хроматографии может находиться в пределах от 0 до 1. Для крупных молекул, не способных проникать в поры геля, D = 0, следовательно, удерживаемый объём равен свободному объёму колонки - VR = Vm. В случае молекул, размер которых позволяет им свободно диффундировать через пористый материал, D = 1 (поскольку состав подвижной и неподвижной фаз одинаков), следовательно, удерживаемый объём равен сумме свободного объёма колонки и объёма жидкости, находящейся в порах – VR = Vm + Vs. Для молекул промежуточного размера Vm < VR < VS. Поскольку диапазон возможных значений D в эксклюзионной хроматографии очень узок, то для эффективного разделения в данном виде хроматографии приходится применять длинные колонки или несколько соединённых друг с другом колонок.
Рис. 24.10. Принцип эксклюзионной хроматографии
Большинство из мягких гелей гидрофильны. Процесс хроматографирования на мягких гелях называется гель-фильтрационной хроматографией. Полужёсткие гели в основном гидрофобны. Процесс хроматографирования на таких гелях называется гель-проникающей хроматографией.  В качестве растворителей в эксклюзионной хроматографии используют воду, диметилформамид, хлороформ, толуол и т.д. Выбор растворителя зависит от типа используемого геля, вида разделяемых веществ, применяемой системы детектирования. Основное назначение гель-хроматографии - разделение смесей высокомолекулярных соединений (а также высокомолекулярных и низкомолекулярных) и определение молекулярномассового распределения полимеров. Как и ионообменная хроматография гель-хроматография может быть колоночной и плоскостной, проводиться как в «классическом» варианте, так и в высокоэффективном. ГЛАВА 25
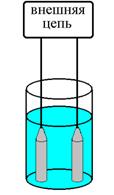
Электрохимическими называют методы анализа, основанные на использовании процессов, происходящих в электрохимической ячейке. 25.1. Основные понятия, связанные с электрохимическими методами анализа Электрохимической ячейкой называется система, состоящая из пары электродов и электролита, контактирующих между собой. Электродом называется граница раздела, на которой электронный механизм переноса заряда (направленное движение электронов) меняется на ионный (направленное движение ионов). В менее строгом смысле под термином «электрод» обычно подразумевают проводник электрического тока с электронной проводимостью. Электролитом называется среда, в которой происходит перенос заряда в результате направленного движения ионов. Электроды, входящие в состав электрохимической ячейки, могут находиться в одном растворе либо в разных растворах, контактирующих друг с другом с помощью солевого мостика или через пористую перегородку (рис. 25.1). Ячейки первого типа называются ячейками без жидкостного соединения, второго типа - ячейками с жидкостным соединением.
Рис. 25.1. Электрохимическая ячейка с жидкостным соединением (слева) и без жидкостного соединения (справа) В состав электрохимической ячейки должно входить, по крайней мере, два электрода.
Потенциал электрода сравнения должен: · быть хорошо воспроизводимым; · не изменяться во времени; · не зависеть от состава анализируемого раствора, действия электрического тока и т.д.
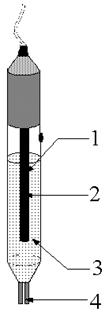
На практике в качестве электродов сравнения чаще всего применяют хлоридсеребряный и каломельный электроды. Например, хлоридсеребряный электрод представляет собой серебряную проволочку, покрытую AgCl и помещённую в раствор KCl (рис. 25.2). AgCl¯ +
При использовании насыщенного раствора KCl потенциал хлоридсеребряного электрода при температуре 25 °С равен +0,222 В. В некоторых случаях в состав электрохимической ячейки может входить ещё и третий электрод, называемый вспомогательным. Этот электрод служит источником электронов либо, наоборот, играет роль стока электронов и тем самым обеспечивает возможность протекания электрического тока через ячейку. Как правило, ни сила тока, ни потенциал вспомогательного электрода не измеряются. Вспомогательный электрод изготавливают из инертного материала. Если в электрохимической ячейке протекают электрохимические реакции, то в зависимости от режима работы она может быть:
Если во внешней цепи не протекает электрический ток, то потенциал индикаторного электрода подчиняется уравнению Нернста и называется равновесным. Если во внешней цепи начинает протекать электрический ток, то это приводит к отклонению величины потенциала электрода от рассчитанной по уравнению Нернста. Такое явление называется поляризацией, а электрод (или электрохимическая ячейка) - поляризованным. Концентрационная поляризация (hс) возникает вследствие медленной диффузии вещества из объёма раствора к поверхности электрода и приводит к уменьшению потенциала электрода. В том случае, когда измеряют величину равновесного потенциала, концентрационная поляризация является нежелательным процессом, и её стремятся свести к минимуму. В вольтамперометрических методах анализа она, наоборот, необходима. Для уменьшения концентрационной поляризации, анализируемый раствор постоянно перемешивают и кроме того, плотность тока на индикаторном электроде должна быть незначительной. В вольтамперометрии измерение проводят в разбавленных неперемешиваемых растворах и применяют электроды с большой плотностью тока. Кинетическая поляризация, илиперенапряжение (ht) обусловлена медленным переносом электронов на поверхности электродов. Величина кинетической поляризации зависит от природы окислительно-восстановительной системы и материала электрода.
|
|||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 416. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |



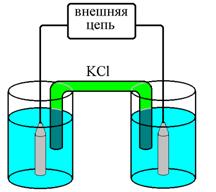

 › Ag¯ + Cl-
› Ag¯ + Cl-