
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
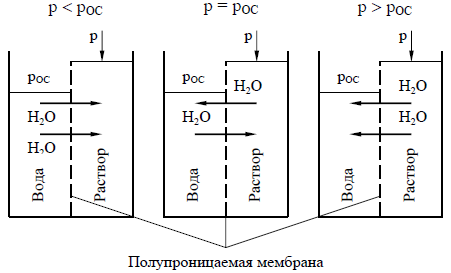
Механизмы мембранного массопереноса.I. Без химического взаимодействияпроникающего компонента и материаламембраны. 1. Осмос-процесс разделения раствора путем проницания через мембранурастворителя из области с меньшей концентрацией растворенного вещества в область с большей концентрацией. В основе метода разделения растворов обратным осмосом лежит явление самопроизвольного перехода растворителя через полупроницаемую мембрану в раствор (рис. 2.20). Если давление над раствором ниже осмотического р<рОС, то растворитель будет переходить в раствор до достижения осмотического равновесия в системе. Равновесное состояние наступает, когда гидростатическое давление между раствором и растворителем, определяемое разностью уровней, станет равным осмотическому р=рОС. Если после достижения равновесия со стороны раствора приложить давление, превышающее осмотическое р>рОС, то растворитель начнет переходить из раствора в обратном направлении. В этом случае будет иметь место обратный осмос. Растворитель, прошедший через мембрану, называют пермеатом.
Рис. 2.20. Схема разделения раствора обратным осмосом 2. Обратный осмос-процесс разделения раствора путем преимущественногопроницания растворителя через мембрану под действием внешнего давления. 3. Аномальный осмос–осмотический процесс в электролитах,при котором врезультате массопереноса компонента противоположные поверхности мембраны получают разноименные заряды, и в теле мембраны проходит ток. 4. Ультрафильтрация-мембранный процесс отделения растворенноговещества большой молекулярной массы (условно принимается, что она должна быть больше 500) от низкомолекулярных веществ и растворителя под действием внешнего давления.  5. Диализ-диффузионный процесс разделения смеси веществ,основанный наразличии их скоростей диффузии через мембрану. 6. Пьезодиализ–процесс диффузионного проникновения раствора черезмембрану за счет разности давлений. 7. Электродиализ–процесс разделения ионов растворенного вещества поддействием постоянного электрического поля при их пропускании через мембрану; 8. Испарение через мембрану-процесс проницания компонента из жидкой впаровую фазу через мембрану. II. С химическим взаимодействиемпроникающего компонента и материаламембраны. 1) Облегченная диффузия–процесс диффузионного переноса целевогокомпонента в мембране с повышенным коэффициентом диффузии за счет наличия в мембране вещества-носителя. 2) Активный перенос–процесс диффузионного переноса вещества противградиента его концентрации за счет химического взаимодействия компонентов между собой внутри мембраны при каталитическом воздействии ее материала. I закон Фика(закон молекулярной диффузии для мембранного процесса) (2.95):
где М – количество вещества, кг; F – поверхность мембраны, м2; Закон Дарси -характеризует скорость проницания потока вещества черезпористую среду (2.96):
где V – объем жидкости, м3; Закон Вант-Гоффа–осмотическое давление в растворах прямопропорционально концентрации растворенного вещества (2.97):
где R - универсальная газовая постоянная 8,31 Дж/(моль·К); T - абсолютная температура, K. Закон Ома для электродиализа–ионный поток прямо пропорционаленградиенту электрических потенциалов (2.98):
где Rэ – электрическое сопротивление; |
||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 393. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 (2.95)
(2.95) - время процесса, с; W – скорость процесса, кг/(м2·с), D – коэффициент молекулярной диффузии, м2/c;
- время процесса, с; W – скорость процесса, кг/(м2·с), D – коэффициент молекулярной диффузии, м2/c;  - градиент концентрации, кг м/м3.
- градиент концентрации, кг м/м3. (2.96)
(2.96) - динамический коэффициент вязкости, Па с;
- динамический коэффициент вязкости, Па с; 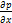 - градиент давления, Па/м; К – коэффициент проницаемости Дарси.
- градиент давления, Па/м; К – коэффициент проницаемости Дарси. (2.97)
(2.97) (2.98)
(2.98) – градиент электрического потенциала, b – коэффициент пропорциональности.
– градиент электрического потенциала, b – коэффициент пропорциональности.