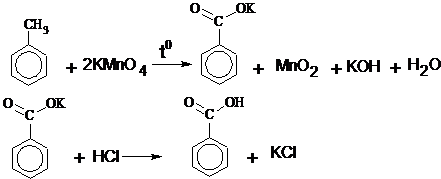Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Выход 1-нитронафталина 20 г.G Техника безопасности.Диоксид азота NO2 и его димеры – газ красно-бурого цвета с резким запахом. Водой разлагается. Растворим в азотной и серной кислотах, хлороформе, сероуглероде. Ткип. = 21,3°С. Вызывает раздражение слизистых оболочек глаз и дыхательных путей, сухость в горле, кашель, тошноту, возможен отек легких. Обладает скрытым периодом действия. Первая помощь при отравлении: дышать чистым воздухом, избегать физических усилий. Полный покой, тепло. Пить молоко (лучше небольшими порциями) или каждые 10 минут по 2-3 глотка воды, содержащей хлороформ (2-3 капли хлороформа на стакан воды). Меры предосторожности: синтез проводить только в вытяжном шкафу с опущенными стеклами, колбу (стакан) с реакционной смесью не выносить из-под вытяжного шкафа. Синтез 3-нитрофталевой кислоты Уравнения основных реакций:
Побочные реакции:
Реактивы Основные
Вспомогательные
Посуда и приборы
Выполнение синтеза В круглодонную колбу емкостью 100 см3 вносят 10 г фталевой кислоты  После охлаждения к реакционной смеси добавляют 48 см3 воды. Если добавить меньше воды, то наряду с 3-нитрофталевой кислотой в осадок частично выпадает лучше растворимая в воде 4-нитрофталевая кислота, образовавшаяся в качестве побочного продукта реакции. Раствор охлаждают в бане со льдом и выпавшую через некоторое время (приблизительно через час) 3-нитрофталевую кислоту трижды перекристаллизовывают из минимального количества воды, каждый раз охлаждая раствор в бане со льдом. Такой прием позволяет полностью освободиться от примеси 4-нитрофталевой кислоты. Выход 3-нитрофталевой кислоты 5 г. G Техника безопасности.Диоксид азота NO2 и его димеры – газ красно-бурого цвета с резким запахом. Водой разлагается. Растворим в азотной и серной кислотах, хлороформе, сероуглероде. Ткип. = 21,3°С. Вызывает раздражение слизистых оболочек глаз и дыхательных путей, сухость в горле, кашель, тошноту, возможен отек легких. Обладает скрытым периодом действия. Первая помощь при отравлении: дышать чистым воздухом, избегать физических усилий. Полный покой, тепло. Пить молоко (лучше небольшими порциями) или каждые 10 минут по 2-3 глотка воды, содержащей хлороформ (2-3 капли хлороформа на стакан воды). Меры предосторожности: синтез проводить только в вытяжном шкафу с опущенными стеклами, колбу (стакан) с реакционной смесью не выносить из-под вытяжного шкафа. Окисление Окисление алканов. Условия окисления и применяемые окислители. Получающиеся продукты. Окисление алканов как способ получения высших жирных кислот. Окисление непредельных углеводородов. Реакция окисления без расщепления углеродного скелета молекулы: реакция Вагнера, получение эпоксидов. Реакции окисления с расщеплением углеродного скелета: озонирование и окисление сильными окислителями (К2Сr2О7, КМnО4 и др.). Реакция окисления как метод установления строения непредельных углеводородов. Окисление алициклических углеводородов. Окисление моно- и полициклических ароматических углеводородов и их гомологов. Окислительное расщепление бензола и нафталина (озонирование, окисление кислородом на катализаторе). Окисление боковых цепей ароматических углеводородов: до альдегидов, кетонов и карбоновых кислот (катализаторы и условия реакции). Окисление первичных и вторичных спиртов в карбонильные соединения. Применяемые окислители. Применяемые катализаторы. Окисление третичных спиртов. Окисление альдегидов кислородом воздуха. Окисление альдегидов другими окислителями. Реакция с аммиачным раствором гидрата окиси серебра, с Фелинговым раствором. Окисление сильными окислителями (НNО3, КМnО3, К2Сr2О7). Условия проведения этих реакций. Окисление кетонов. Применяемые окислители и направление реакции. Синтез бензойной кислоты Уравнения основных реакций:
KOH + Hcl ¾¾® Kcl + H2O
Окисление толуола идет в щелочной среде, которую создает образующееся во время реакции едкое кали. Реактивы Основные
Вспомогательные
Посуда и приборы
Выполнение синтеза В круглодонную колбу, снабженную обратным холодильником (рис. В.3), помещают 2,1 см3 толуола, 3,2 г тонко измельченного марганцевокислого калия и 75 см3 воды. Для равномерного кипения реакционной смеси в колбу бросают несколько «кипелок». Содержимое колбы нагревают на электрической плитке в течение 3-х часов, периодически перемешивая (при этом диоксид марганца оседает на дно колбы), до обесцвечивания раствора. В течение 3-х часов кипячения жидкость должна находиться в состоянии равномерного кипения, не должно наблюдаться «захлебывание» холодильника. Если реакционная жидкость не обесцветилась, для разложения оставшегося окислителя прибавляют 1-2 см3 этилового спирта (можно вводить спирт через верх внутренней трубки холодильника) или 0,5 г щавелевой кислоты (вводят в предварительно охлажденную реакционную жидкость), взбалтывают и нагревают несколько минут. Бесцветный раствор отфильтровывают от выпавшего диоксида марганца на установке для вакуум-фильтрования (рис. В.4), диоксид марганца промывают два раза кипящей водой (по 10-15 см 3). Фильтраты собирают и упаривают на водяной бане примерно до 25 см3 . Вновь выпавший диоксид марганца отфильтровывают и промывают небольшим количеством горячей воды. Фильтрат – раствор бензойнокислого калия – действием концентрированной соляной кислоты (ее добавляют до явно кислой реакции на лакмус) переводят в свободную бензойную кислоту. Бензойная кислота выделяется в виде белых кристаллов. Кристаллы отфильтровывают на установке для вакуум-фильтрования, промывают небольшим количеством холодной воды и сушат на воздухе (не в сушильном шкафу, может возогнаться). Идентифицируют полученную бензойную кислоту по температуре плавления. |
||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-06-01; просмотров: 712. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
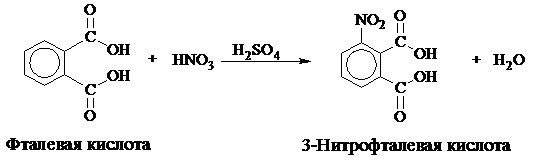


 = 1,5 г/см3) азотной кислоты. Реакционную смесь нагревают 2 часа на кипящей водяной бане, при этом наблюдается энергичное выделение ядовитых окислов азота. К концу реакции 3-нитрофталевая кислота начинает выпадать в виде блестящих призм.
= 1,5 г/см3) азотной кислоты. Реакционную смесь нагревают 2 часа на кипящей водяной бане, при этом наблюдается энергичное выделение ядовитых окислов азота. К концу реакции 3-нитрофталевая кислота начинает выпадать в виде блестящих призм.