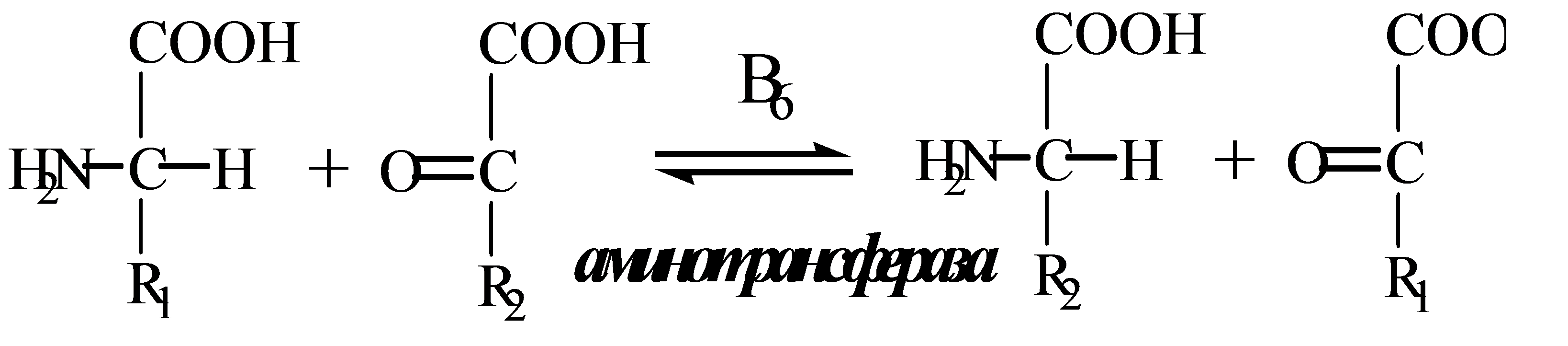Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Трансаминирование аминокислот. Аминотрансферазы, роль пиридоксальфосфата.
Трансаминирование — реакция переноса α-аминогруппы с АК на α-кетокислоту, в результате чего образуются новая α-кетокислота и новая АК. Процесс трансаминирования легко обратим, при нем общее количество АК в клетке не меняется.
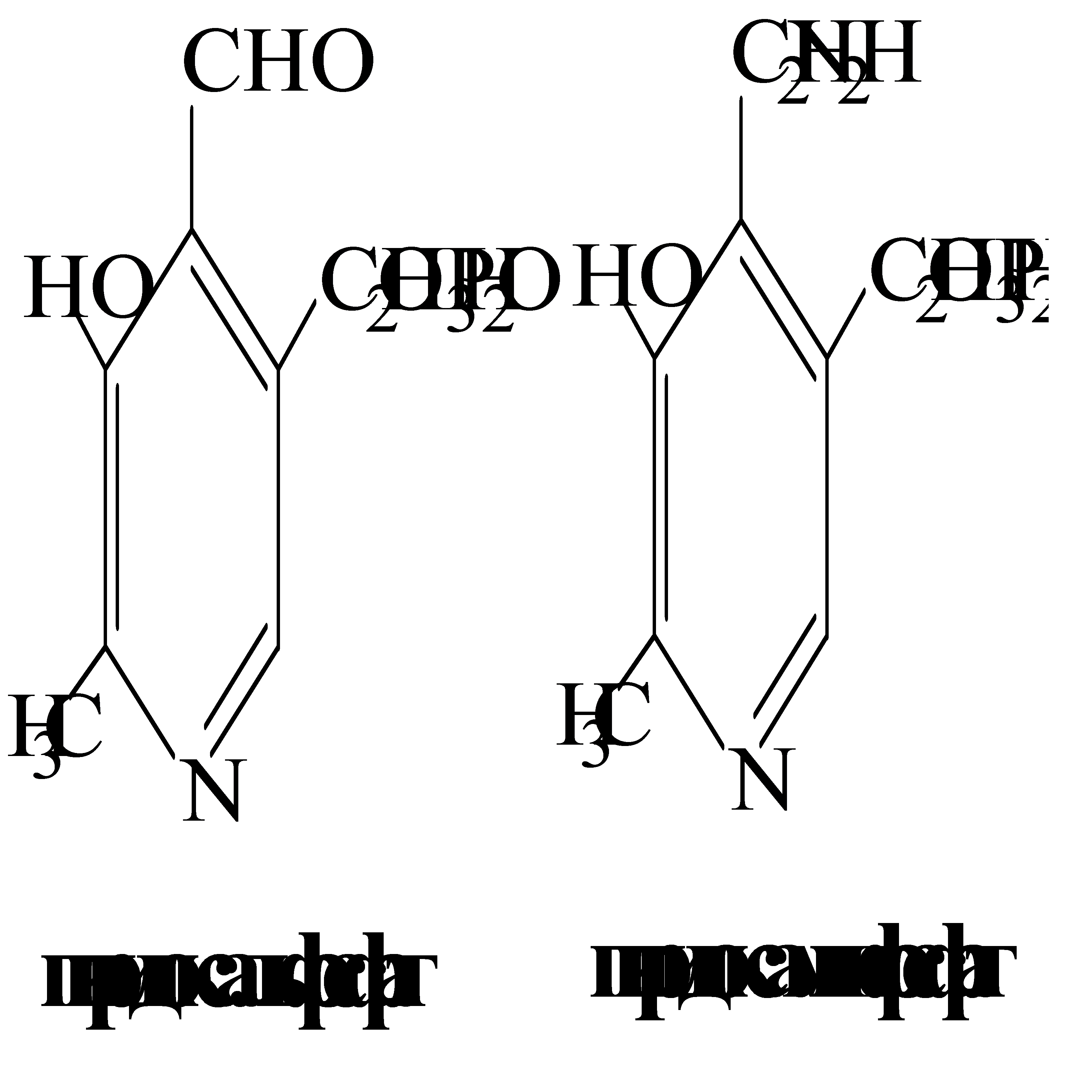
Сначала происходит обратимая реакция – перенос NH2-группы с аминокислоты на другую кетокислоту (трансаминирование). Последняя при этом превращается в аминокислоту. Механизм реакции трансаминирования достаточно сложен и протекает по принципу пинг-понг. Аминотрансферазы являются сложными ферментами, в качестве кофермента они имеют пиридоксальфосфат (активная форма витамина В6). Сначала к нему присоединяется аминокислота, превращается в кетокислоту и отделяется. Аминогруппа при этом переходит на кофермент и образуется пиридоксамин-фосфат. После этого присоединяется другая кетокислота, получает аминогруппу, образуется новая аминокислота и регенерирует пиридоксальфосфат. Роль пиридоксальфосфата сводится к образованию промежуточных соединений – шиффовых оснований (альдимин, кетимин). Трансаминирование активируется: • при поступлении в клетку избыточного количества аминокислот; • при прекращении использования аминокислот на синтез азотсодержащих соединений: белков, креатина,фосфолипидов, пуриновых и пиримидиновых оснований; • при гипогликемиях различного генеза, сахарном диабете, т.е. при внутриклеточном голодании. В результате аминокислоты теряют NH2-группы и превращаются в соответствующие кетокислоты. Далее их кетоскелет катаболизирует специфическими путями и вовлекается в цикл трикарбоновых кислот, где сгорает до СО2 и Н2О.  Представления о биосинтезе холестерина. Биосинтез Происходит в эндоплазматическом ретикулуме. Источником всех атомов углерода в молекуле является ацетил-S-КоА, поступающий сюда в составе цитрата, как и при синтезе жирных кислот. При биосинтезе холестерола затрачивается 18 молекул АТФ и 13 молекул НАДФН. Образование холестерола идет более чем в 30 реакциях, которые можно сгруппировать в несколько этапов. 1. Синтез мевалоновой кислоты 2. Синтез изопентенилдифосфата. 29 3. Синтез фарнезилдифосфата. 4. Синтез сквалена. 5. Синтез холестерола.
Регуляция синтеза холестерола Основным регуляторным ферментом является гидрооксиметилглутарил-S-КоА-редуктаза: • во-первых, по принципу обратной отрицательной связи она ингибируется конечным продуктом реакции - холестеролом. • во-вторых, ковалентная модификация при гормональной регуляции: инсулин, активируя протеинфосфатазу, способствует переходу фермента гидроокси-метил-глутарил-S=КоА-редуктазы в активное состояние. Глюкагон и адреналин посредством аденилатциклазного механизма активируют протеинкиназу А, которая фосфорилирует фермент и переводит его в неактивную форму. Задача. В больницу доставлен ребенок с явлениями отсталости в физическом и умственном развитии. В моче обнаружен фенилаланин и фенилпировиноградная кислота. Какой фермент неактивен? Напишите химизм и предложите лечение данного случая. Фенилкетонурия. Неактивен фермент фенилаланин-4-гидроксилаза. Лечение: ограничить поступление в организм фенилаланина с пищей.
17 билет |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 486. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |