
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Сила тока в электролите и анодная поляризационная криваяСтр 1 из 6Следующая ⇒ Лекция 3 Технологические параметры размерной электрохимической обработки Напряжение на электродах Напряжение, подаваемое на электроды U, (В), определяется как сумма эффективного напряжения, непосредственно затрачиваемого на анодное растворение Uэл, потери напряжения в двойных электрических слоях катода и анода DUи потери напряжения при прохождении электрического тока через заготовку DUз: U = Uэл + DU + DUз, (3.11) Потери напряжения в заготовке DUзпринимают во внимание только тогда, когда заготовка имеет большие размеры, а её конструкция не позволяет разместить токопроводы вдоль всей длины. В этом случае DUзнаходится в диапазоне 4…5 В, и его следует учитывать в расчётах. Потери напряжения в двойном электрическом слое DUопределяют как разность электродных потенциалов анода jа и катода jк с учётом значений их поляризации при прохождении электрического тока. DU = jа – jк = (jар + Djа) – (jкр + Djк). (3.12) При отсутствии точных данных по значениям jа и jк с достаточной для практических расчётов точностью принимают jа = 2,5…4 В и jк = – 1,5 В. Процесс электрохимического растворения начинается, как правило, при значениях U, превышающих суммарный потенциал поляризации электродов DU. На практике это соответствует примерно значению Uэл более 3…5 В. Большинство операций ЭХРО осуществляется при U = 9…12 В; при обработке титановых сплавов — 18…30 В.Превышение значения более 30 В приводит к возникновению электрического пробоя межэлектродного промежутка. Напряжение, необходимое для прохождения тока в электролите, а соответственно для осуществления анодного растворения, определяется формулой  Uэл = I ´Rэл, где I— сила тока в электролите, А. При этом сопротивление электролита рассчитывается по формуле
где gэл— удельная электропроводность электролита, См/м; d— межэлектродный зазор, м; Rэл— сопротивление электролита в межэлектродном промежутке, Ом; S— площадь обработки, м2. Исходя из этого эффективное напряжение, затрачиваемое непосредственно на анодное растворение Uэл (В), можно определить по формуле
Возможность использования представленных формул для расчёта значения напряжения U, которое нужно подать на электроды для реализации процесса ЭХРО, затруднено в связи со сложным характером процессов поляризации электродов при прохождения тока и нелинейным характером изменения в связи с этим значения составляющей DU. Учёт этих изменений проводят на основе изучения поляризационных катодной и анодной кривых, устанавливающих связь между напряжением U, подаваемым на электроды, и силой тока I в электролите. Сила тока в электролите и анодная поляризационная кривая Зависимость силы токаI в электролите от напряжения U на электродахпри электролизе имеет сложный характер. Связано это с тем, что процесс электролиза не является одномоментным актом, а состоит из последовательно проходящих физико-химических процессов, называемых стадиями. Каждая стадия характеризуется определённой скоростью, зависящей от напряжения на электродах. От этого напряжения существенно зависят и соотношения между скоростями процессов на отдельных стадиях. В связи с этим скорость анодного растворения материала uрустанавливается равной скорости прохождения процесса на той её стадии, скорость которой наименьшая. Поскольку скорости прохождения стадий электролиза существенно меняются и по величине, и по соотношению в зависимости от прикладываемого к электродам напряжения, вид зависимости I – U может существенно изменяться при изменении значения U.
Участок АВ на обобщённой поляризационной кривой называют активной областью ЭХРО. Точка А этой кривой соответствует равновесному электрическому потенциалу на аноде jар, при достижении которого начинается электролиз. При значениях напряжения на электродах, соответствующих участку АВ, происходит растворение материала анода.Однако сила тока здесь незначительна, а потому высокой скорости анодного растворения uр в этой зоне достичь не удаётся. Из-за низкой производительности область напряжений на участке АВ используется редко. При напряжениях на электродах, соответствующих точке В, на поверхности анода начинают образовываться устойчивые оксидные плёнки. Толщина этих плёнок на участке напряжений ВС растёт с ростом напряжения U на электродах. Появление анодных плёнок вызвано тем, что скорость образования продуктов анодного растворения при данном режиме обработки превышает скорость их удаления с поверхности заготовки и перехода в электролит. Плохо растворимые соединения вблизи анода и на его поверхности накапливаются и препятствуют взаимодействию электрода с электролитом. Сопротивление прохождению тока в связи с этим по мере роста напряжения возрастает, а сила тока I в электролите падает.Эти процессы вызывают уменьшение скорости растворения анода. Явление образования оксидных плёнок на аноде получило название «пассивация анода». Участок CDполяризационной кривой характеризуется равновесием между скоростями роста и растворения оксидной плёнки. При напряженияхjа, соответствующих этому участку, сила тока в электролите мала, процесс электрохимического растворения анода протекает медленно. Дальнейшее увеличение потенциала анода (участок DF)характеризуется разрушением оксидной плёнки, ростом силы тока и повышением скорости растворения анода. На этом участке можно получить большую силу тока I и соответственно высокую производительность обработки. Именно этот участок поляризационной кривой используют для ЭХРО. После прохождения точки Fпри обработке некоторых материалов может снова начаться уменьшение силы тока и наступить электрический пробой межэлектродного промежутка (короткое замыкание). Растворение анода при этом прекращается. В ЭХРО используют разность потенциалов между электродами в диапазоне U = 6…30 В, но при обработке струей электролита (струйная обработка, см. рис. 3.6, б) значения U повышают до 100…800 В. Для разных металлов и сплавов пассивация (точка В на рис. 3.15) наступает при различных напряжениях U, значения которых кроме того зависят от химического состава электролита, его температуры и условий течения жидкости в межэлектродном промежутке. При обработке коррозионностойких сталей и некоторых сплавов пассивация поверхности заготовки вообще не наступает, а ток растёт с ростом Uдо электрического пробоя промежутка. Такие стали и сплавы называют слабо пассивирующимися. В противоположность им титан, вольфрам и ряд сплавов этих металлов характеризуются значительной пассивацией, что приводит к повышению энергоёмкости процесса ЭХРО, снижению производительности обработки и необходимости создания условий ЭХРО, затрудняющих образование пассивирующей плёнки. В расчётах технологических параметров ЭХРО наряду с силой тока I часто используют характеристику «плотность тока» ri, которая характеризует интенсивность энергетического воздействия на заготовку и не зависит от площади обрабатываемой поверхности: ri = I/S. Обычно применяемые плотности тока находятся в диапазоне от 5 до 100 А/см2. При ri< 5 А/см2 поверхность заготовки, как правило, покрывается прочной пассивной плёнкой и процесс прекращается. В области ri>100...200 А/см2 трудно стабилизировать состав и температуру электролита в зазоре (электролит быстро насыщается продуктами реакции). При ri= 400...600 А/см2 наступают диффузионные ограничения: даже при наибольших возможных давлении и скорости прокачки электролита ионы растворившегося металла и газа не успевают отводиться от электродов и сила тока падает. |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 532. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
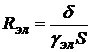 , (3.13)
, (3.13) . (3.14)
. (3.14) Для описания зависимости силы тока I в электролите от напряжения на электродах U используют поляризационные катодные и анодные кривые. Вид поляризационной кривой зависит от материала электрода и условий проведения электролиза. На рис. 3.15 приведена обобщённая анодная поляризационная кривая, учитывающая все возможные виды и стадии протекания процессов электрохимического растворения анода при электрохимической обработке, свойственные анодам, изготовленным из разных металлов.
Для описания зависимости силы тока I в электролите от напряжения на электродах U используют поляризационные катодные и анодные кривые. Вид поляризационной кривой зависит от материала электрода и условий проведения электролиза. На рис. 3.15 приведена обобщённая анодная поляризационная кривая, учитывающая все возможные виды и стадии протекания процессов электрохимического растворения анода при электрохимической обработке, свойственные анодам, изготовленным из разных металлов.