
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Определение восстанавливающей способности сахарозыРеактивы:раствор сахарозы; гидролизат сахарозы; растворы NaOH и CuSO4, 5 %; концентрированная НС1 и раствор, 25 %; резорцин. А(реакция Троммера). В две пробирки наливают по 3 мл раствора сахарозы, в первую добавляют 2 капли конц. НС1 и нагревают на кипящей водяной бане, в третью пробирку приливают 3 мл раствора гидролизата сахарозы. Во все пробирки прибавляют по 1 мл раствора щелочи, 5 капель раствора CuSO4 и нагревают на водяной бане. Отмечают наличие и цвет осадка. Б(Реакция Селиванова). В две пробирки наливают по 3 мл раствора сахарозы и гидролизата, добавляют по 1 мл раствора НС1 и несколько крупинок резорцина. Нагревают смеси на водяной бане до появления окраски.
Опыт № 3. Полисахариды Реактивы:раствор крахмала,1 %;концентрированная НС1; растворы NaOH и CuSO4, 15 и 1 % соответственно. В две пробирки помещают по 5 мл раствора крахмала. В одну добавляют 2–3 капли конц. НС1, кипятят на водяной бане 15 мин. Затем в обе пробирки добавляют по 2 мл раствора щелочи и по 5 капель раствора сульфата меди и кипятят. Отмечают наличие и окраскуосадка.
Вопросы коллоквиума:
1. Что такое инверсия и инвертный сахар? 2. Почему крахмал не проявляет восстановительных свойств? Напишите схему реакции гидролиза крахмала, укажите промежуточные и конечные продукты. 3. Напишите схему связывания концевого остатка полисахарида хондроитинсульфата с остатком серина в полипептидной цепи.
Лабораторная работа № 4 «Изучение состава нуклеиновых кислот» Нуклеиновые кислоты и нуклеопротеины играют огромную и разностороннюю роль в сохранении и передаче генетической информации и регуляции важнейших биосинтетических процессов в организме. Нуклеопротеиды – сложные белки, молекулы которых построены из простых белков (гистонов, протаминов, реже – альбуминов и глобулинов), взаимодействующих с нуклеиновыми кислотами. Нуклеопротеинами богаты печень, селезенка, почки, поджелудочная железа. Для качественного анализа их состава используют дрожжи, богатые этими сложными белками. Они растворяются в разбавленных растворах щелочей и выпадают в осадок при подкислении раствора. Продукты щелочного гидролиза нуклеопротеидов дрожжей обнаруживают специфическими качественными реакциями. 
Опыт № 1. Обнаружение белков в составе нуклеопротеидов Реактивы:гидролизат нуклеопротеидов дрожжей; раствор NaOH, 10 %; раствор CuSO4, 1 %; индикаторная бумага. В пробирку помещают 0,5 мл гидролизата, при необходимости нейтрализуют раствором щелочи, добавляют 0,5 мл раствора щелочи и 2–3 капли раствора соли меди. Смесь перемешивают. Отмечают окрашивание раствора.
Опыт № 2.Обнаружение пуриновых оснований Реактивы:гидролизатнуклеопротеидов дрожжей; аммиак конц.; раствор нитрата серебра, 1 %. К 1 мл гидролизата приливают по каплям концентрированный аммиак до получения щелочной среды (по индикаторной бумаге) и 0,5 мл раствора нитрата серебра. Через 3–5 мин отмечают выпадение осадка.
Опыт № 3. Обнаружение углеводов Реактивы:гидролизат нуклеопротеидов; дифениламиновый или орциновый реактив, 1 %. К 5 каплям щелочного раствора гидролизата добавляют 20 капель дифениламинового (орцинового) реактива. Смесь выдерживают 15 мин в кипящей водяной бане. Отмечают окрашивание раствора.
Опыт № 4. Обнаружение остатков фосфорной кислоты Реактивы:гидролизат нуклеопротеидов дрожжей; молибденовый реактив. К 1 мл гидролизата добавляют 1 мл молибденового реактива и кипятят. Отмечают окраску раствора, после охлаждения — цвет осадка фосфорнокислой соли молибдата аммония (NH4)3PO4·12MoO3·6H2O.
При оформлении отчета приводят уравнения реакций с указанием окраски растворов или осадков, отмечают выделение газообразных продуктов. Делают вывод о наличии или отсутствии компонентов в изучаемом биологическом объекте.
Вопросы коллоквиума: 1. Изобразите строение участка цепи нуклеопротеида. 2. Что такое температура плавления (Тпл) препарата ДНК? Как Тпл зависит от нуклеотидного состава?
Лабораторная работа № 5 «Физико-химические свойства липидов» Липиды — большая группа жиров и жироподобных веществ. Общим для всех этих соединений свойством является их нерастворимость в воде и растворимость в органических растворителях (бензоле, ацетоне, петролейном и диэтиловом эфире, хлороформе и т. д.). Из-за большого разнообразия химической структуры липидов их единая классификация затруднена. По химической природе липиды можно разделить на следующие группы: жиры (нейтральные жиры) или триацилглицериды; воска и воскоподобные вещества; фосфолипиды, цереброзиды; стерины и стероиды. Жиры – важный энергетический резерв организма. Содержание резервного жира в организме зависит от уровня и характера питания. Одним из наиболее распространенных классов липидов являются фосфолипиды (фосфатиды). Они являются структурными компонентами клеточных мембран, особенно много их содержится в клетках нервных тканей. Фосфолипиды можно рассматривать как несимметричные диэфиры фосфорной кислоты. К ним относят глицерофосфолипиды (лецитины, фосфа-тидилэтаноламины, фосфатидилсерины и др.), инозитфосфатиды и сфинго-фосфолипиды. Сухие фосфолипиды хорошо растворимы в алифатических и ароматических углеводородах, их галогенпроизводных и в некоторых полярных растворителях.
Опыт № 1. Качественные реакции на жиры Растворимость жиров Реактивы и оборудование: растительное масло; твердый жир; диэтиловый эфир; ацетон; этанол; дистиллированная вода; предметные стекла. На четыре предметных стекла наносят по капле растительного масла или небольшому кусочку твердого жира. На первое стекло наносят две–три капли дистиллированной воды, второе – столько же диэтилового эфира, третье – ацетона, четвертое – этанола. Все капли перемешивают палочкой и сравнивают растворимость жиров. Эмульгирование жирных масел Реактивы и оборудование: растительное масло; карбонат натрия, 2%-й раствор; мыло, 2%-й раствор; желчь; дистиллированная вода; пробирки; воронки с бумажными фильтрами. В четыре пробирки вносят по 5 капель масла В первую пробирку добавляют 2 мл воды, во вторую – 2 мл раствора карбоната натрия, в третью– 2 мл раствора мыла, в четвертую – 2 мл воды и несколько капель желчи. Пробирки взбалтывают и наблюдают образование эмульсий. Затем содержимое пробирок фильтруют через бумажные фильтры в другие пробирки. Отмечают содержимое фильтрата. Определение глицерина в жирах Реактивы: растительное масло или животный жир; кислый сернокислый калий (или натрий)или борная кислота; нитрат серебра, 1 %-й раствор. В сухую пробирку вносят несколько капель растительного масла или кусочек животного жира, добавляют на кончике шпателя порошка калия кислого сернокислого (или борной кислоты) и осторожно подогревают. Отмечают выделение и запах паров (можно поднести к отверстию пробирки кусочек бумаги, смоченной аммиачным раствором нитрата серебра).
Омыление жира Реактивы и оборудование: растительное масло или животный жир; КОН, 30%-й спиртовый раствор; CaCl2, 5%-й раствор; дистиллированная вода; пробирка со шлифом; обратный холодильник; водяная баня. В пробирку вносят 0,5 мл растительного масла или 0,5 г животного жира и добавляют 5–7 мл спиртового раствора КОН. Пробирку соединяют с обратным холодильником и нагревают на водяной бане в течение 30 мин, после чего в пробирку наливают горячую воду. После охлаждения отбирают в другую пробирку 2–3 мл полученного раствора и добавляют 1 мл раствора CaCl2. Отмечают произошедшие изменения.
Вопросы коллоквиума: 1. Назовите липиды: А) Б)
2. Какое количество энергии выделяется при окислении 1 г жира? Ответ подтвердите расчетами.
Лабораторная работа № 6 «Ферменты. Изучение их свойств» 6.1. Амилаза и ее свойства Амилаза – фермент, вырабатываемый слюнными железами, катализи-рует гидролиз α - 1,4 - гликозидной связи крахмала и гликогена до промежуточных продуктов (декстринов). Крахмал с иодом дает соединение синего цвета, амилодекстрин — красно-бурого, ахродекстрин — желтого.
Опыт №1. Действие амилазы Реактивы:раствор крахмала, 1 %;раствор иода, 0,1 % в 0,2 %-м растворе KJ; раствор слюны (рот ополаскивают 2–3 раза для удаления остатков пищи, отмеряют цилиндром 25–30 мл дистиллированной воды и ополаскивают ею рот в течение 3–5 мин в несколько приемов. Собранную жидкость фильтруют через вату. Фильтрат используют в качестве источника фермента). Оборудование:штатив с пробирками, пипетки. В две пробирки вносят по 5 мл раствора крахмала, в одну добавляют 0,5 мл раствора слюны, хорошо перемешивают и дают постоять. Через 15 мин в обе пробирки прибавляют по 5 капель раствора иода. Отмечают окраску растворов. Опыт № 2. Влияние температуры на активность амилазы Реактивы:препарат слюны; раствор крахмала, 1 %; раствор J2, 0,1 % в 0,2 %-ом растворе KJ; лед. Оборудование:пробирки, пипетки, предметные стекла, водяная баня, термостат. В четыре пробиркиналивают по 5 мл раствора крахмала. Первую помещают в кипящую водяную баню, вторую — в термостат при 40 0С, третью оставляют при комнатной температуре, четвертую ставят на лед. Через 10–15 мин во все пробирки прибавляют по 1 мл препаратаслюны и перемешивают палочкой. Гидролиз крахмала наблюдают по реакции с иодом. На стекла наносят несколько капель раствора иода и смешивают их с каплями смеси, которую отбирают из каждой пробирки, находящейся в вышеуказанных условиях, через 1; 2; 4; 6; 8; 10 и 12 мин (желательно отбирать одинаковое во всех опытах число капель). По изменению степени окрашивания раствора крахмала с иодом судят о степени гидролиза в каждой пробирке. Опыт № 3. Влияние рН среды на активность амилазы Реактивы:препарат слюны; раствор крахмала, 1 %; раствор иода, 0,1 % в 0,2 %-ом растворе KJ; раствор Na2HPO4 , 0,2 М; раствор NaH2PO4, 0,2 М; фосфат-ные буферные растворы с различными значениями рН. Оборудование:пробирки, термостат, рН-метр (используют для измерения рН приготовленных растворов).
Состав фосфатных буферных растворов
В семь пробирок наливают по 2 мл буферного раствора с различным значением рН. Затем добавляют по 5 мл раствора крахмала и по 1 мл раствора слюны. Содержимое перемешивают и помещают в термостат на 10 мин при температуре 38 0С. Затем во все пробирки добавляют по 5 капель раствора иода, перемешивают и наблюдают окраску растворов (для наглядности в каждую пробирку можно добавить немного дистиллированной воды и перемешать). Опыт № 4. Влияние активаторов и ингибиторов на активность амилазы Реактивы:препарат слюны; раствор крахмала, 0,5 %; раствор иода, 0,1 % в 0,2 %-ом растворе KJ; растворы NaCl и CuSO4, 1 %. Оборудование:пробирки, термостат. В первую из трех пробирок наливают 2,5 мл воды, во вторую –2 мл воды и 0,5 мл раствора NaCl, в третью – 2 мл воды и 0,5 мл раствора CuSO4. Во все пробирки вносят по 2,5 мл раствора слюны и 2,5 мл раствора крахмала, перемешивают и термостатируют при 38 0С. Через 5 мин прибавляют по 5 капель раствора иода. Отмечают изменение окраски.
При оформлении отчета делают вывод о механизме действия фермента и объясняют действие на него изученных факторов.
Вопросы коллоквиума: 1. Что такое активный центр фермента? Каков механизм его действия? 2. Какие факторы влияют на ферментативную активность? Ответ поясните. 3. Установите соответствие:
Уреаза и ее свойства Уреаза ускоряет расщепление мочевины до аммиака и углекислого газа. По изменению рН раствора в щелочную область судят о ее действии. Уреаза – высокоспецифичный фермент: незначительные изменения в структуре субстрата приводят к тому, что фермент не оказывает действия на этот субстрат.
Опыт № 1. Действие уреазы Реактивы:препарат уреазы (готовят суспензию из 30–40 растертых без кожуры арбузных семян в 50 мл воды); раствор мочевины, 5 %; раствор фенолфталеина, 1 %. Оборудование:пробирки, пипетки, ступка с пестиком. В две пробирки наливают по 1 мл раствора мочевины и 5 капель раствора фенолфталеина. В одну пробирку добавляют 5 мл препарата уреазы, перемешивают. Отмечают окраску растворов. Опыт № 2. Влияние температуры на активность уреазы Реактивы: как в опыте № 1, лед. Оборудование:пробирки, пипетки, электроплитка. В три пробирки наливают по 3 мл препарата уреазы. В первой пробирке раствор кипятят 5 мин. Затем во все пробирки приливают по 1 мл раствора мочевины и по 5 капель раствора фенолфталеина. Вторую пробирку ставят на лед, третью выдерживают при температуре 20–25 0С. Отмечают интенсивность окраски индикатора во всех пробирках. Опыт № 3. Специфичность действия уреазы Реактивы и оборудование:какв опыте № 1; раствор тиомочевины, 5 %; раствор ацетамида, 1%. В три пробирки наливают по 5 мл препарата уреазы и по 5 капель раствора фенолфталеина. В первую пробирку добавляют 1 мл раствора мочевины, во вторую – 1 мл раствора тиомочевины, в третью – 1 мл раствора ацетамида. Через 20 мин отмечают окраску в пробирках. Опыт № 4. Определение активности уреазы Реактивы:препарат уреазы; раствор мочевины, 2 %; раствор HgBr2, 0,1 %; раствор HCl, 0,1 н.; метиловый красный, 0,05 %-ый спиртовый раствор. Оборудование: колбы конические емк. 100 мл, пипетки, градуированные пробирки, бюретка, электроплитка. В две колбы вносят по 10 мл препарата уреазы. Одну из них (контроль) нагревают до кипения. Затем в обе колбы приливают по 5 мл раствора мочевины, перемешивают и термостатируют 30 мин при 20 0С. Прибавляют по 10 капель раствора метилового красного, 2 мл раствора HgBr2 . Выделив-шийся аммиак титруют 0,1 н. раствором HCl ( 1 мл 0,1 н. раствора HCl соответствует 1,4 мг азота). Единица уреазного действия — количество фермента, которое способно образовывать из мочевины 1 мг азота аммиака в течение 5 мин при 20 0С и рН 7,0. Действие уреазы на мочевину в буферном растворе описывается уравнением нулевого порядка где Х — количество расщепленной мочевины, t — время действия фермента. Тогда активность уреазы, выраженную через количество расщепившейся мочевины, рассчитывают по формуле
где V1 и V2 – результаты титрования раствором 0,1 н. HCl исследуемого и контрольного образцов, мл; V – количество мочевины в пробах; F – поправка на титр раствора; t – время действия фермента, мин; Q – количество азота, соответствующее 1 мл 0,1 н. раствора HCl, мл.
При оформлении отчета делают вывод о механизме действия фермента и объясняют действие на него изученных факторов.
Вопросы коллоквиума: 1. Что такое активный центр фермента? Каков механизм его действия? 2. Какие факторы влияют на ферментативную активность? Ответ поясните. 3. Установите соответствие:
|
|||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 463. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
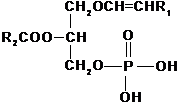
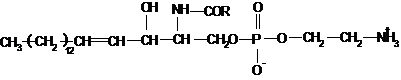
 ,
,
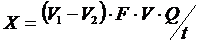 ,
,