
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Билет № 9 Атомистические гипотезы строения вещества. Идеальный газ. Основное уравнение МКТ. Абсолютная температура как мера средней кинетической энергии молекул.Атомистическая теория — современная теория строения вещества — зародилась еще в Древней Греции. Основное направление мысли древнегреческих философов основывалось на представлении о непрерывности материи (взгляд Аристотеля). Однако некоторые древнегреческие философы, особенно Демокрит, не соглашались с такой точкой зрения и считали, что материя состоит из мельчайших неделимых частиц. Демокрит называл их атомами, что значит “неделимые”. То, что вещество состоит из Идеальный газ — это физическая модель реального газа, взаимодействие, между молекулами которого пренебрежимо мало.Модель введена для математического описания поведения газов. Реальные разреженные газы (верхние слои атмосферы) ведут себя как идеальный газ. · молекулы — это упругие шары; · расстояние между молекулами намного больше размеров молекул- диаметра (r>d); · силы отталкивания возникают только при их соударении; · движение молекул подчиняется законам Ньютона; · давление газа на стенки сосуда оказывается за счет ударов молекул газа.
 Основное уравнение МКТ идеального газа связывает микропараметры частиц ( массу молекулы, средний квадрат скорости молекул) с макропараметрами газа (р — давление, V — объем, Т — температура). Температура характеризует степень нагретости тела, тепловое равновесие, указывает направление теплообмена. Измеряют температуру термометром.При измерении температуры используется зависимость изменения какого-либо макроскопического параметра (объема, давления, электрического сопротивления и т.д.) вещества от температуры. В жидкостных термометрах — это изменение объема жидкости. В процессе измерения температура тела и термометра приходят в состояние теплового равновесия.
Абсолютная шкала температур введена англ. физиком У. Томсоном(Кельвином). Ее называют шкалой Кельвина или термодинамической температурной шкалой. В ней нет отрицательных температур. Абсолютная шкала температуры называется так, потому что мера нижнего предела температуры — абсолютный ноль, то есть наиболее низкая возможная температура, при которой молекулы вещества перестают двигаться. Единица абсолютной температуры в СИ: [T]=1K (Кельвин). Нулевая температура абсолютной шкалы – это абсолютный ноль 00К = −273.15 °C (точно). По величине 1К = 10С. Шкала температур Кельвина — это шкала, в которой начало отсчёта ведётся от абсолютного нуля. В формулах абсолютная температура обозначается буквой «Т», а температура по шкале Цельсия буквой «t». T = t+273(K). |
||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 4208. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 мельчайших частиц – молекул и атомов экспериментально доказывают броуновское движение и явление диффузия.
мельчайших частиц – молекул и атомов экспериментально доказывают броуновское движение и явление диффузия.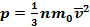 или
или 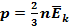 — выражения основного уравнения МКТ, где р — давление газа на стенки сосуда (Па); n — концентрация молекул, т.е. число молекул в единице объема n=N/V, ( 1/м3); m0 — масса одной молекулы (кг);
— выражения основного уравнения МКТ, где р — давление газа на стенки сосуда (Па); n — концентрация молекул, т.е. число молекул в единице объема n=N/V, ( 1/м3); m0 — масса одной молекулы (кг); 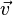 — средняя квадратичная скорость движения газовых молекул (м/с); ρ — плотность газа (кг/м3);
— средняя квадратичная скорость движения газовых молекул (м/с); ρ — плотность газа (кг/м3); 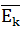 — средняя кинетическая энергия молекул (Дж).
— средняя кинетическая энергия молекул (Дж).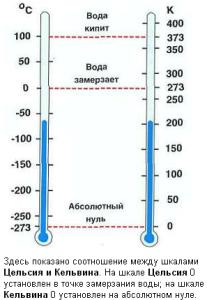
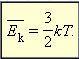 —средняя кинетическая энергия поступательного движения молекул, где
—средняя кинетическая энергия поступательного движения молекул, где 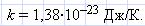 — постоянная Больцмана, устанавливает связь между энергетическими и температурными единицами.
— постоянная Больцмана, устанавливает связь между энергетическими и температурными единицами.