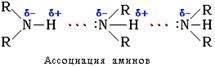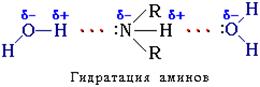Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
ФИЗИЧЕСКИЕ СВОЙСТВА АМИНОВ.Стр 1 из 2Следующая ⇒ АМИНЫ Амины– органические производные аммиака NH3, в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы: R-NH2, R2NH, R3N
Простейший представитель – метиламин:
Строение Атом азота находится в состоянии sp3-гибридизации, поэтому молекула имеет форму тетраэдра. Также атом азота имеет два неспаренных электрона, что обуславливает свойства аминов как органических оснований.
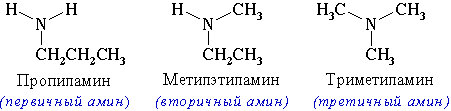
КЛАССИФИКАЦИЯ АМИНОВ. По количеству и типу радикалов, связанных с атомом азота:
НОМЕНКЛАТУРА АМИНОВ. 1. В большинстве случаев названия аминов образуют из названий углеводородных радикалов и суффикса амин. Различные радикалы перечисляются в алфавитном порядке. При наличии одинаковых радикалов используют приставки ди и три. CH3-NH2 Метиламин СH3CH2-NH2 Этиламин CH3-CH2-NH-CH3 Метилэтиламин (CH3)2NH Диметиламин
2. Первичные амины часто называют как производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на аминогруппы -NH2. В этом случае аминогруппа указывается в названии приставкой амино-: CH3-CH2-CH2-NH2 1-аминопропан H2N-CH2-CH2-CH(NH2)-CH3 1,3-диаминобутан
Символ N- ставится перед названием алкильного радикала, чтобы показать, что этот радикал связан с атомом азота, а не является заместителем в бензольном кольце.  ИЗОМЕРИЯ АМИНОВ 1) углеродного скелета,начиная с С4H9NH2: СН3-СН2- СН2-СН2 –NH2 н-бутиламин (1-аминобутан)
CH3-CH- СН2-NH2 изо-бутиламин (1-амин-2-метилпропан) │ СН3 2) положения аминогруппы, начиная с С3H7NH2: СН3-СН2- СН2-СН2 –NH2 1-аминобутан (н-бутиламин)
CH3-CH- СН2-СH3 2-аминобутан (втор-бутиламин) │ NН2 3) изомерия между типами аминов –первичный, вторичный, третичный:
ФИЗИЧЕСКИЕ СВОЙСТВА АМИНОВ. Первичные и вторичные амины образуют слабые межмолекулярные водородные связи:
Это объясняет относительно более высокую температуру кипения аминов по сравнению с алканами с близкой молекулярной массой. Например:
Третичные амины не образуют ассоциирующих водородных связей (отсутствует группа N–H). Поэтому их температуры кипения ниже, чем у изомерных первичных и вторичных аминов:
По сравнению со спиртами алифатические амины имеют более низкие температуры кипения, т.к. в спиртах водородная связь более прочная:
При обычной температуре только низшие алифатические амины CH3NH2, (CH3)2NH и (CH3)3N – газы (с запахом аммиака), средние гомологи – жидкости (с резким рыбным запахом), высшие – твердые вещества без запаха.
Ароматические амины – бесцветные высококипящие жидкости или твердые вещества.
Амины способны к образованию водородных связей с водой:
Поэтому низшие амины хорошо растворимы в воде. С увеличением числа и размеров углеводородных радикалов растворимость аминов в воде уменьшается, т.к. увеличиваются пространственные препятствия образованию водородных связей. Ароматические амины в воде практически не растворяются.
ПОЛУЧЕНИЕ АМИНОВ. |
||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 411. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
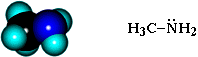
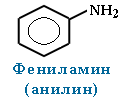
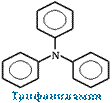
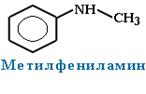
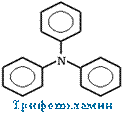
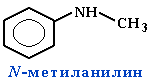 Для смешанных аминов, содержащих алкильные и ароматические радикалы, за основу названия обычно берется название первого представителя ароматических аминов анилин.
Для смешанных аминов, содержащих алкильные и ароматические радикалы, за основу названия обычно берется название первого представителя ароматических аминов анилин.