
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Материальный баланс адсорбции.Стр 1 из 9Следующая ⇒ АДСОРБЦИЯ Адсорбцией называют процесс поглощения вещества из смеси газов, паров или растворов поверхностью или объемом пар твердого тела - адсорбента. Поглощаемое вещество, находящееся в газе, паре называется адсорбтивом, а поглощенное - адсорбатом. Адсорбцию подразделяют на два вида: физическую и химическую. Физическая адсорбция обусловлена поверхностными вандервальсовыми силами, удерживающими на поверхности адсорбента несколько слоев молекул адсорбата. При химической адсорбции поглощаемое вещество вступают в химическое взаимодействие с адсорбентом с образованием на его поверхности химических соединений. Силы притяжения возникает на поверхности адсорбента благодаря тому, что силовое поле поверхностных атомов и молекул не уравновешено силами взаимодействия соседних частиц. Заполнение адсорбатом поверхности адсорбента частично уравновешивает поверхностные силы и уменьшает поверхностное натяжение. Это в конечном счете приводит к выделению тепла. Следовательно, процессы адсорбции экзотермичны. Процессы адсорбции избирательны и обратимы (десорбция). Адсорбция – применяется в главным образом при небольших концентрациях поглощаемого вещества в исходной смеси, когда требуется достичь практически полного извлечения адсорбтива. В тех случаях, когда концентрация извлекаемого вещества в исходной смеси велика, обычно выгоднее использовать абсорбцию. Частным случаем хемосорбции является ионный обмен между твердым ионообменным сорбентом и раствором электролита. Кинетика, а также аппаратурное оформление ионообменных процессов близки к адсорбционным. 
Адсорбенты. Адсорбенты - пористые тела, обладающие большим объемом микропор. В адсорбентах основное количество поглощенного вещества сорбируется на стенках микропор (r< Поглотительная (адсорбционная) способность адсорбентам- максимально возможная концентрация адсорбтива в единице массы или объема адсорбента. Максимально возможную в данных условиях поглотительная способность адсорбента называют равновесной активностью. Статическая активность (Аст)- количество вещества, поглощенного единицей массы адсорбента от начало до равновесия при статических условиях, динамическая активность (Адин) - при движении смеси через слой адсорбента. Как показывают эксперименты Аст > Адин . Однако расчеты ведут по Адин. По химическому составу адсорбенты можно разделить на углеродные и не углеродные. Углеродные - активные угли, углеродные волокнистые материалы, некоторые виды твердого топлива. Удельная поверхность активных углей очень высока и составляет (6 ÷17)· Неуглеродные – силикагели, активный оксид алюминия, алюмогели, цеолиты, глинистые породы. Удельная поверхность селикагеля составляет - (4÷8)· 4 · Глинистые породы применяют для очистки жидкостей от различных примесей.
6.2 Равновесие при адсорбции. Равновесная концентрация
Или, в случае адсорбции газов:
Здесь с – концентрация адсорбтива в объемной сплошной фазе, р– парциальное давление адсорбтива в объемной фазе. Зависимость Равновесные зависимости описываются рядом эмпирических и теоретических уравнений. Одна из них уравнение Лангмюра:
Здесь Изотермы адсорбции обычно определяются опытным путем.
Рис.6.1. Изотермы адсорбции: 1 – изотерма Лангмюра, 2,3,4 – реальные изотермы (2 – линейная, 3 – вогнутая, 4 – выпуклая).
Адсорбция сопровождается уменьшением парциального давления поглощаемого компонента из газовой смеси и заметным выделением тепла. Поэтому количество адсорбированного вещества возрастает с понижением температуры и повышением давления (рис.6.2).
Рис.6.2. Изотермы адсорбции для одного вещества при различных температурах:
Материальный баланс адсорбции. Характер протекания процесса во времени зависит от того, проводится процесс периодически или непрерывно. Для периодических процессов – адсорбент неподвижен, непрерывных – движется (псевдоожиженный или плотный слой). В аппаратах с неподвижным слоем адсорбента поток сплошной фазы, содержащий адсорбтив, периодически проходит через зернистый слой адсорбента. При составлении материального баланса для этого случая упростим задачу: допустим, что сплошная фаза движется в режиме МИВ в изотермических условиях. Рассмотрим элемент слоя, имеющий площадь поперечного сечения S и высоту dx: - объем сплошной фазы εSdx (ε- пористость), - объем дисперсной фазы (1-ε)Sdx, - с - концентрация адсорбента в сплошной фазе, - ст - концентрация абсорбента в дисперсной фазе.
конвективный поток диффузионный поток абсорбтива абсорбтива
Сплошной поток (газ) входит в элемент при концентрации абсорбтива с, а выходит при концентрации
молекулярный поток в элемент:
Сумма молекулярного и конвективного потоков в элемент будет равна скорости изменения массы целевого компонента в данном объеме (в элемент):
Сокращаем на Sdx получим:
Полученное уравнение справедливо (6.7) для МИВ, но в реальных условиях это не выполняется. Поэтому D меняем на DL – коэффициент продольного перемешивания. При использования концентрации в твердой фазе Х выраженной в кг/кг чистого абсорбента, последнее уравнение принимает вид:
Здесь ст=Х В последнем уравнение два неизвестных Х(х,t) и с(х,t), поэтому для получения замкнутой системы уравнений уравнение материального баланса дополняют уравнением кинетики:
где f- удельная внешняя поверхность твердой фазы м2/м3 ,Кс-коэффициент массопередачи К уравнениям материального баланса (6.8) и кинетики (6.9) необходимо добавить уравнение изотермы адсорбции:
Система уравнений (6.8) – (6.10) описывают процесс адсорбции в аппаратах с неподвижным слоем адсорбента.
|
|||||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 380. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 м). Количество остальных пор, более крупных, сводится к транспортированию адсорбтива к макропорам.
м). Количество остальных пор, более крупных, сводится к транспортированию адсорбтива к макропорам.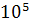
 . Недостаток активных углей их горючесть.
. Недостаток активных углей их горючесть. , алюмогели - до
, алюмогели - до (
(  чистого адсорбента) поглощаемого вещества в адсорбенте может быть представлена:
чистого адсорбента) поглощаемого вещества в адсорбенте может быть представлена: , (6.1)
, (6.1) , (6.2)
, (6.2)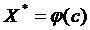 или
или  при T=const называется изотермой адсорбции.
при T=const называется изотермой адсорбции. (6.4)
(6.4) - предельная величина адсорбции, при полном заполнение внутренних пор мономолекулярным слоем адсорбата, b- константа, зависящая от температуры (рис.6.1)
- предельная величина адсорбции, при полном заполнение внутренних пор мономолекулярным слоем адсорбата, b- константа, зависящая от температуры (рис.6.1)

 .
. х
х 
 выход из элемента
выход из элемента





 dx
dx
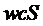
 вход в элемент
вход в элемент . При этом реализуется конвективный поток в элемент:
. При этом реализуется конвективный поток в элемент: ; (6.4)
; (6.4) . (6.5)
. (6.5) (6.6)
(6.6) (6.7)
(6.7) (6.8)
(6.8) ,
,  - насыпная плотность твердой фазы кг/м3.
- насыпная плотность твердой фазы кг/м3. (6.9)
(6.9) (6.10)
(6.10)