
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ (МВС)В основе два положения: - ковалентная химическая связь образуется двумя электронами с противоположно направленными спинами, причем эта пара электронов принадлежит двум атомам; - ковалентная связь тем прочнее, чем больше степень перекрывания взаимодействующих электронных облаков. МВС введено понятие валентности, которая определяется числом неспаренных электронов, и объяснена переменная валентность многих элементов. МВС предложены два механизма образования ковалентной связи: - обменный, при котором каждый атом предоставляет для образования связи один неспаренный электрон; - донорно-акцепторный, при котором один атом (донор) предоставляет для образования связи пару электронов, а другой атом (акцептор) – свободную орбиталь. МВС введено понятие гибридизации атомных орбиталей – смешении их и выравнивании по форме и энергии. В соответствии с экспериментальными данными считают, что не происходит гибридизации атомных орбиталей центрального атома в следующих молекулах: H2S, PH3, PHal3, AsH3, AsHal3, SbH3, SbHal3. Согласно МВС существует два способа перекрывания атомных орбиталей: - вдоль линии связи – образуется σ-связь(при перекрывании s-орбиталей и рх-орбиталей); - по обе стороны от линии связи – образуется π-связь(при перекрывании рy-орбиталей и рz-орбиталей). МВС предложен метод определения пространственной структуры молекул, которая определяется взаимодействием связывающих электронных пар молекулы друг с другом и неподеленными (несвязывающими) парами электронов центрального атома.
Определение геометрической формы молекул и ионов
 Пример: Определить тип гибридизации атома серы и пространственную структуру молекулы SO2. Решение: 1. Определить валентности элементов и записать структурную формулу молекулы: валентность атома серы (IV), кислорода (II) ; структурная формула: О=S=О. 2. Составить электронно-графическую формулу валентного уровня атома серы:
3d __ __ __ __ __
Чтобы атом серы мог проявить валентность IV, у него должно быть 4 неспаренных электрона, что достигается при переходе одного электрона с 3p-подуровня на свободную орбиталь 3d-подуровня. 3. Определить число гибридных орбиталей атома серы, которое определяется суммой числа σ-связей и числа неподеленных пар электронов на валентном уровне атома серы. Атом серы образует 2 σ-связи с атомами кислорода и имеет одну неподеленную пару электронов, то есть число гибридных орбиталей равно 3. Отсчитываем три орбитали, начиная с 3s-орбитали и определяем, что тип гибридизации sр2. 4. Так для образования треугольника в молекуле SO2 не хватает одной вершины, пространственная структура – угловая. Практические задания 3.1. Составьте электронную и электронно-графическую формулы элементов: Са, Al, Hf. Используя только Периодическую систему элементов Д.И. Менделеева, дайте характеристику элементов по указанному плану. 3.2. Объясните два механизма образования связи на примере частиц РН3 и РН4+ . 3.3. Объясните два механизма образования связи на примере частиц ВF3 и ВF4-. 3.4. Определите возможные валентности атома хлора, фосфора, углерода. 3.5. Определить тип гибридизации и геометрическую форму молекулы (иона): BeF2, AlF3, SiCl4, SO3, SO42-. 3.6. Определить тип гибридизации и геометрическую форму молекулы (иона): Н2О, NH3, SiCl4, CO2, SO32-. 3.7. Определить тип гибридизации и геометрическую форму молекулы (иона): ClO3-, ClO-, РН3.
|
||||||||||||
|
Последнее изменение этой страницы: 2018-06-01; просмотров: 304. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
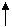
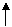
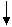 3p __ __ __
3p __ __ __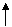
 3s __
3s __