Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Первый класс ферментов: тип катализируемых реакций, химическая природа коферментов. Основные группы, представители.
Ферменты катализируют окислительно-восстановительные реакции, лежащие в основе биологического окисления. Класс насчитывает 22 подкласса (около 480 ферментов). Коферменты: 1) Никотинамидные (НАД, НАДФ) 2) Флавиновые (ФМН, ФАД) 3) Металлопорфириновые (геммы a,b,c,d) 4) Хинонкоферменты (убихинон, пластохинон) 5) Пептидные (глутатион) 6) Липоевая кислота. Наиболее распространены следующие подклассы оксидоредуктаз: 1. Дегидрогеназы – оксидоредуктазы, катализирующие дегидрирование субстрата с использованием в качестве акцептора водорода любых молекул, кроме кислорода.(лактат-дг, сукцинат-дг) 2. Если перенос водорода от молекулы донора трудно доказуем, то такие оксидоредуктазы называют редуктазами. 3. Оксидазы – оксидоредуктазы, катализирующие окисление субстратов с молекулярным кислородом в качестве акцептора электронов без включения кислорода в молекулу субстрата.(ксантиноксидаза) 4. Монооксигеназы – оксидоредуктазы, катализирующие внедрение одного атома кислорода в молекулу субстрата с молекулярным кислородом в качестве донора кислорода. 5. Диоксигеназы – оксидоредуктазы, катализирующие внедрение 2 атомов кислорода в молекулу субстрата с молекулярным кислородом в качестве донора кислорода. 6. Пероксидазы – оксидоредуктазы, катализирующие реакции с пероксидом водорода в качестве акцептора электронов.
2.Окислительное декарбоксилирование пирувата: последовательность реакций и биоэнергетический эффект. Превращение пирувата в ацетил-КоА включает 5 стадий.
Стадия I.Пируват соединяется с ТДФ в составе Е1 и подвергается декарбоксилированию. В результате этой реакции образуется производное ТДФ с гидроксиэтильной группой при тиазоловом кольце.  Стадия П.Дигидролипоилтрансацетилаза (Е2) катализирует перенос атома водорода и ацетильной группы от ТДФ на окисленную форму липоиллизиновых групп с образованием ацетилтиоэфира липоевой кислоты. Стадия III.На стадии III КоА взаимодействует с ацетильным производным Е2, в результате чего образуются ацетил-КоА и полностью восстановленный липоильный остаток, простетическая группа Е2. Стадия IV.На стадии IV дигидролипоилде-гидрогеназа (Е3) катализирует перенос атомов водорода от восстановленных липоильных групп на FAD - простетическую группу фермента Е3. Стадия V. На стадии V восстановленный FADH2 передаёт водород на NAD+ с образованием NADH. Окислительное декарбоксилирование пирувата сопровождается образованием NADH, поставляющим электроны в дыхательную цепь и обеспечивающим синтез 3 молей АТФ на 1 моль пирувата путём окислительного фосфорилирования. Так же ацетил-Коа, образующийся в ходе декарбоксилирования пирувата, окисляется в дальнейшем в ЦТК с образованием 12 АТФ.
3.Пантотеновая кислота, химическая структура и влияние на обмен веществ.
Пантотеновая кислота состоит из остатков D-2,4-дигидрокси-3,3-диметилмасляной кислоты и β-аланина, соединённых между собой амидной связью: Она синтезируется растениями и микроорганизмами, содержится во многих продуктах животного и растительного происхождения (яйцо, печень, мясо, рыба, молоко, дрожжи, картофель, морковь, пшеница, яблоки). В кишечнике человека пантотеновая кислота в небольших количествах продуцируется кишечной палочкой. Суточная потребность: 10-12 мг. Биологические функции.Пантотеновая кислота используется в клетках для синтеза коферментов: 4-фосфопантотеина, кофермента пальмитоилсинтазы и КоА, который участвует в переносе ацильных радикалов в реакциях общего пути катаболизма, активации жирных кислот, синтеза холестерина и кетоновьж тел, синтеза ацетилглюкозаминов, обезвреживания чужеродных веществ в печени. Клинические проявления недостаточности витамина: дерматиты, дистрофические изменения желёз внутренней секреции, нарушение деятельности нервной системы (невриты, параличи), дистрофические изменения в сердце, почках, депигментация и выпадение волос, потеря аппетита, истощение.
4. Задача. У больного с мочой за сутки выделяется 1,5 г мочевой кислоты (норма до 0,7 г), повышено ее содержание и в крови. Врач назначил лечебный препарат гипоксантин, рекомендовал ограничить мясную пищу. Какую болезнь вы диагностируете? Принцип действия гипоксантина.
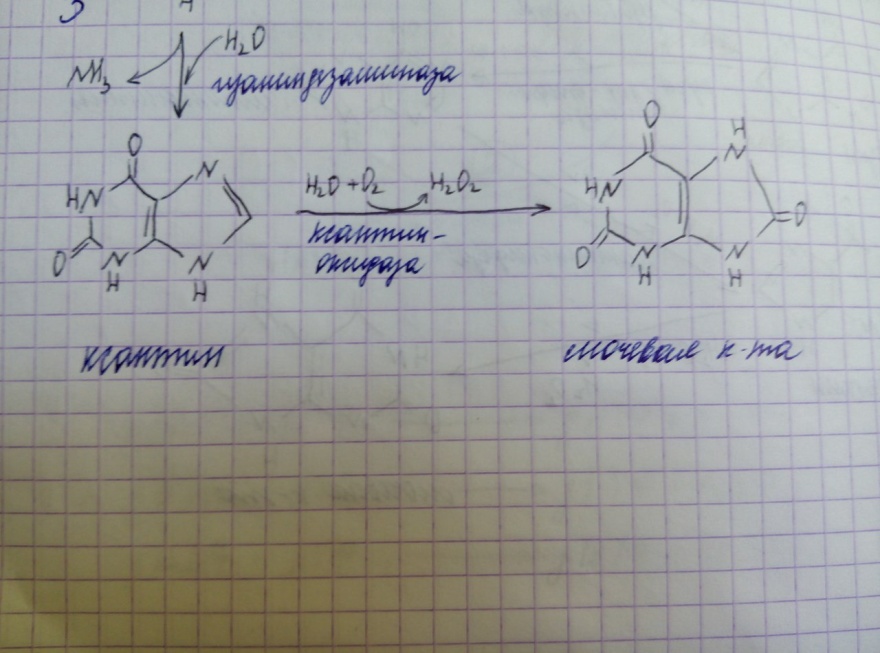
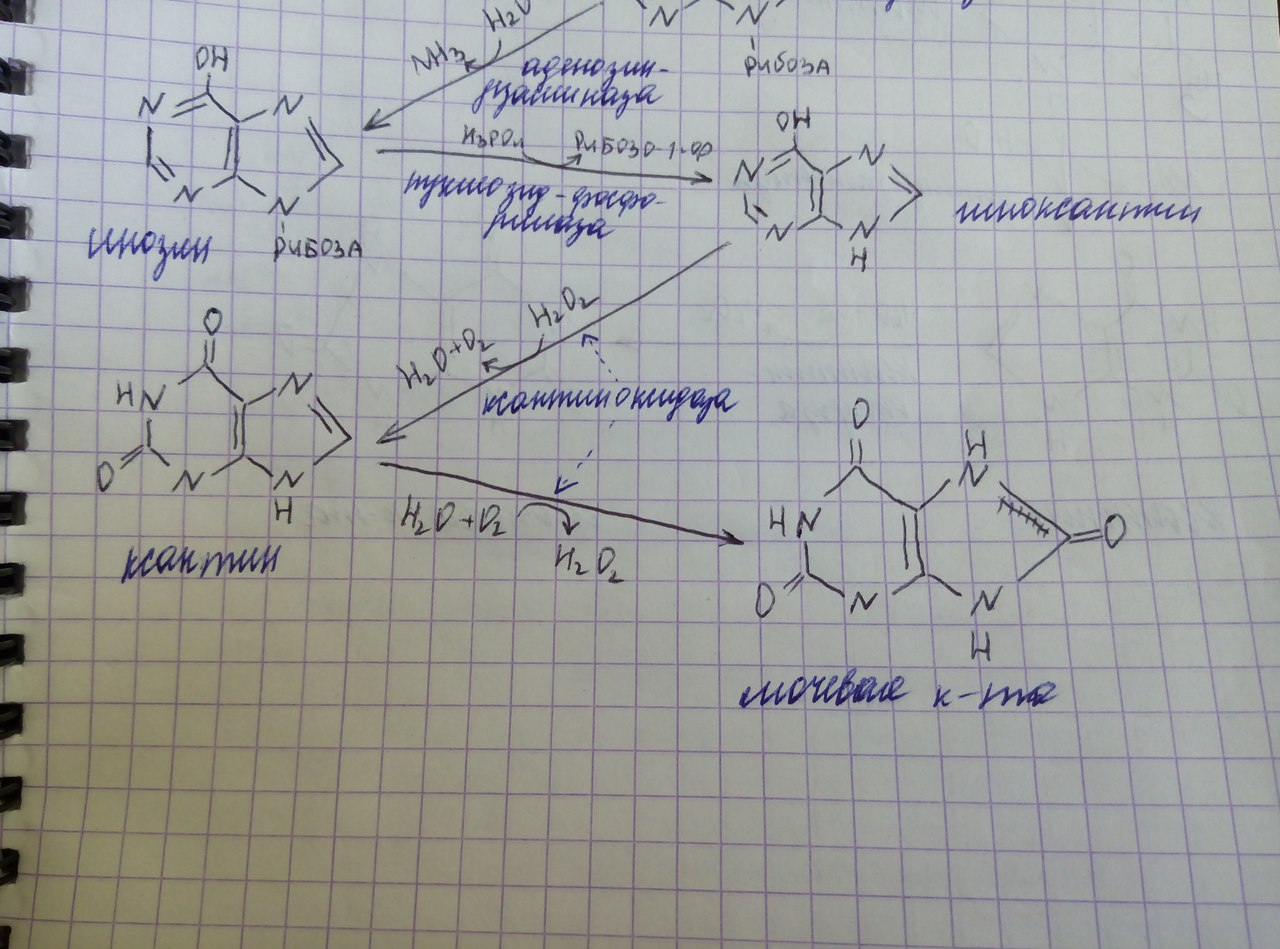
Когда в плазме крови концентрация мочевой кислоты превышает норму, то возникает гиперурикемия. Вследствие гиперурикемии может развиться подагра - заболевание, при котором кристаллы мочевой кислоты и уратов откладываются в суставных хрящах, синовиальной оболочке, подкожной клетчатке с образованием подагрических узлов, или тофусов. Накопление мочевой кислоты связано с повышенной скоростью распада пуриновых нуклеотидов. Гипоксантин окисляется до ксантика, ксантин – до мочевой кислоты при действии фермента ксантиноксидазы:
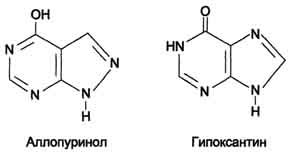
Лечение: аллопуринол – структурный аналог гипоксантина.
Аллопуринол оказывает двоякое действие на обмен пуриновых нуклеотидов:
8билет |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 429. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |