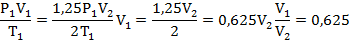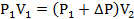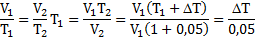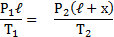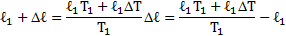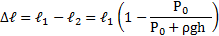Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Аналитические задачи на газовые законы ⇐ ПредыдущаяСтр 5 из 5 При решении аналитических задач на газовые законы надо: 1.Убедиться, что при изменении состояния масса газа остается постоянной. 2.Сделать схематический чертеж, на котором условно отметить состояния газа параметрами Р, V, Т. Записать закон Клапейрона для данных двух состояний. 3.Если какой-либо параметр при переходе газа из одного состояния в другое остается неизменным (могут меняться все три параметра), то уравнение Клапейрона перевести в закон Бойля — Мариотта, Гей-Люссака или Шарля. 4.В случае, когда газ заключен в цилиндрический сосуд и объем газа меняется только за счет изменения высоты его столба h, уравнение Клапейрона можно сразу записывать в виде: 5.Используя условия задачи, определить термодинамические параметры, выразив их через заданные величины. И если газ граничит с жидкостью, то особое внимание следует обратить на определение давления. Для его определения тех случаях, когда газ производит давление на жидкость, следует использовать закон Паскаля: провести нулевой уровень через границу, отделяющую газ от жидкости, и записать уравнение равновесия жидкости. 6.Полученную систему уравнений решить относительно неизвестной величины. P.S. § Если в задаче рассматривают состояния нескольких газов, отделенных друг от друга поршнями или входящих в состав смеси, то все указанные действия нужно проделать для каждого газа отдельно. § В задачах на газовые законы используется только абсолютная температура.
 Запишем уравнение Клапейрона и, так как процесс изотермический, переведем его в закон Бойля-Мариотта
Поэтому можно записать:
Отсюда находим первоначальное давление:
И объемы газов можно оставить в литрах, не переводить в систему СИ.
Для газа в отделе I: Для газа в отделе II: Отсюда следует:
Для газа в отделе I:
Газ граничит с жидкостью
Объем воды, поступившей в сосуд равен изменению объема газа при изотермическом процессе. Вода будет заходить в колбу до тех пор, пока давление внутри колбы не станет равным давлению наружному, то есть атмосферному. Запишем закон Бойля-Мариотта для газа в колбе:%
Отсюда определим изменение объема:
Масса поступившей воды равна:
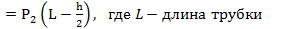

В обоих концах трубки воздух первоначально занимал объем V = S(L - h)/2, где S - площадь поперечного сечения трубки, и имел давление Р. Когда трубку поставили вертикально, объем воздуха в верхней части трубки стал V1 = S[(L - h)/2 + ℓ], а давление стало Р1; В нижней части трубки объем стал V2 = S[(L - h)/2 - ℓ], а давление стало равным Р2 Согласно закону Бойля-Мариотта для верхней части трубки PV = P1V2 Откуда (L - h) P =(L-h + 2ℓ)P1; Для нижней части трубки PV = P2V2, откуда (L-h)P = (L-h-2ℓ)Р2.
С другой стороны, столбик ртути находится в равновесии, когда давление воздуха в нижней части трубки равно сумме давлений воздуха в верхней части трубки и столбика ртути, т.е. P2=P1+ρgh Исключив Р1 иР2 из уравнений, найдем = 50 кПа.
|
||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 591. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |

 При увеличении абсолютной температуры газа в 2 раза давление увеличилось на 25%. во сколько раз изменился объем газа?
При увеличении абсолютной температуры газа в 2 раза давление увеличилось на 25%. во сколько раз изменился объем газа?
 С учетом данных, уравнение принимает вид:
С учетом данных, уравнение принимает вид: