
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Моделирование явлений тепло- и массопереносаДля технологических процессов более характерным являются гетерогенные химические реакции. В таких реакциях участвующие вещества находятся в разных фазах, собственно химическая реакция осуществляется на поверхности раздела фаз. Доставка реагентов к поверхности реагирования и отвод продуктов реакции в соответствующие фазы осуществляется в результате массопереноса.
Массоперенос Рассмотрим взаимодействие сульфида железа, одного из компонентов медного штейна, с дутьем и флюсом в условиях конвертирования медного штейна. В первом периоде конвертирования медного штейна эта реакция является основной: FeS(ж1) + О2(г) + SiO2(тв) → 2FeO(тв) + SiO2(ж2) + SO2(г).
У поверхности раздела фаз концентрация этого вещества иная, обозначим ее Сп – поверхностная концентрация. Перенос вещества из объема фазы к поверхности реагирования осуществляется в соответствии с законом Фика: где D – коэффициент диффузии; δ – толщина диффузионного слоя; (Ся-Сп) – движущая сила процесса, разность концентраций. При заданных условиях (например, температуре), известном характере химической реакции, известных размерах частиц диффундирующих веществ D=const, определяется характером диффундирующих частиц и среды. δ – зависит от гидродинамических особенностей процесса; β – константа скорости диффузии; rg – диффузионный поток – число молей вещества, доставляемых диффузией в зону реакции и отнесённое к единице поверхности.
Справедливо для реакции 1-го порядка:  k – кинетическая константа скорости (истинная).
kCп заменим на k'Cя; известная концентрация в объёме Ся.
Величина, обратная экспериментальной константе скорости, является суммой обратных величин истинной константы и константы диффузии. 1.
Поверхностная концентрация выравнивается с концентрацией в объёме фазы. Таким образом, диффузия доставляет вещество в зону реакции с высокой скоростью. 2. 3. В реальных задачах моделирования определение константы диффузии и кинетической константы скорости представляет собой сложную задачу. Кинетическая константа скорости определяется экспериментально, для расчёта констант диффузии используются критериальные уравнения.
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 468. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 Обозначим концентрацию вещества Ся – концентрация в ядре фазы вдали от межфазной границы;
Обозначим концентрацию вещества Ся – концентрация в ядре фазы вдали от межфазной границы; ,
,
 , k – константа, Сп – поверхностная концентрация.
, k – константа, Сп – поверхностная концентрация.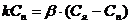




 – наблюдается быстрая диффузия при относительно медленной химической реакции. Скорость гетерогенной реакции определяется скоростью самой медленной стадии.
– наблюдается быстрая диффузия при относительно медленной химической реакции. Скорость гетерогенной реакции определяется скоростью самой медленной стадии.

 – химическая реакция быстрая при медленной диффузионной стадии. Лимитирующая стадия – диффузионная, при этом
– химическая реакция быстрая при медленной диффузионной стадии. Лимитирующая стадия – диффузионная, при этом 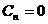 ,
, 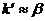 .
.