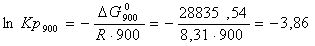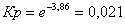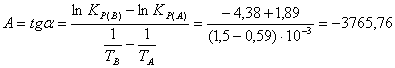Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Расчет константы равновесия ⇐ ПредыдущаяСтр 3 из 3 Для реакций, в которых участвуют только газы или газы и конденсированные фазы, представляющие собой чистые вещества, константу равновесия выражают обычно через равновесные парциальные давления (Pi) и обозначают символом Кр. Константа равновесия связана с изменением стандартной энергии Гиббса соотношением: После подстановки выражения (8) в уравнение (9) получим: Можно полагать, что в сравнительно небольшом интервале температур тепловой эффект реакции (∆Н0т) и изменение энтропии (∆S0т) практически постоянные величины (это подтверждают и результаты табл. 2 и 3). Отсюда уравнение можно записать в виде: где А и В – постоянные, которые соответственно равны: Уравнение (11) отвечает линейной зависимости lnKP = f(1/T). Определим коэффициенты А и В графически. С этой целью по уравнению (9) и данным табл. 4 рассчитаем величину lnKP, в заданном интервале температур. Например для температуры 900 К: Константа равновесия, соответствующая полученному значению lnKp900 вычисляется следующим образом: Аналогично рассчитываем lnKP и КР при других температурах. Полученные значения этих величин вместе со значениями сведем в табл. 5.  Таблица 5. Константы равновесия для реакции H2S+CO2=H2O+ COS при различных температурах (Т)
Реакции, для которых значения константы равновесия находятся в пределах от 10-3 до 103 (10-3 < KP < 103), принято считать практически обратимыми. Для реакции (1) в интервале 800 –1700 К 10-3 < KP < 103 то есть это практически обратимая реакция. Увеличение Кр с ростом температуры означает, что равновесие реакции (1) сдвигается слева направо. По данным табл. 5 строим график зависимости lnKP =f(1/Т), приведенной на рис. 4. Точки на графике практически ложатся на прямую, тангенс угла которой к оси абсцисс численно равен коэффициенту А в уравнении (11). Для нахождения величины тангенса возьмем на прямой, как это показано на рис. 4, произвольно две точки «А» и «В» и определим численные значения их ординат и абсцисс. Можно записать: Для определения численного значения В поступим следующим образом. Из табл. 5 возьмем значение lnKP = при 1700 К (-1,89), подставим его вместе с численным коэффициентом А (-3765,76) найденным ранее в уравнение (11), предварительно выразив его через В. В = lnKp – A/T = -1,89 – (-3765,76 / 1700) = 0,33 Итак, приближенное уравнение зависимости константы равновесия от температуры имеет вид: lnKp = (-3765,76 / Т) + 0,33 (14) Последнее уравнение позволяет рассчитать значение Кр при любой температуре, если последняя находится в заданном интервале (то есть в пределах 800 – 1700 К) или незначительно выходит за этот интервал. По значениям коэффициентов А и В рассчитаем величину среднего теплового эффекта реакции (∆Н0т) и изменения энтропии (∆S0т). Согласно уравнениям (12) – (13) имеем: ∆Н0т = -А∙R = -(-3765,76) ∙ 8,31 = 31293,45 Дж ∆S0т = В ∙ R = 0,33 ∙ 8,31 = 2,74 Дж/К Полученные данные неплохо согласуются с данными, приведенными в табл. 2 и 3. Если подсчитать средние значения величин, приведенных в табл. 2 и 3, то они будут приблизительно равны полученным выше результатам.
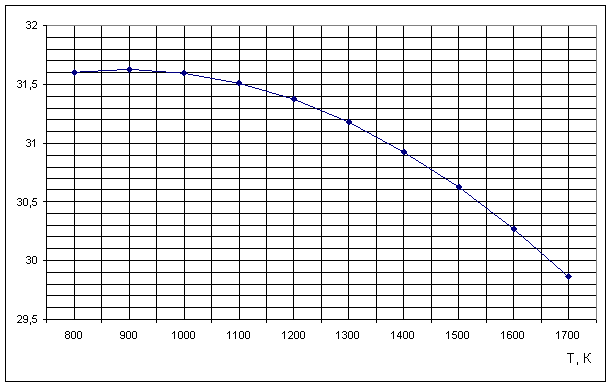
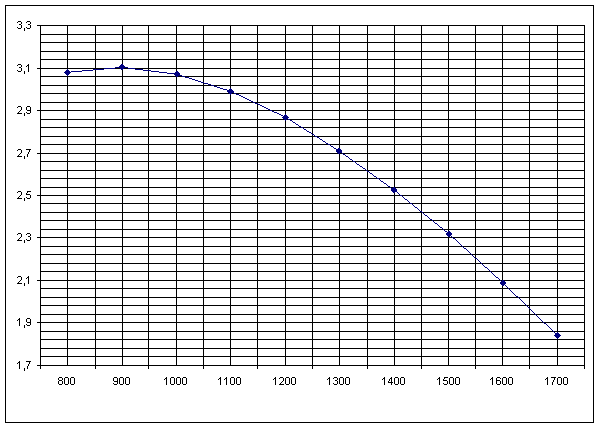
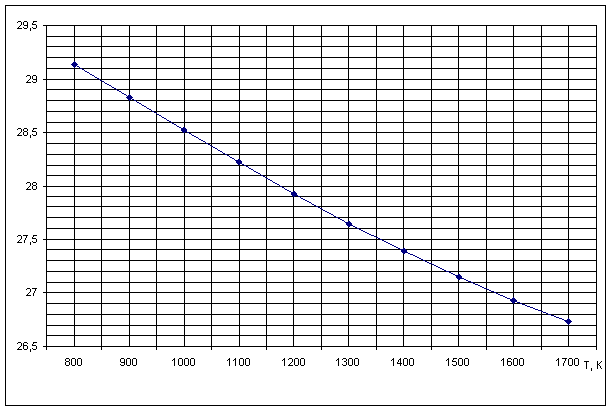
Рисунок 1. Зависимость теплового эффекта реакции H2S+CO2=H2O+ COS от температуры Рисунок 2. Зависимость изменения энтропии от температуры реакции H2 S+CO2=H2O+ COS Рисунок 3. Зависимость изменений стандартной энергии Гиббса от температуры реакции H2S+CO2=H2O+ COS Рисунок 4. Зависимость lnKp от обратной температуры для реакции H2S+CO2=H2O+ COS |
||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 376. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
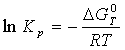 (9)
(9)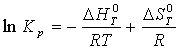 (10)
(10)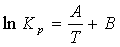 (11)
(11)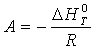 (12)
(12)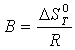 (13)
(13)