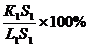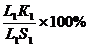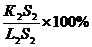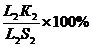Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
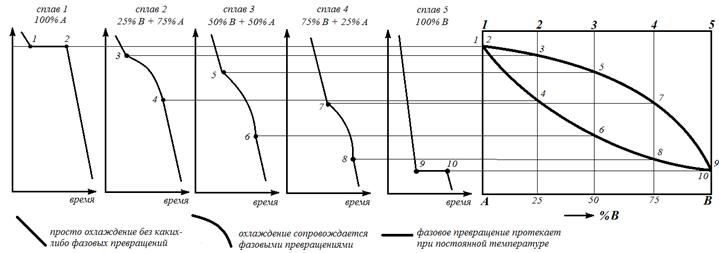
Диаграммы и способы их построенияКурс металловедения тесно связан с изучением диаграмм состояния. Диаграмма состояния сплава представляет собой графическое изображение состояния сплава и показывает превращения, протекающие в сплавах в зависимости от температуры и концентрации элементов (в условиях минимальной свободной энергии). Без знания диаграмм состояния нельзя научно обоснованно выбирать сплавы с заданными свойствами и выбирать режимы литья, термической обработки и обработки давлением. Диаграммы состояния строятся для определения количества фаз в сплаве и их состава. Диаграммы состояния, как правило, строят экспериментально (на основании кривых охлаждения). Для их построения обычно используется термический метод, с помощью которого получают кривые затвердевания и охлаждения сплавов. Готовят ряд сплавов с различным содержанием компонентов А и В, расплавляют и начинают медленно охлаждать, фиксируя их температуру через равные промежутки времени. По этим данным строят кривые охлаждения для всех сплавов.
По остановкам и перегибам на этих кривых, обусловленных тепловыми эффектами превращений, определяют температуры превращений. Фиксируют эти температуры и переносят на поле диаграммы состояния. Затем точки с одинаковым физико-химическим смыслом (начало кристаллизации, конец кристаллизации, образование химического соединения, и т.д.) соединяют между собой. Кривая, замыкающая критические точки начала кристаллизации a-твердого раствора (линия 1-3-5-7-9) называется линией ликвидус («ликва» – жидкость, лат.). Семейство критических точек, соответствующих температуре окончания кристаллизационных процессов (линия 2-4-6-8-10), образует линию солидус (solid, «солид» – твердый, лат.).  Выше линии 1-3-5-7-9 сплавы находятся в жидком состоянии. Ниже линии 2-4-6-8-10 сплавы находятся в твердом состоянии. Точки перегиба (3–8) или остановки (1, 2, 9, 10) на кривых охлаждения называют критическими точками. Они соответствуют температурам, при которых в сплавах начинаются, заканчиваются или полностью протекают какие-либо превращения.
Правило отрезков
А В
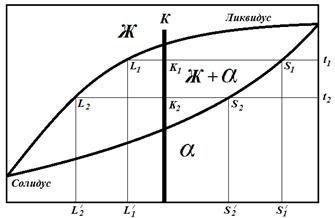
С помощью правила отрезков на диаграмме определяют: 1.Состав фаз сплава заданного состава при определенной температуре. Пусть имеем сплав К определенной концентрации. Проводим горизонтальную линию, соответствующую данной температуре t1, до пересечения с линиями ликвидус (l1) и солидус(s1). Проекции точек пересечения на ось концентраций (l/1 и s/1) показывают состав фаз. При охлаждении состав жидкой фазы в соответствии с правилом отрезков меняется по линии ликвидус, а состав твердой фазы – по линии солидус. 2. Относительное количество каждой фазы при определенной температуре. Отрезки горизонтальной линии между точкой К и точками, определяющими составы фаз, обратно пропорциональны количествам этих фаз:
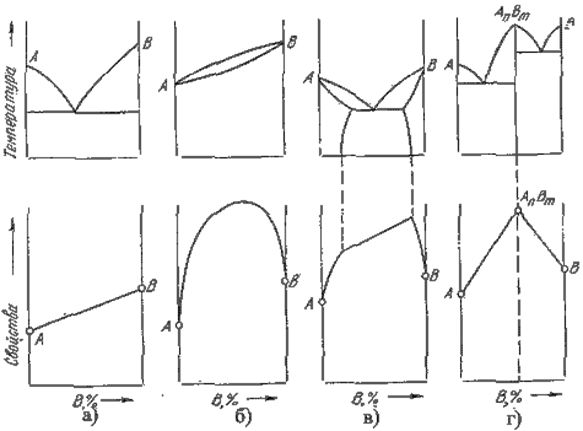
Существует большое количество диаграмм различных типов. Свойства сплавов зависят от их положения на диаграмме:
|
|||||||||||
|
Последнее изменение этой страницы: 2018-04-11; просмотров: 345. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |