Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Разрушение структуры липидовКонечные продукты перекисного окисления полиеновых кислот - малоновый диальдегид и гидропероксид кислоты. 4) Обрыв цепи - взаимодействие радикаловмежду собой: Развитие цепи может останавливаться при взаимодействии свободных радикалов между собой или при взаимодействии с различными антиоксидантами, например, витамином Е, который отдаёт электроны, превращаясь при этом в стабильную окисленную форму. Повреждение клеток в результате перекрестное окислении липидов. Активные формы кислорода повреждают структуру ДНК, белков и различные мембранные структуры клеток. В результате в клетки могут проникать вода, ионы натрия, кальция, что приводит к набуханию клеток, органелл и их разрушению. При дистрофии мышц (болезнь Дюшенна), болезни Паркинсона, , при атеросклерозе, развитии опухолей.: с возрастом увеличивается количество. Этот пигмент называют липофусцин,. ПОЛ происходит не только в живых организмах, но и в продуктах питания, особенно при неправильном приготовлении и хранении пищи. Билет №4 1- Фонд свободных аминокислот организма составляет примерно 35 г. Содержание свободных аминокислот в крови в среднем равно 35-65 мг/дл. Большая часть аминокислот входит в состав белков, Источники свободных аминокислот в клетках - белки пищи, собственные белки тканей и синтез аминокислот из углеводов. Многие клетки, за исключением высокоспециализированных (например, эритроцитов), используют аминокислоты для синтеза белков, а также большого количества других веществ: фосфолипидов мембран, гема, пуриновых и пиримидиновых нуклеотидов, биогенных аминов (катехоламинов, гистамина) и других соединений (  Какой-либо специальной формы депонирования аминокислот, не существует. Поэтому резервом аминокислот могут служить все функциональные и структурные белки тканей, но преимущественно белки мышц, поскольку их больше, чем всех остальных. сутки распадается на аминокислоты около 400 г белков, примерно такое же количество синтезируется. Поэтому тканевые белки не могут восполнять затраты аминокислот при их катаболизме и использовании на синтез других веществ. Первичными источниками аминокислот не могут служить и углеводы, так как из них синтезируются только углеродная часть молекулы большинства аминокислот, а аминогруппа поступает от других аминокислот. Следовательно, основным источником аминокислот организма служат белки пищи
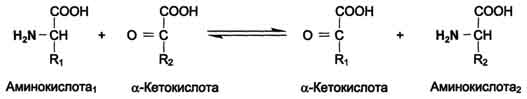
Катаболизм большинства аминокислот начинается с Отщепления α-аминогруппы.Аминокислота теряет аминогруппу в результате двух типов реакций: трансаминирования и дезаминирования. Трансаминирование - реакция переноса α-аминогруппы с аминокислоты на α-кетокислоту, в результате чего образуются новая кетокислота и новая аминокислота.
Дезаминирование аминокислот -реакция отщепления α-аминогруппы от аминокислоты, в результате чего образуется соответствующая α-кетокислота (безазотистый остаток) и выделяется молекула аммиака
2-Распад гема Гем(гемоксигеназа)-биливердин(биливердинредуктаза)-билирубин(УДФ-глюкуранилтрансфераза)-билирубинмоноглюкуронид(УД-глюкуронилтрансфераза)-билирубиндиглюкуронид В нормальном состоянии концентрация общего билирубина в плазме составляет 0,3-1 мг/дл (1,7-17 мкмоль/л), 75% от общего количества билирубина находится в неконъюгированной форме (непрямой билирубин). В клинике конъ-югированный билирубин называют прямым, потому что он водорастворим и может быстро взаимодействовать с диазореагентом, образуя соединение розового цвета, - это прямая реакция Ван дер Берга. Неконъюгированный билирубин гидрофобен, поэтому в плазме крови содержится в комплексе с альбумином и не реагирует с диазореактивом до тех пор, пока не добавлен органический растворитель, например этанол, который осаждает альбумин. Неконъюгированный илирубин, взаимодействующий с азокрасителем только после осаждения белка, называют непрямым билирубином. Когда содержание билирубина превышает норму, говорят о гипербилирубинемии. В зависимости от того, концентрация какого типа билирубина повышена в плазме - неконъюгированного или конъюгированного, - гипербилирубинемию классифицируют как неконъюгированную и конъюгированную. У больных с печёночно-клеточной патологией, сопровождающейся длительным повышением концентрации конъюгированного билирубина, в крови обнаруживают третью форму плазменного билирубина, при котором билирубин ковалентно связан с альбумином, и поэтому его невозможно отделить обычным способом. В некоторых случаях до 90% общего содержания билирубина крови может находиться в этой форме. 3-Обезвреживание этилового спирта в печени. NAD-зависимая алкогольдегидрогеназа, Р450-зависимая микросомальная этанолокисляющая система, каталаза. Метаболизм и токсичность ацетальдегида. Катаболизм этилового спирта осуществляется в печени. Превращение этанола в печени осуществляется тремя путями с образованием ацетальдегида А. ОКИСЛЕНИЕ ЭТАНОЛА NAD-ЗАВИСИМОЙ АЛКОГОЛЬДЕГИДРОГЕНАЗОЙ Основную роль в играет цинксодержащий NAD+-зависимый фермент - алкогольдегидрогеназа, локализующаяся в основном в цитозоле и митохондриях печени (95%). В ходе реакции пpoиcxoдит дегидрирование этанола, образуются ацетальдегид и восстановленный кофермент NADH. Алкогольдегидрогеназа катализирует обратимую реакцию, направление которой зависит от концентрации ацетальдегида и соотношения NADH/NAD+ в клетке. С9H5ОН + NAD+ ↔ CH3CHO + NADH + H+. При хроническом алкоголизме количество фермента в печени не увеличивается, т.е. он не является индуцируемым ферментом. Б. ОКИСЛЕНИЕ ЭТАНОЛА ПРИ УЧАСТИИ ЦИТОХРОМ Р450-ЗАВИСИМОЙ МИКРОСОМАЛЬНОЙ ЭТАНОЛОКИСЛЯЮЩЕЙ СИСТЕМЫ Цитохром Р450-зависимая микросомальная этанолокисляющая система локализована в мембране гладкого ЭР гепатоцитов. При хроническом алкоголизме окисление этанола ускоряется на 50-70% за счёт гипертрофии ЭР и индукции цитохрома Р450 II Е1. C9H5OH + NADPH + Н+ + О2 → CH3CHO + NADP+ + 2 Н2О. Кроме основной реакции, цитохром Р450 катализирует образование активных форм кислорода (О2-, Н2О2), которые стимулируют ПОЛ в печени и других органах в. окисление этанола каталазой Второстепенную роль в окислении этанола играет каталаза, находящаяся в пероксисомах цитоплазмы и митохондрий клеток печени. Этот фермент расщепляет примерно 2% этанола, но при этом утилизирует пероксид водорода. СН3СН2ОН + Н2О2 → СН3СНО +2 Н2О. г. метаболизм и токсичность ацетальдегида Ацетальдегид, образовавшийся из этанола, окисляется до уксусной кислоты FAD-зависимой альдегидоксидазой и NАD+-зависимой АлДГ. CH3CHO + О2 + Н2О → CH3COOH +Н2О2. Повышение концентрации ацетальдегида в клетке вызывает индукцию фермента альдегид-оксидазы. В ходе реакции образуются уксусная кислота, пероксид водорода и другие активные формы кислорода, что приводит к активации ПОЛ. АлДГ окисляет субстрат при участии кофермента NАD+. CH3CHO + Н2О + NAD+ → CH3COOH + + NADH + H+. Полученная в ходе реакции уксусная кислота активируется под действием фермента ацетил-КоА-синтетазы. При поступлении больших доз алкоголя в цитозоле резко повышается концентрация Ацетальдегида . Ацетилирование белков приводит к снижению синтеза экспортируемых печенью в кровь белков, например альбумина, который, поддерживает осмотическое давление, а также участвует в транспорте многих гидрофобных веществ в крови. При хроническом алкоголизме снижение синтеза фосфолипидов и белков в печени, в том числе и апобелков, участвующих в формировании ЛПОHП, вызывает внутриклеточное накопление ТАГ и ожирение печени. Повышение в крови концентрации лактата, ацетоуксусной кислоты и β-гидроксибутирата служит причиной метаболического ацидоза при алкогольной интоксикации. При повышении концентрации ацетальдегида и NADH в клетках печени образуется этанол. Этанол - растворяется в липидном бислое мембран и нарушает их функции. Это негативно отражается на трансмембранном переносе веществ, межклеточных контактах, взаимодействиях рецепторов клетки с сигнальными молекулами. Этанол может проходить через мембраны в межклеточное пространство и кровь и далее в любую клетку организма. Билет №5 1- Катаболизм аминок-т сводится к образованиюпируват, ацетил-КоА,α-кетоглутарат, сукцинил-КоА, фумарат, оксалоацетат гликогенных аминокислоты - превращаются в пируват и промежуточные продукты ЦТК и образуют в конечном итоге оксалоацетат, могут использоваться впроцессе глюконеогенеза. кетогенныеаминок-ты в процессе катаболизма превращаются в ацетоацетат (Лиз, Лей) или ацетил-КоА (Лей) и могут использоваться в синтезе кетоновых тел. гликокетогенными аминокислоты используется и для синтеза глюкозы, и для синтеза кетоновых тел, так как в процессе их катаболизма образуются 2 продукта - определённый метаболит цитратного цикла и ацетоацетат (Три, Фен, Тир) или ацетил-КоА (Иле). Анаплеротические реакции - безазотистые остатки аминокислот используются для восполнения того количества метаболитов общего пути катаболизма, которое затрачивается на синтез биологически активных веществ. 1. Фермент пируваткарбоксилаза (кофермент - биотин), катализирующий эту реакцию, обнаружен в печени и мышцах. 2. Аминокислоты → Глутамат → α-Кетоглутарат под действием глутаматдегидрогеназы или аминотрансфераз. 3. Пропионил-КоА, а затем и сукцинил-КоА могут образоваться также при распаде высших жирных кислот с нечётным числом атомов углерода 4. Аминокислоты → Фумарат 5. Аминокислоты → Оксалоацетат Реакции 2, 3 происходят во всех тканях (кроме печени и мышц), где отсутствует пируваткарбоксилаза.
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 421. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |