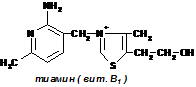Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
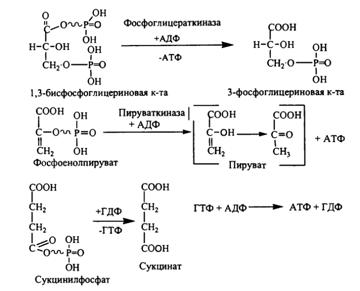
Транспорт кислорода в кровиОсновная часть кислорода связана с гемоглобином (оксигемоглобин, HbO2) и истинное содержание кислорода в крови зависит от двух дополнительных параметров – концентрации Hb и сатурации (насыщении) гемоглобина кислородом (HbOsat или SO2). Оксигемоглобин (HbО2) – процентное содержание в крови, является отношением фракции оксигемоглобина (HbО2) к сумме всех фракций (общему гемоглобину). Насыщение (сатурация) гемоглобина кислородом (HbOSAT, SО2), представляет собой отношение фракции оксигенированного гемоглобина к тому количеству гемоглобина в крови, который способен транспортировать О2. 4. Субстратное фосфорилирование Субстратное фосфорилирование[лат. substratum — подстилка, подкладка; греч. phos — свет и phoros — несущий] — синтез богатых энергией фосфорных соединений (в основном АТФ, см. Аденозинтрифосфат, АТФ) за счет энергии окислительно-восстановительных реакций гликолиза (катализируемых фосфоглицеральдегиддегидрогеназой и энолазой) и при окислении ?-кетоглутаровой кислоты в цикле трикарбоновых кислот (под действием a-кетоглутаратдегидрогеназы и сукцинаттиокиназы). При С.ф. происходит перенос фосфорильной группы, образующейся из ортофосфорной кислоты, на аденозиндифосфат (АДФ) с образованием АТФ
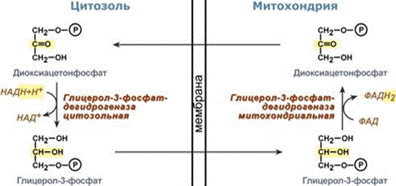
№14. Челночные механизмы транспорта через мембрану митохондрий. Так как сама молекула НАДН через мембрану не проходит, то существуют специальные системы, принимающие атомы водорода от НАДН в цитоплазме и отдающие их в матриксе митохондрий. Эти системы получили название челночные системы. Определены две основные челночные системы – глицеролфосфатная и малат-аспартатная 
Коферменты . Их роль. связь с витаминами Коферменты в каталитических реакциях осуществляют транспорт различных групп атомов, электронов или протонов. Коферменты связываются с ферментами: ковалентными связями; ионными связями; гидрофобными взаимодействиями и т.д. Один кофермент может быть коферментом для нескольких ферментов. Многие коферменты являются полифункциональными (например, НАД, ПФ). В зависимости от апофермента зависит специфичность холофермента. Все коферменты делят на две большие группы: витаминные и невитаминные.
Коферменты витаминной природы – производные витаминов или химические модификации витаминов. Сюда относят:флавинмононуклеотид (ФМН); флавинадениндинуклеотид (ФАД).Ребитол и изоалоксазин образуют витамин В2. Витамин В2 и остаток фосфорной к-ты образуют ФМН ФМН в соединении с АМФ образуют ФАД.
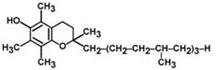
Витамин Е Жирорастваримый антистерильный витамин, антиоксидантный энзим. В химическом плане это альфа-, бета-, гамма- и дельта-токоферолы, но преобладающим является альфа-токоферол. Витамин Е устойчив к нагреванию. Роль витамина Е в обмене веществ 1. регулирует интенсивность свободно-радикальных реакций. Препятствует перекисному окислению липидов биомембран; 2. повышает активность витамина А. Суточная потребность витамина Е 20-25 мг. Источники витамина Е: растительные масла (!), а также печень, желток яиц, проросшие зерна; масло облепихи.
Гемоглобин Гемоглобин входит в состав группы белков гемопротеины, которые сами являются подвидом хромопротеинов и подразделяются на неферментативные белки (гемоглобин, миоглобин) и ферменты (цитохромы, каталаза, пероксидаза). Небелковой частью их является гем – структура, включающая в себя порфириновое кольцо (состоящее из 4 пиррольных колец) и иона Fe2+. Железо связывается с порфириновым кольцом двумя координационными и двумя ковалентными связями.
№15 АДФ,АТФ
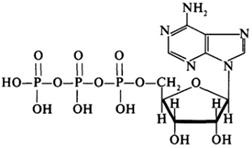
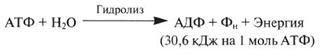
АТФ (Аденозинтрифосфа́т) Значение АТФ При расщеплении АТФ на АДФ и неорганический фосфат (Фн) высвобождается энергия:
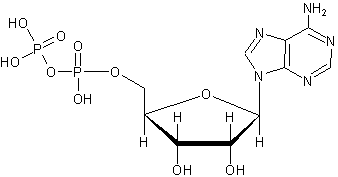
Помимо энергетической АТФ выполняет в организме ещё ряд других не менее важных функций: -Вместе с другими нуклеозидтрифосфатами АТФ является исходным продуктом при синтезе нуклеиновых кислот. -Кроме того, АТФ отводится важное место в регуляции множества биохимических процессов. Являясь аллостерическим эффектором ряда ферментов, АТФ, присоединяясь к их регуляторным центрам, усиливает или подавляет их активность. -АТФ является также непосредственным предшественником синтеза циклического аденозинмонофосфата — вторичного посредника передачи в клетку гормонального сигнала. -Также известна роль АТФ в качестве медиатора в синапсах и сигнального вещества в других межклеточных взаимодействиях (пуринергическая передача сигнала Аденозиндифосфат (АДФ) — нуклеотид, состоящий из аденина, рибозы и двух остатков фосфорной кислоты. АДФ образуется в результате переноса концевой фосфатной группы АТФ. АДФ участвует в энергетическом обмене во всех живых организмах.
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 404. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |