
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Яка із запропонованих формул описує закон радіоактивного розпаду?
99. Бета-випромінювання – це: 1. потік електронів і позитронів; 2. потік ядер; 3. потік атомів; 4. потік альфа-частинок. 100. Ядра з однаковим зарядовим числом, але різним масовим числом називають: 1. ізотопами; 2. ферміонами; 3. схожими; 4. чарівними.
ХІМІЯ 1. Калій – це: 1. F - елемент. 3. P - елемент. 2. S - елемент. 4. D - елемент. 2. K2O відноситься до оксидів: 1. Основних. 3. Амфотерних. 2. Кислотних. 4. Несолетвірних. 3. Сполука КОН дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Основа. 4. Сіль. Еквівалент К дорівнює: 1. Ar(K)/2. 3. Ar(k)/4. 2. Ar(K)/1. 4. Ar(k)/3. 5. Розчин має рН = 3, це середовище: 1. Кисле. 3. Лужне. 2. Нейтральне. 4. Слабколужне. 6. Змішали 5 г солі і 95 г води – це розчин: 1. 95 %-ний. 3. 100 %-ний. 2. 5 %-ний. 4. 0,5 %-ний. 7. Розчин солі NaNO3 має середовище: 1. Кисле 3. Лужне. 2. Нейтральне. 4. Слабкокисле. 8. Ступінь окиснення хрому у сполуці K2Cr2O7: 1.+2. 3. +6. 2. +7. 4. - 2.  9. Na2O відноситься до оксидів: 1. Основних. 3. Амфотерних. 2. Кислотних. 4. Несолетвірних. 10. Сполука NaОН дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Основа. 4. Сіль. 11. Еквівалент Na дорівнює: 1. Ar(Na)/2. 3. Ar(na)/4. 2. Аr(Na)/1. 4. Ar(na)/5. 12. Розчин має рН = 2, це середовище: 1. Кисле. 3. Лужне. 2. Нейтральне. 4. Сильнокисле. 13. Змішали 3 г солі і 97 г води – це розчин: 1. 97 %-ний. 3. 100 %-ний. 2. 3 %-ний. 4. 0,3 %-ний. 14. Розчин солі KnO3 має середовище: 1. Кисле. 3. Лужне. 2. Нейтральне. 4. Слабколужне. 15. Ступінь окиснення хрому у сполуці Na2Cr2O7: 1. +2. 3. +6. 2. +7. 4. – 6. 16. К2o відноситься до оксидів: 1. Несолетвірних. 3. Амфотерних. 2. Кислотних. 4. Солетвірних. 17. Сполука КОН дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Сіль. 4. Основа. 18. Еквівалент Са дорівнює: 1. Ar(Са)/2. 3. Ar(Са)/3. 2. Ar(Са)/1. 4. Ar(Са)/4. 19. Розчин має рН = 11, це середовище: 1. Кисле. 3. Слабколужне. 2. Нейтральне. 4. Сильнодужне. 20. Змішали 31 г солі і 69 г води – це розчин: 1. 69 %-ний. 3. 31 %-ний. 2.100 %-ний. 4. 3,1 %-ний. 21. Розчин солі LiCl має середовище: 1. Кисле. 3. Нейтральне. 2. Лужне. 4. Слабколужне. 22. Ступінь окиснення сульфуру у сполуці Na2S2O3: 1. +2. 3. +6. 2. +7. 4. -2. 23. Li2o відноситься до оксидів: 1. Амфотерних. 3. Основних. 2. Кислотних. 4. Несолетвірних. 24. Гідроксид LiОН дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Сіль. 4. Основа. 25. Еквівалент Li дорівнює: 1. Ar(Li)/2. 3. Ar(Li)/3. 2. Ar(Li)/4. 4. Ar(Li)/1. 26. Розчин має рН = 2, це середовище: 1. Слабкокисле. 3. Лужне. 2. Нейтральне. 4. Сильнокисле. 27. Змішали 7 г солі і 93 г води – це розчин: 1. 93 %-ний. 3. 100 %-ний. 2. 7 %-ний. 4. 0,7 %-ний. 28. Розчин солі LiNO3 має середовище: 1. Сильнокисле. 3. Лужне. 2. Нейтральне. 4. Слабколужне. 29.змішали 17 г солі і 83 г води – це розчин: 1. 83 %-ний. 3. 100 %-ний. 2. 17 %-ний. 4. 1,7 %-ний. 30. Ступінь окиснення хрому у сполуці Na2CrO4: 1. +2. 3. +6. 2. +7. 4. – 2. 31. Ag2О відноситься до оксидів: 1. Основних. 3. Амфотерних. 2. Кислотних. 4. Несолетвірних. 32. Сполука AgОН дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Основа. 4. Сіль. 33. Еквівалент Ag дорівнює: 1.Аr(Аg)/2. 3. Ar(Na)/4. 2.Аr(Аg)/1. 4. Ar(Na)/3. 34. Au2O3 відноситься до оксидів: 1. Основних. 3. Амфотерних. 2. Кислотних. 4. Несолетворних. 35. Сполука Аu(ОН)3 дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Сіль. 4. Основа. 36. Еквівалент Аu дорівнює: 1. Ar(Аu)/2. 3. Ar(Аu)/3. 2. Ar(Аu)/1. 4. Ar(Аu)/4. 37. Розчин має рН = 4,5 це середовище: 1. Сильнокисле. 3. Лужне. 2. Нейтральне. 4. Слабкокисле. 38. Змішали 14 г солі і 86 г води – це розчин: 1. 86 %-ний. 3. 100 %-ний. 2. 14 %-ний. 4. 1,4 %-ний. 39. Розчин солі Аu(NO3)3 має середовище: 1. Слабкокисле. 3. Лужне. 2. Нейтральне. 4. Сильнокисле. 40. Ступінь окиснення аргентуму у сполуці Ag4Р2O7: 1. +2. 3. +5. 2. +7. 4. +1. 41. Розчин має рН = 4, це середовище: 1. Слабкокисле. 3. Лужне. 2. Нейтральне. 4. Сильнокисле. 42. Змішали 4 г солі і 96 г води – це розчин: 1. 96 %-ний. 3. 100 %-ний. 2. 4 %-ний. 4. 0,4 %-ний. 43. Розчин солі AgNO3 має середовище: 1. Сильнокисле. 3. Лужне. 2. Нейтральне. 4. Слабкокисле. 44. Ступінь окиснення фосфору у сполуці Ag4Р2O7: 1. +2. 3. +5. 2. +7. 4. +1. 45. PbO2 відноситься до оксидів: 1. Основних. 3. Амфотерних. 2. Кислотних. 4. Несолетвірних. 46. Сполука Pb(ОН)2 дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Основа. 4. Сіль. 47. Еквівалент Pb дорівнює: 1. Ar(Pb)/2. 3. Ar(Pb)/3. 2. Ar(Pb)/1. 4. Ar(Pb)/4. 48. Розчин має рН = 5,5 це середовище: 1. Сильнокисле. 3. Лужне. 2. Нейтральне. 4. Слабкокисле. 49. Змішали 12 г солі і 88 г води – це розчин: 1. 8 %-ний. 3. 100 %-ний. 2. 88 %-ний. 4. 12 %-ний. 50. Розчин солі Pb(NO3)2 має середовище: 1. Слабкокисле. 3. Лужне. 2. Нейтральне. 4. Сильнокисле. 51. Ступінь окиснення плюмбуму у сполуці Pb2Р2O7: 1. +2. 3. +5. 2. +7. 4. +4. 52. SO2 відноситься до оксидів: 1. Основних. 3. Амфотерних. 2. Несолетвірних. 4. Солетвірних. 53. Сполука Pb(ОН)4 дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Основа. 4. Сіль. 54. Еквівалент S дорівнює: 1. Ar(S)/2. 3. Ar(S)/6. 2. Ar(S)/1. 4. Ar(S)/4. 55. Розчин має рН = 6,5 це середовище: 1. Сильнокисле. 3. Лужне. 2. Нейтральне. 4. Слабкокисле. 56. Змішали 42 г солі і 58 г води – це розчин: 1. 58 %-ний. 3. 100 %-ний. 2. 42 %-ний. 4. 4,2 %-ний. 57. Розчин солі Na2SO3 має середовище: 1. Слабкокисле. 3. Лужне. 2. Нейтральне. 4. Сильнокисле. 58. Ступінь окиснення сульфуру у сполуці Na2S2O7: 1. +2. 3. +6. 2. +7. 4. – 2. 59. N2O5 відноситься до оксидів: 1. Основних. 3. Амфотерних. 2. Кислотних. 4. Несолетворних. 60. Сполука Ca(ОН)2 дисоціює як: 1. Кислота. 3. Основа. 2. Амфотерна сполука. 4. Сіль. 61. Еквівалент N дорівнює: 1. Ar(N)/2. 3. Ar(N)/5. 2. Ar(N)/1. 4. Ar(N)/3. 62. Розчин має рН = 8,5 це середовище: 1. Слабкокисле. 3. Слабколужне. 2. Нейтральне. 4. Сильнолужне. 63. Змішали 32 г солі і 68 г води – це розчин: 1. 68 %-ний. 3. 100 %-ний. 2. 32 %-ний. 4. 3,2 %-ний. 64. Розчин солі Na2SO4 має середовище: 1. Сильнокисле. 3. Слабколужне. 2. Нейтральне. 4. Сильнолужне. 65. Ступінь окиснення сульфуру у сполуці K2S2O7: 1. +2. 3. +6. 2. +7. 4. -2. 66. F2O відноситься до оксидів: 1. Основних. 3. Амфотерних. 2. Кислотних. 4. Несолетвірних. 67. Сполука Zn(ОН)2 дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Основа. 4. Сіль. 68. Еквівалент P дорівнює: 1. Ar(P)/2. 3. Ar(P)/5. 2. Ar(P)/1. 4. Ar(P)/3. 69. Розчин має рН = 9,5 це середовище: 1. Сильнокисле. 3. Сильнолужне. 2. Нейтральне. 4. Слабколужне. 70. Змішали 6 г солі і 94 г води – це розчин: 1. 6 %-ний. 3. 100 %-ний. 2. 94 %-ний. 4. 0,6 %-ний. 71. Розчин солі ZnSO4 має середовище: 1. Сильнокисле. 3. Лужне. 2. Нейтральне. 4. Слабкокисле. 72. Ступінь окиснення сульфуру у сполуці (NH4)2S2O7: 1. +2. 3. +6. 2. +7. 4. -2. 73. Rb2O відноситься до оксидів: 1. Основних. 3. Амфотерних. 2. Кислотних. 4. Несолетвірних. 74. Сполука RbОН дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Основа. 4. Сіль. 75. Еквівалент Rb дорівнює: 1. Ar(Rb)/2. 3. Ar(Rb)/4. 2. Ar(Rb)/1. 4. Ar(Rb)/3. 76. Розчин має рН = 3,5 це середовище: 1. Сильнокисле. 3. Лужне. 2. Нейтральне. 4. Слабкокисле. 77. Змішали 7,5 г солі і 92,5 г води – це розчин: 1. 92,5 %-ний. 3. 100 %-ний. 2. 7,5 %-ний. 4. 75 %-ний. 78. Розчин солі RbNO3 має середовище: 1. Сильнокисле. 3. Лужне. 2. Нейтральне. 4. Слабкокисле. 79. Ступінь окиснення хрому у сполуці Rb2Cr2O7: 1. +2. 3. +6. 2. +7. 4. +3. 80. Cs2O відноситься до оксидів: 1. Основних. 3. Амфотерних. 2. Кислотних. 4. Несолетвірних. 81. Сполука CsОН дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Основа. 4. Сіль. 82. Еквівалент Cs дорівнює: 1. Ar(Cs)/2. 3. Ar(Cs)/3. 2. Ar(Cs)/1. 4. Ar(Cs)/4. 83. Розчин має рН = 1,2 - це середовище: 1. Слабкокисле. 3. Лужне. 2. Нейтральне. 4. Сильнокисле. 84. Змішали 2,3 г солі і 97,7 г води – це розчин: 1. 97,7 %-ний. 3. 100 %-ний. 2. 2,3 %-ний. 4. 23 %-ний. 85. Розчин солі CsNO3 має середовище: 1. Кисле. 3. Лужне. 2. Нейтральне. 4. Слабколужне. 86. Ступінь окиснення хрому у сполуці Cs2Cr2O7: 1. +2. 3. +6. 2. +7. 4. +3. 87. BaO відноситься до оксидів: 1. Основних. 3. Амфотерних. 2. Кислотних. 4. Несолетвірних. 88. Сполука Ba(ОН)2 дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Основа. 4. Сіль. 89. Еквівалент Ва дорівнює: 1. Ar(Ba)/2. 3. Ar(Ba)/3. 2. Ar(Ba)/1. 4. Ar(Ba)/4. 90. Розчин має рН = 1,1, це середовище: 1. Слабкокисле. 3. Лужне. 2. Нейтральне. 4. Сильнокисле. 91. Змішали 11 г солі і 89 г води – це розчин: 1. 89 %-ний. 3. 11 %-ний. 2. 100 %-ний. 4. 1,1 %-ний. 92. Розчин солі BaCl2 має середовище: 1. Сильнокисле. 3. Лужне. 2. Нейтральне. 4. Слабкокисле. 93. Ступінь окиснення сульфуру у сполуці BaS2O3: 1.+2. 3. +6. 2. +7. 4. +4. 94. СdO відноситься до оксидів: 1. Основних. 3. Амфотерних. 2. Кислотних. 4. Несолетвірних. 95. Сполука Cd(ОН)2 дисоціює як: 1. Кислота. 3. Амфотерна сполука. 2. Основа. 4. Сіль. 96. Еквівалент Cd дорівнює: 1. Ar(Cd)/2. 3. Ar(Cd)/3. 2. Ar(Cd)/1. 4. Ar(Cd)/4. 97. Розчин має рН = 3,7 це середовище: 1. Сильнокисле. 3. Лужне. 2. Нейтральне. 4. Слабкокисле. 98. Змішали 2,7 г солі і 92,3 г води – це розчин: 1. 92,3 %-ний. 3. 100 %-ний. 2. 2,7 %-ний. 4. 27 %-ний. 99. Розчин солі Cd(NO3)2 має середовище: 1. Сильнокисле. 3. Лужне. 2. Нейтральне. 4. Слабкокисле. 100. Ступінь окиснення хрому у сполуці CdCrO4: 1.+2. 3. +5. 2. +3. 4. +6.
ОСНОВИ СТАНДАРТИЗАЦІЇ, МЕТРОЛОГІЇ ТА УПРАВЛІННЯ ЯКІСТЮ 1. Вкажіть види стандартизації: 1. Міжнародна, національна, регіональна. 2. Міжнародна, національна, республіканська. 3. Національна, регіональна, республіканська. 4. Міжнародна, республіканська, регіональна. 2. Вид стандартизації, яка запроваджується на рівні однієї конкретної держави: 1. Регіональна. 2. Національна. 3. Державна. 4. Галузева. 3. Вкажіть види стандартизації, які діють лише на національному рівні: 1. Державна, міжнародна. 2. Національна, міждержавна. 3. Національна, галузева. 4. Галузева, міждержавна. 4. Вид стандартизації, участь у якій є відкритою для відповідних органів усіх країн: 1. Регіональна. 2. Міжнародна. 3. Національна. 4. Державна. 5. Вид стандартизації, яка запроваджується на рівні однієї країни від імені держави: 1. Міждержавна. 2. Національна. 3. Регіональна. 4. Галузева. 6. Назвіть вид стандартизації, яка діє у країнах СНД: 1. Національна. 2. Державна. 3. Міжнародна. 4. Міждержавна. |
||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 817. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
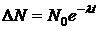 ;
;
 ;
;
 ;
;
 .
.