Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Дифференциальная диагностикаНЕСПЕЦИФИЧЕСКИЙ ЯЗВЕННЫЙ КОЛИТ Неспецифический язвенный колит (НЯК) - хроническое рецидивирующее заболевание кишечника неизвестной этиологии, характеризующееся диффузным воспалением слизистой оболочки прямой и ободочной кишки. НЯК в иностранной литературе и в последнее время в России называют язвенным колитом. В ранней стадии НЯК проявляется нарушением целостности эпителия и сосудистой реакцией, позднее присоединяются изъязвления слизистой оболочки, не распространяющиеся глубоко в стенку кишки. В выраженной стадии слизистая оболочка отечна, с многочисленными небольшими или обширными язвами неправильной формы. В слизистой оболочке развиваются псевдополипы, что связано с регенерацией эпителия. При хронизации процесса репаративносклеротические изменения начинают преобладать, происходит рубцевание язв, образуются обширные зоны рубцовой ткани, приводящие к резкой деформации и укорочению кишки, просвет ее сужается. НЯК болеют люди всех возрастных групп (чаще в возрасте 20-40 и 60- 70 лет), мужчины и женщины болеют одинаково часто. Заболеваемость - 50- 80 на 100 тыс. населения. Чаще болеют жители Северной Америки и северной части Европы. Этиология Точных сведений о причине развития болезни в настоящее время нет. Предполагается наследственная предрасположенность (связь заболевания с носительством антигенов HLA-DR27 и B27), при которой инфекционные факторы (в том числе дисбактериоз) и иммунные реакции запускают воспалительный процесс. Патогенез Основными патогенетическими механизмами являются изменение иммунологической реактивности, дисбактериоз и своеобразие нервно-вегетативных реакций организма (рис. 3-3).  Дисбактериоз и, в частности, увеличение количества Escherichia coli и Yersinia оказывают местное токсическое и аллергизирующее влияние. Особенности нервно-вегетативных реакций вызывают дисфункцию вегетативной и гормональной регуляции, а также изменение проницаемости слизистой оболочки толстой кишки. В результате облегчается проникновение веществ, обладающих антигенными свойствами. Известно, что антигены некоторых штаммов E. coli индуцируют синтез антител к ткани кишечника. Цитопатогенное действие противотолстокишечных антител сочетается с действием протеолитических и иных продуктов метаболизма микрофлоры кишечника и вызывает иммунное и неиммунное воспаление стенки кишечника. Иммунные механизмы обусловливают вовлечение в патологический процесс других органов и систем (внекишечные поражения), к которым относятся поражения кожи, органа зрения, полости рта, опорно-двигательного аппарата, системы крови.
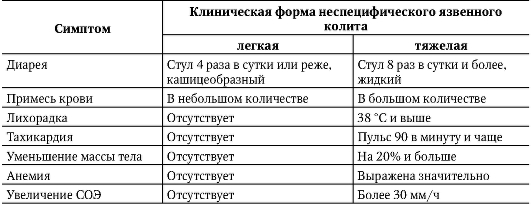
Рис. 3-3. Патогенез неспецифического язвенного колита Классификация В настоящее время общепринятой классификации НЯК нет. Для практических целей выделяют 3 основные формы:острую, хроническую и рецидивирующую. В пределах каждой клинической формы встречаются легкие, среднетяжелые и тяжелые варианты течения болезни. • Острая (молниеносная)форма встречается редко, отличается тяжестью общих и местных проявлений, ранним развитием осложнений. Процесс развивается бурно, как правило, захватывает всю толстую кишку. • Хроническая формахарактеризуется непрерывным, длительным, истощающим течением, с постепенным нарастанием симптоматики. • Рецидивирующая формавстречается наиболее часто. Для нее характерны ремиссии продолжительностью 3-6 мес и более, сменяющиеся обострениями различной выраженности. Одна клиническая форма может переходить в другую. НЯК всегда поражает прямую кишку и, прогрессируя, распространяется проксимально. В связи с этим выделяют проколит, левосторонний колит, тотальный колит. Тяжесть заболевания обусловлена степенью воспаления и топографией патологического процесса толстой кишки. Наиболее часто наблюдается проктосигмоидит (67%), тотальный колит встречается у 16% больных, изолированный проктит - у 5%. Клиническая картина Проявления болезни обусловлены обширностью и выраженностью поражения толстой кишки и внекишечными проявлениями, однако на первом месте стоят «кишечные» симптомы. На первом этапе диагностического поискавыявляют жалобы на диарею, жидкий или кашицеобразный стул, наличие в нем крови, слизи и гноя. Выделяют несколько вариантов начала заболевания. • Постепенное появление поноса; через несколько дней в жидких испражнениях обнаруживают слизь, кровь. • Болезнь дебютирует ректальными кровотечениями при оформленном или кашицеобразном стуле. Потеря крови при дефекации в первые дни обычно незначительная. • Появление диареи с кровью и слизью, болью, интоксикацией. При развернутой картине болезни дискинетический и язвенно-геморрагический синдромы проявляются в виде частого жидкого стула с примесью крови и гноя, иногда слизи, что служит основным симптомом. Стул до 20 раз в сутки, а при тяжелом течении число дефекаций достигает 40 и более, преимущественно ночью и утром. Больные тяжелой формой НЯК нередко страдают недержанием кала, что связано с поражением наружного сфинктера заднего прохода и общей слабостью. Примесь крови в стуле бывает значительной, иногда выделения из толстой кишки состоят из одной крови. В период обострения больные в день теряют 100-300 мл крови. Количество слизи в испражнениях зависит от сохранности слизистой оболочки кишки. При тотальном глубоком поражении слизистой оболочки слизь в испражнениях отсутствует. В период обострения испражнения представляют собой зловонную гнойнослизистую жидкость с примесью крови. Во время ремиссии понос может полностью прекратиться, но чаще стул кашицеобразный, 3-4 раза в день, с незначительным включением слизи и крови. Обязательный симптом тотального НЯК - схваткообразные боли. Больные не всегда могут точно определить локализацию боли, лишь приблизительно указывая зону основного поражения. Чаще всего это область сигмовидной ободочной и прямой кишки, реже - область пупка и слепой кишки. Типично усиление болей перед дефекацией и ослабление после опорожнения кишечника. Прием пищи также усиливает боль и диарею, так что иногда больные отказываются от еды. Поражение прямой и сигмовидной ободочной кишки приводит к тенезмам. Позывы на дефекацию носят резко императивный характер. Больные нередко отмечают чувство неполного опорожнения прямой кишки. При неспецифическом язвенном проктите и проктосигмоидите некоторые больные отмечают запор по 2-3 дня, чередование поноса с запором, которое носит спастический характер. Практически все больные жалуются на слабость, похудание. В период ремиссии состояние улучшается, увеличивается масса тела. С каждым рецидивом слабость и похудание прогрессируют. При проктите и проктосигмоидите масса тела обычно не снижается, аппетит сохранен, слабость умеренная. При молниеносной форме бурно нарастают явления интоксикации: тошнота, рвота, высокая температура тела, слабость вплоть до адинамии. Похудание быстро достигает степени кахексии. Развиваются синдром органных поражений и астеноневротический синдром в виде резкого изменения психики (больные становятся обидчивыми, плаксивыми, утрачивают чувство юмора). Неэффективность противодизентерийной терапии в дебюте, дальнейшее прогрессирование заболевания, вовлечение других органов и систем позволяют заподозрить тяжелое поражение кишечника, в том числе НЯК, опухоль, туберкулез и т.д. На втором этапе диагностического поискавыявляют клинические признаки дистрофическо-анемического и дискинетического синдромов, местных и системных осложнений. При остром течении и тотальном поражении кишечника больные впадают в прострацию, истощены, обезвожены. Наблюдается сухость кожи и слизистых оболочек, резко снижен тургор. Кожные покровы бледные, температура тела 39-40 °С и выше. Отмечаются тахикардия, артериальная гипотензия, уменьшение диуреза. Печень и селезенка нередко увеличены. Пальпируется болезненная урчащая толстая кишка с уплотненными стенками. Кожа вокруг заднего прохода мацерирована, слизистая оболочка прямой кишки пролабирует. Острая форма часто сопровождается осложнениями. Наибольшую опасность представляет перфорация, возможны множественные перфорации. Перфорации, возникшие на фоне тяжелой интоксикации, резких болей в животе, часто протекают атипично, без бурного начала, без острых болей. Не сразу возникает мышечная защита. В связи с этим наличие перфорации можно предполагать на основании только общего ухудшения состояния больного в сочетании с учащением пульса, падением АД. Для острой токсической дилатации толстой кишки характерны резкое расширение и вздутие отдельных сегментов, чаще поперечной ободочной кишки. Участок кишки резко растягивается жидкостью и газами, что может закончиться прободением и перитонитом. При этом осложнении частота дефекации уменьшается, стул теряет каловый характер, увеличивается выделение крови, гноя и слизи. Определяются высокая лихорадка, значительная тахикардия, коллапс. Живот вздут, пальпация по ходу вздутых участков толстой кишки резко болезненна. Перистальтика вялая или отсутствует. При хронической форме НЯК в клинической картине преобладают проявления гиповитаминоза, анемии, эндокринных расстройств (дистрофическианемический синдром). На втором этапе выявляется также ряд патологических изменений других органов и систем (синдром органных поражений). Типичным проявлением кожных изменений НЯК служит узловатая эритема: появляются единичные или множественные узлы, чаще на разгибательной поверхности голеней. При тяжелых формах болезни встречаются гангренозная пиодермия и массивные изъязвления кожи нижних конечностей. Для тяжелых форм НЯК характерны также поражение слизистой оболочки рта, афтозный стоматит, глоссит и гингивит. Обычно отмечается изъязвление края или нижней поверхности языка, реже десен. Боли при приеме пищи настолько сильны, что больные отказываются от пищи. Возможен язвенный эзофагит. При НЯК могут возникать ириты, конъюнктивиты и блефариты. Отмечается четкая зависимость выраженности глазных симптомов от формы и фазы болезни. НЯК может осложниться полиартритом. Обычно поражаются голеностопные и коленные суставы с небольшим ограничением движений и нерезкими болями. Артриты возникают одновременно с НЯК и исчезают при ремиссии, не оставляя деформации. У некоторых больных развиваются спондилиты. Сравнительно часто НЯК осложняется сужением просвета кишки, что проявляется картиной толстокишечной непроходимости. При пальцевом исследовании прямой кишки можно выявить осложнения, которые при НЯК возникают часто (перианальные абсцессы, анальные трещины, парапроктит, флегмона клетчатки параректального пространства, прямокишечные и ректовагинальные свищи). На третьем этапевыявление характерных изменений слизистой оболочки толстой кишки позволяет поставить окончательный диагноз. Для постановки диагноза НЯК (с учетом постоянного поражения прямой кишки) достаточно ректороманоскопии. В начале болезни наблюдаются отек и контактная гиперчувствительность слизистой оболочки. Малейшее механическое раздражение ведет к кровотечению (контактная кровоточивость). Слизистая оболочка гиперемирована, отечна, покрыта слизью, под которой отмечается «зернистость» с точечными и мелкими изъязвлениями. Позднее под слизистой оболочкой образуются характерные просовидные абсцессы; после их вскрытия остаются мелкие язвы, которые в дальнейшем сливаются. При тяжелой острой форме возможно полное разрушение слизистой оболочки и глубжележащих слоев; внутренняя поверхность становится более гладкой, стенка хрупкой, легко рвется. Стиханию клинических проявлений соответствует эндоскопическая картина в виде частичной эпителизации, уменьшения размеров язв, появления псевдополипов. В период ремиссии происходит полная эпителизация, слизистая оболочка гладкая, со стертым сосудистым рисунком, могут выявляться мелкие псевдополипы. Для определения степени и характера поражения толстой кишки, выявления ряда осложнений следует проводить ирригоскопию. Рентгенологическая картина в ранние стадии НЯК при неглубоких морфологических изменениях скудна и неспецифична. После длительного лечения при рентгенологическом исследовании выявляют отсутствие гаустрации, ригидность, равномерные атрофию и сужение кишки, ее укорочение. Кишка имеет вид «водопроводной трубы». В фазу обострения можно выявить изменение рельефа: широкие поперечные валики с краевыми зубцами, псевдополипоз. Этот метод может обнаружить стриктуру кишки и возможную малигнизацию. При токсической дилатации толстой кишки, в связи с опасностью ирригоскопии (провокация перфорации), диагностическое значение приобретает обзорная рентгенография: на снимках видны растянутые (от 10 см и более) сегменты кишки. При подозрении на перфорацию следует чаще прибегать к обзорной рентгеноскопии брюшной полости для обнаружения «свободного» газа. Фиброколоноскопияпозволяет точно определить характер изменений на всем протяжении толстой кишки, а также выявить поражение илеоцекального клапана (баугиниева заслонка) и терминального отдела тонкой кишки. При хроническом течении НЯК и в фазе ремиссии в диагностике помогают эндомикроскопическое исследование и биопсия слизистой оболочки. Лабораторное исследование крови позволяет определять степень и характер анемии. При массивном кишечном кровотечении возникает острая постгеморрагическая анемия. Постоянная ежедневная, даже «скрытая» кровопотеря также приводит к дефициту железа в организме и развитию анемии. У некоторых больных развивается приобретенная аутоиммунная гемолитическая анемия (с положительной реакцией Кумбса, ретикулоцитозом и неконъюгированной гипербилирубинемией). При тотальном НЯК с вовлечением тонкой кишки возникает дефицит фолиевой кислоты и витамина B12, в генезе которого определенную роль играет дисбактериоз. Для острого НЯК и рецидивов характерны повышение СОЭ и небольшой лейкоцитоз со сдвигом лейкоцитарной формулы влево. Важным является определение СОЭ в динамике, так как количество лейкоцитов часто остается нормальным даже в тяжелых случаях, что связывают с гипокортицизмом и приемом сульфаниламидов. Нечасто возникающий высокий лейкоцитоз почти всегда служит сигналом тяжелого осложнения. Биохимическое исследование крови помогает установить степень нарушения белкового и электролитного обмена, а также выявить поражение печени и почек. Копрологическое исследование отражает степень воспалительно-деструктивного процесса. Микроскопически обнаруживают скопления лейкоцитов, эритроциты, большие скопления клеток кишечного эпителия. Резко положительная реакция на растворимый белок в кале (проба Трибуле) свидетельствует также о воспалении кишечной стенки. Бактериологическое исследование кала в дебюте НЯК помогает исключить острую дизентерию. Определение характера и степени дисбактериоза необходимо для проведения антибактериальной терапии. Показательными для нарушенного биоценоза кишечника служат количественные сдвиги облигатной микрофлоры: отсутствие роста бифидобактерий в разведении 10-7 и резкое изменение количества кишечной палочки. Дисбактериоз проявляется также высоким представительством кишечной палочки со слабовыраженными ферментативными свойствами (более 10%), лактозонегативных энтеробактерий (более 5%), появлением микроорганизмов рода протея, грибов рода кандида, гемолизирующих эшерихий, стафилококка. Диагностика Распознавание НЯК основано на выявлении следующих признаков: • «характерных» изменений стула: частый, неоформленный стул с примесью крови и гноя; • патологических изменений при копрологическом исследовании: скудные неоформленные испражнения, кровь, слизь, гной в кале, стул типа «малинового желе»; резко положительная реакция на растворимый белок; • «специфических» изменений слизистой оболочки: контактная кровоточивость, отсутствие сосудистого рисунка, просовидные абсцессы, язвы различной величины и формы, псевдополипы; • «типичных» изменений кишки при ирригоскопии: укорочение, сужение, отсутствие гаустрации, кишка в виде «водопроводной трубы». На основании данных, полученных на всех трех этапах диагностического поиска, выработаны критерии тяжести НЯК (табл. 3-2). Дифференциальная диагностика В силу того что клиническая картина НЯК сходна с проявлениями других поражений кишечника, его приходится дифференцировать от ряда заболеваний. Таблица 3-2. Клинико-лабораторные критерии тяжести неспецифического язвенного колита
Прежде всего, НЯК дифференцируют от острой инфекционной диареи. НЯК протекает тяжелее, быстро возникают осложнения, введение антибиотиков не улучшает состояния, как при бактериальной дизентерии, а усугубляет его. При бактериальной дизентерии, в отличие от НЯК, ректороманоскопия не выявляет обширных язвенных полей, диффузной кровоточивости, псевдополипоза. Диарея, возбудителем которой служит Clostridium difficili (псевдомембранозный колит), обусловлена приемом антибиотиков, возникает остро, с лихорадкой, кровавой диареей. В диагностике псевдомембранозного колита (ПМК), ишемического колита вследствие нарушения мезентериального кровоснабжения, дивертикулита ведущая роль принадлежит эндоскопическому исследованию. НЯК следует дифференцировать также от БК (терминальный илеит), при которой отмечают боли в илеоцекальной области, понос, сменяющийся запором (без примеси крови), лихорадку, анемию. Поперечная и нисходящая ободочная кишка интактны, поэтому не наблюдаются понос и выраженные кровотечения. В ряде случаев в патологический процесс вовлекается сигмовидная, ободочная и прямая кишка, и тогда дифференцировать НЯК можно только по данным эндоскопического исследования, а также микроскопии биоптата слизистой оболочки. При хронических формах НЯК, когда ведущими симптомами служат кашицеобразный стул и выделение крови из прямой кишки, дифференциальную диагностику проводят с новообразованием прямой и толстой кишки. Окончательный диагноз ставят с учетом результатов эндоскопии. Формулировка развернутого клинического диагнозастроится по следующей схеме: • клиническая форма; • степень вовлечения отделов толстой кишки; • степень тяжести; • фаза заболевания; • осложнения. Лечение Объем лечебных мероприятий зависит от тяжести течения болезни, фазы (обострение или ремиссия) и наличия или отсутствия осложнений. Комплексное лечение предусматривает борьбу с воспалительным процессом, воздействие на моторику и микрофлору кишечника, коррекцию обменных нарушений, создание психического и физического покоя. Общие мероприятия включают диету, создание физического и психического покоя. Больные с НЯК легкого течения в госпитализации не нуждаются. Пища должна быть достаточно калорийной и включать 110-120 г белка в сутки, в период обострения больного переводят на диету № 4 (механически щадящая пища с исключением сырых и вареных овощей, фруктов, молока), при стихании обострения пища может быть непротертой. В период ремиссии некоторые больные не переносят определенные продукты, которые следует исключить из рациона, это касается молока, винограда, изюма, кваса, пива. Больные НЯК эмоционально лабильны, тревожны. Большая роль принадлежит доверительным взаимоотношениям врача и больного. При необходимости назначают седативные препараты или, главным образом, антидепрессанты. Больные с тяжелым течением болезни нуждаются в неотложной госпитализации и строгом постельном режиме. Назначают парентеральное питание (путем катетеризации подключичной вены вводят различные растворы - аминопептид*, альвезин, липофундин* или интралипид*, глюкозу* вместе с электролитами и витаминами комплекса В*). Из противовоспалительных препаратов (если нет показаний к хирургическому лечению) назначают глюкокортикоиды, особенно если одновременно имеются внекишечные проявления болезни. Преднизолон вначале вводят внутривенно (в дозе эквивалентной 40 мг преднизолона), при недостаточном эффекте добавляют цитостатики (азатиоприн внутрь по 2,5 мг/кг в сутки). Затем переходят на прием преднизолона внутрь (1 мг/кг массы тела); при достижении эффекта дозу постепенно снижают. При лихорадке, клинических симптомах септического состояния назначают антибактериальную терапию ципрофлоксацин внутривенно по 500 мг каждые 8 ч до стихания симптомов. При НЯК средней тяжести в периоде обострения больных необходимо госпитализировать. Назначают преднизолон 40-60 мг/сут (снижая дозу в зависимости от клинической картины на 5-10 мг в неделю) и месалазин внутрь по 4,0 г/сут, снижая дозу при достижении ремиссии приблизительно на 1 мг в неделю. Исчезновение симптомов, нормализация эндоскопической картины и лабораторных показателей свидетельствуют об эффективности лечения. Эффективность сульфасалазина и месалазина оценивают на 14-21-й день терапии, глюкокортикоидов - на 7-21-й день, азатиоприна - через 2-3 мес. В фазе ремиссии, для которой характерно отсутствие жалоб, лихорадки, анемии и других патологических показателей, обычно назначают на длительное время прием сульфасалазина по 2-3 г/сут без существенных ограничений в диете или месалазин 1,0-1,5 г/сут. Если рентгенологические, эндоскопические данные нормальны в течение длительного времени (не менее 2 лет), то можно на несколько месяцев полностью отменить прием сульфасалазина. В периоды обострения или же при сохранении ряда симптомов в периоде улучшения состояния при частом стуле используют антидиарейные препараты - реасек3 (ломотил3) по 20-30 мг в день, желательно сочетание его со спазмолитиками; следует применять также вяжущие средства (отвар коры дуба, плодов черники, черемухи). Лицам с длительностью НЯК более 10 лет следует проводить колоноскопию 1-2 раза в год (опасность малигнизации). Борьба с осложнениями включает в себя консервативное лечение острой токсической дилатации толстой кишки. Для этого необходимо ограничить прием пищи и полностью отменить холинолитики и опиаты. Требуется полноценная коррекция электролитного обмена, особенно калиевого, а также восполнение потери жидкости и белка. Проводят гемотрансфузии, как правило, прямое переливание крови. Назначают антибиотики широкого спектра действия. Осторожно проводят декомпрессию желудка с помощью зонда. Клизмы противопоказаны. Необходимо соблюдать осторожность с газоотводной трубкой (опасность перфорации сигмовидной и ободочной кишки). Применение сульфасалазина позволило ограничить прием глюкокортикоидов и проводить длительные курсы поддерживающей терапии. Считается, что действующим эффектом обладает 5-аминосалициловая кислота; клинические наблюдения позволяют считать, что и сам сульфасалазин, как комплексный препарат, обладает противовоспалительным эффектом. Сульфасалазин обладает как дозозависимыми побочными эффектами (тошнота, рвота, головная боль, алопеция), так и дозонезависимыми (агранулоцитоз, гемолитическая анемия, гепатит, панкреатит, фиброз легких). Применение при НЯК блокатора ФНО-а - инфликсимаба не получило однозначной оценки. При неэффективности консервативных мероприятий выполняют тотальную колэктомию с наложением илеостомы (одномоментно). В случае перфорации толстой кишки ушивание не производят. Показана гемиили тотальная колэктомия с наложением илеостомы. Показания к оперативному лечению: • обоснованное подозрение на перфорацию; • острая токсическая дилатация толстой кишки, не поддающаяся терапии в течение 24 ч; • профузное кишечное кровотечение; • неэффективность комплексной интенсивной терапии при острой тяжелой форме в течение 7-10 дней; • неэффективность комплексной терапии рецидивирующего НЯК; • развитие стриктур с явлениями частичной кишечной непроходимости; • малигнизация. У больных с илеостомой в дальнейшем необходимо стремиться к осуществлению реконструктивных и восстановительных операций (илеоректальный анастомоз, создание искусственной ампулы и т.д.). Прогноз Прогноз при НЯК зависит от клинической формы заболевания, распространенности процесса и тяжести его течения. При тяжелом течении НЯК прогноз неблагоприятный вследствие развития различных осложнений. Комплексная терапия может смягчить проявления болезни, однако полной и длительной ремиссии обычно не наступает. Профилактика Специфические профилактические меры неизвестны. Профилактика сводится к предупреждению обострений, что достигается упорным лечением. Больных ставят на диспансерный учет, чтобы своевременно выявить начинающееся обострение или осложнение.
БОЛЕЗНЬ КРОНА Болезнь Крона (БК) - хроническое рецидивирующее заболевание неясной этиологии, характеризующееся гранулематозным воспалением с сегментарным поражением разных отделов пищеварительного тракта. Патологический процесс при БК локализуется преимущественно в кишечнике, хотя могут поражаться все отделы ЖКТ, включая пищевод, желудок, ротовую полость. Выделяют БК с поражением подвздошной кишки (терминальный илеит) - 30-35%; илеоцекального отдела - около 40%; толстой кишки, включая аноректальную зону, - 20%; тонкой кишки - 10%. В 5% случаев болезнь может дебютировать с поражением пищевода, желудка, двенадцатиперстной кишки или перианальной области. Неспецифическое иммунное воспаление распространяется на всю толщу кишечной стенки, имеет регионарный характер: зоны воспалительной инфильтрации клеточными элементами (лимфоциты, плазматические клетки, в меньшей степени - нейтрофилы) чередуются с относительно неизмененными участками кишки. В слизистой оболочке, в зоне инфильтрации образуются глубокие язвы, развиваются абсцессы и свищи с последующим рубцеванием и сужением просвета кишки. Протяженность поражения пищеварительного тракта при БК весьма различна: от 3-5 см до 1 м и более. Распространенность БК в разных регионах мира колеблется в широких пределах - 20-150 случаев на 100 000 населения. Отмечено, что БК страдают чаще люди трудоспособного возраста (20-50 лет) обоего пола. У родственников первой линии пациентов с БК риск развития данного заболевания в 10 раз выше, чем в популяции. Этиология Причины развития болезни неизвестны. Предполагают этиологическую роль бактерий, вирусов, пищевых аллергенов, генетических факторов (семейный характер болезни отмечен в 5% случаев). Отмечено, что БК ассоциируется с антигеном гистосовместимости HLA-B27. Патогенез Точные представления о механизмах развития болезни отсутствуют. В настоящее время рабочей гипотезой служит предположение о нарушении иммунного ответа организма на кишечную микрофлору у генетически предрасположенных лиц. Предполагают, что органы иммуногенеза вырабатывают аутоантитела к клеткам слизистой оболочки кишечника, а также сенсибилизированные лимфоциты, обладающие повреждающим действием. Отмечено, что кишечной микрофлоре принадлежит важная роль, так как при БК выявляются значительные нарушения микробиоценоза кишечника. Характерно уменьшение количества бифидобактерий при одновременном увеличении числа энтеробактерий и появлении энтеробактерий с признаками патогенности. В развитии воспалительного процесса придают большое значение провоспалительным цитокинам, в особенности фактору некроза опухоли-а (ФНО-а), который синтезируется разными типами клеток (макрофагами, Т-лимфоцитами, клетками эндотелия). При воспалении ФНО-а ведет себя как активный провоспалительный агент. Биологические реакции, связанные с его гиперпродукцией, весьма обширны (в частности, индукция синтеза свободных кислородных радикалов, увеличение сосудистой проницаемости, торможение апоптоза воспалительных клеток, индукция синтеза ИЛ-1, ИЛ-2 и др.). Одни из самых мощных индукторов ФНО-а - бактериальные липополисахариды, которые при БК в избытке присутствуют в просвете толстой кишки, поэтому нарушение состава микрофлоры может быть причиной повышения уровня этого цитокина. Кроме того, ФНО-а участвует в формировании воспалительной гранулемы. Воспалительный процесс при БК начинается в подслизистом слое и распространяется на все слои кишечной стенки. В подслизистом слое на фоне диффузной инфильтрации лимфоцитами и плазматическими клетками отмечается гиперплазия лимфоидных фолликулов, которые могут изъязвляться. Язвы при БК имеют удлиненную щелевидную форму и глубоко проникают в подслизистый и мышечные слои, образуя свищи и абсцессы. Наличие свищей, стриктур и кишечного стаза способствует развитию дисбактериоза. Распространенное поражение тонкой кишки вызывает тяжелый синдром нарушения всасывания (мальабсорбция). Снижение всасывания железа, витамина B12 и фолиевой кислоты вызывает анемию, чему способствуют и повторные кровопотери. Возникновение воспалительного процесса и изъязвлений в кишечнике приводит также к интоксикации, профузным поносам, потере массы тела, нарушениям электролитного обмена. Клиническая картина Клинические проявления и характер течения заболевания определяются тяжестью морфологических изменений, анатомической локализацией и протяженностью патологического процесса, наличием осложнений и внекишечных поражений. К проявлению собственно кишечных поражений относят боль в животе, диарею, синдром недостаточного всасывания, поражения аноректальной области (свищи, трещины, абсцессы), ректальные кровотечения (редко). К внекишечным признакам относят лихорадку, анемию, снижение массы тела, артрит, узловатую эритему, афтозный стоматит, поражения глаз (ирит, увеит, эписклерит), вторичную аменорею у женщин. Однако, несмотря на значительную вариабельность клинических проявлений при БК, в 90% случаев доминируют боль в животе, диарея, снижение массы тела. На первом этапе диагностического поискаобращают на себя внимание боли в животе, которые бывают практически у всех больных, они носят чаще тупой или схваткообразный характер (при поражении толстой кишки). Максимальная выраженность болей отмечается при вовлечении в процесс тонкой кишки. Причины болей разнообразны: • вовлечение в патологический процесс брюшины; • повышение давления в просвете кишки в результате повышенного газообразования и увеличения объема кишечного содержимого вследствие нарушения всасывания; • наличие осложнений (частичная кишечная непроходимость, свищи, абсцессы). Больные также предъявляют жалобы на диарею, имеющую достаточно упорный характер. Частота стула достигает 4-6 раз в сутки, масса испражнений - более 200 г в сутки, кал разжиженный или водянистый. Диарея возникает после каждого приема пищи, но может быть и ночью. Объем стула зависит от локализации патологического процесса в кишечнике: при поражении высоких отделов тонкой кишки объем кала оказывается большим, нежели при дистальной локализации воспалительного процесса. Тенезмы отмечаются лишь при вовлечении в процесс аноректальной области. Ректальные кровотечения, обычно необильные, отмечаются у половины больных. В период обострения отмечается лихорадка, сочетающаяся с общей слабостью и уменьшением массы тела. Температура тела может повышаться до 39 °С. В ряде случаев повышение температуры «опережает» местные кишечные симптомы, такая ситуация может продолжаться в течение длительного времени, что создает большие диагностические трудности. Другое частое внекишечное проявление болезни - боли в крупных суставах (артралгии). Таким образом, при сборе анамнеза выявляют кишечные симптомы и системные (внекишечные) проявления. Эти признаки не позволяют еще сформулировать определенную диагностическую концепцию, однако направление диагностического поиска можно определить. Гораздо сложнее, когда в клинической картине доминируют «общие» признаки: лихорадка, уменьшение массы тела, артралгии, артрит. На втором этапе диагностического поискауточняют симптомы со стороны ЖКТ в виде болезненности при пальпации живота (преимущественно вокруг пупка), урчания, болезненного уплотнения терминального отдела подвздошной кишки, болезненности, урчания и «шума плеска» при пальпации слепой кишки. Отмечают уменьшение массы тела, особенно при длительном течении болезни. Снижение массы тела обусловлено, прежде всего, синдромом нарушенного всасывания. Синдром нарушенного всасыванияимеет сложный патогенез и обусловлен рядом факторов: • уменьшением всасывающей поверхности кишки из-за воспалительного процесса слизистой оболочки; • дефицитом кишечных ферментов (дисахаридазы, лактазы); • снижением активности панкреатических ферментов; • нарушением всасывания желчных кислот, что приводит к блокированию всасывания воды и электролитов. Кроме того, снижение массы тела связано с уменьшением приема пищи вследствие анорексии (особенно в период обострения болезни). В 25% случаев можно обнаружить перианальные поражения: отек кожи вокруг анального сфинктера, трещины и изъязвления сфинктера, свищи и периректальные абсцессы. При этом наружные анальные поражения превалируют над поражением слизистой оболочки прямой кишки, в отличие от НЯК, при котором эти соотношения обратные. При осмотре могут быть выявлены внекишечные проявления в виде артрита крупных суставов (дефигурация сустава), узловатой эритемы, поражения глаз. При тяжелом течении болезни и выраженном синдроме нарушенного всасывания отмечают симптомы гиповитаминоза и дефицита железа: сухость кожи, выпадение волос, ломкость ногтей, хейлит, глоссит, кровоточивость десен. На третьем этапе диагностического поисканеобходимо убедиться в характере и обширности поражения кишечника, а также оценить выраженность обменных расстройств и внекишечных поражений. Для постановки окончательного диагноза прежде всего необходимо выполнить эндоскопию (колоноскопию), позволяющую осмотреть слизистую оболочку всей толстой кишки и терминального отдела подвздошной. Выявляются отечность слизистой оболочки, исчезновение сосудистого рисунка, небольшие афтозные язвы с последующим образованием глубоких щелевидных трещин, изменяющих рельеф слизистой оболочки по типу «булыжной мостовой», возможно появление стриктур кишки. Биопсия слизистой оболочки кишки выявляет характерные морфологические изменения в виде гранулем туберкулоидного и саркоидного типов, содержащие многоядерные гигантские клетки Пирогова-Лангханса. Аналогичные изменения слизистой оболочки выявляются и при фиброгастродуоденоскопии (в случаях поражения верхних отделов ЖКТ). Рентгенологическое исследование кишечника (ирригоскопия, энтероскопия) в выраженных случаях болезни демонстрирует сегментарность поражения кишечника с наличием неизмененных участков кишки между пораженными сегментами. В области поражения отмечают волнистый или неровный контур кишки, продольные язвы, образующие рельеф «булыжной мостовой», псевдодивертикулы (представляющие собой глубокие язвы, проникающие в результате фиброзных изменений в кишечную стенку - «симптом шнура»). Лабораторное исследование крови позволяет определить степень и характер анемии (железодефицитная, В12-дефицитная). Для рецидива болезни характерны повышение СОЭ, иногда достигающее значительных величин (50-60 мм/ч). Биохимическое исследование крови отражает нарушения белкового, жирового и электролитного обмена (гипоальбуминемия, гиполипидемия, гипогликемия, гипокальциемия), обусловленные выраженностью синдрома нарушенного всасывания. Для выявления нарушения всасывания используют также тест с D-ксилозой и цианокобаламином (тест Шиллинга). Более детально на этих тестах авторы останавливались при описании ХЭ. Анализ кала предусматривает микроскопию, химическое и бактериологическое исследование. Недостаточность переваривания и всасывания в тонкой кишке проявляется большим количеством мышечных волокон, значительным количеством жирных кислот и мыл; определяется небольшое количество соединительной ткани, нейтрального жира и йодофильной флоры. Степень изменений копрограммы обусловлена тяжестью болезни и ее фазой (ремиссия-обострение). При вовлечении в патологический процесс других органов системы пищеварения (печень, желчные пути, поджелудочная железа) лабораторно-инструментальным исследованием можно обнаружить соответствующие изменения. Осложнения Большинство осложнений БК - хирургическая проблема: кишечная непроходимость, перфорация кишки с развитием абсцессов и перитонита, кишечные кровотечения, формирование энтеро-энтеральных, кишечно-кожных, кишечно-пузырных и ректовагинальных свищей. Диагностика Распознавание болезни в развитой форме при наличии болей и типичных кишечных симптомов, увеличенной СОЭ не представляет сложностей и основывается на сочетании эндоскопических, рентгенологических и морфологических данных, свидетельствующих о наличии очагового, асимметричного, трансмурального и гранулематозного воспаления. Однако достаточно часто возникают ситуации, когда в течение длительного периода доминируют общие симптомы: лихорадка, снижение массы тела, признаки гиповитаминоза, неспецифические лабораторные показатели при отсутствии местных кишечных признаков. Это существенно затрудняет своевременную диагностику, заставляя врача предполагать совершенно иное заболевание. Во всяком случае в круг диагностического поиска при БК включается большое количество заболеваний, имеющих сходные черты с БК. Прежде всего, это злокачественные образования, хронические инфекции, системные заболевания (диффузные заболевания соединительной ткани). Несмотря на совершенство методов исследования, диагноз БК ставят спустя 1-2 года после появления первых симптомов. Если доминируют «кишечные» симптомы, то диагностировать болезнь можно значительно раньше. При наличии «кишечных» симптомов дифференциальная диагностика проводится с кишечными инфекциями (дизентерия, сальмонеллез), НЯК, хроническим неязвенным колитом, ХЭ, раком толстой кишки. В любом случае при наличии «кишечных» симптомов у больного БК должна включаться в круг диагностического поиска. Формулировка развернутого клинического диагнозастроится по следующей схеме: • клиническая форма (с учетом преимущественного поражения тех или иных отделов желудочно-кишечного тракта); • степень тяжести поражения кишечника (с учетом данных эндоскопии); • фаза заболевания (ремиссия-обострение); • внекишечные поражения; • осложнения. Лечение При лечении БК следует учитывать локализацию процесса, активность и продолжительность заболевания, возраст и общее состояние больного. Диета, приближаясь к нормальной, не должна содержать плохо переносимые продукты. При поражении тонкой кишки с наличием стеатореи и непереносимости жиров рекомендуют диету с высоким содержанием белка и ограничением жира, лактулозы и грубоволокнистых продуктов. Этиологическая терапия БК невозможна, так как этиология и патогенез болезни неизвестны. Тем не менее к препаратам первого ряда относят сульфасалазин, глюкокортикоиды и метронидазол. При обострении легкой и средней тяжести в случае локализации процесса в подвздошной и толстой кишке показан прием месалазина 3-4 г/сут внутрь с постепенным снижением дозы при достижении ремиссии (приблизительно 1 г в неделю) или же назначают сульфасалазин внутрь 3-6 г/сут, а затем по 2-4 г/сут в течение 6-8 нед с постепенным переходом на поддерживающую дозу (половина лечебной), которая сохраняется не менее 1 года. Препарат принимают вместе с пищей, что предупреждает раздражение желудка. Возможно применение метронидазола внутрь по 10 мг/кг в сутки, однако длительно этот препарат назначать не следует из-за опасности развития периферической полиневропатии. При обострениях средней тяжести и тяжелых используют глюкокортикоиды внутрь - преднизолон по 40-60 мг/сут сроком до 4 нед с последующим снижением дозы (по 5 мг каждую неделю). Поддерживающая доза может составлять 5-10 мг в течение 6 мес и более. Более 50% пациентов, получавших глюкокортикоиды в фазе обострения, становятся гормонозависимыми или гормонорезистентными. Добавление к глюкокортикоидам азатиоприна (внутрь 2,5 мг/кг в сутки) или метотрексата парентерально (25 мг в неделю) эффективность лечения повышается. При диарее назначают антидиарейные препараты (лоперамид, реасек), ферментные препараты. Гипоальбуминемия корригируется введением плазмы, растворов альбумина и аминокислот, при электролитных нарушениях вводят растворы калия, кальция. По достижении ремиссии активную терапию в полной дозе медикаментов прекращают и переходят на поддерживающие дозы (сульфасалазин или месалазин (более 3 г/сут), возможно применение цитостатиков (азатиоприн или метотрексат) в сочетании с небольшими дозами глюкокортикоидов). Проводится заместительная терапия, включающая цианокобаламин, фолиевую кислоту, микроэлементы. Антидиарейные препараты (лоперамид, реасек) назначают при необходимости. Продолжительность ремиссии БК различна, в среднем она составляет 2 года. Прогноз Зависит от распространенности поражения, выраженности синдрома нарушенного всасывания и осложнений. Комплексная терапия может существенно смягчить проявления болезни, однако длительная ремиссия обычно не наступает. Хирургические вмешательства при патологии аноректальной области улучшают состояние больных. При адекватном лечении больные могут «сосуществовать» со своим заболеванием и вести полноценную жизнь. При развитии осложнений прогноз неблагоприятный. Профилактика Специфических методов профилактики не существует. Профилактика сводится к предупреждению обострений, что достигается упорным лечением. Больных ставят на диспансерный учет, чтобы своевременно выявить начинающееся обострение или осложнение.
Целиакия (глютеновая энтеропатия) — мультифакториальное заболевание, нарушение пищеварения, вызванное повреждением ворсинок тонкой кишки некоторыми пищевыми продуктами, содержащими определённые белки — глютен (клейковина) и близкими к нему белками злаков (авенин, гордеин и др.) — в таких злаках, как пшеница, рожь, ячмень и овёс. Имеет смешанный аутоиммунный, аллергический, наследственный генез, наследуется по аутосомно-доминантному типу.Механизм патологического взаимодействия глютена со слизистой оболочкой до конца не ясен. Предполагается наличие ферментного дефекта — отсутствие или недостаточность глиадинаминопептидазы или другого фермента, участвующего в расщеплении глютена. Важную роль играет иммунологическая реакция (гуморальная и клеточная) на глютен, происходящая в собственном слое слизистой оболочки тонкой кишки. Патогенез Целиакия характеризуется нарушением кишечного всасывания, суб- или атрофией слизистой оболочки тонкой кишки, положительной реакцией на аглютеновую диету (исключение из пищи продуктов из злаков, содержащих глютен). Среди клинических вариантов следует выделять истинную целиакию и синдром целиакии, который может развиться при самых разнообразных заболеваниях кишечника (аномалии развития, инфекции, продолжительный приём антибиотиков и др.). Начало целиакии нередко совпадает с введением в пищевой рацион ребенка прикормов, содержащих мучные изделия. Поэтому заболевают чаще дети в возрасте 6-12 мес. Этот период особенно опасен в плане провокации целиакии. Появляется учащённый пенистый стул, обильный, с резким запахом, светлый или с сероватым оттенком, жирный. В кале, как правило, не обнаруживается патогенная кишечная микрофлора. Лечение диспепсии обычными средствами (антибиотики, ферментные препараты, редукция в питании и др.) эффекта не дает. Ребёнок становится вялым, бледным, теряет массу тела, снижается аппетит. Постепенно развивается дистрофия и дети приобретают типичный для целиакии вид: резкое истощение, потухший взгляд, яркие слизистые оболочки, огромных размеров живот. В ряде случаев развиваются отёки на нижних конечностях, нередки спонтанные переломы костей. Определяется псевдоасцит (скопление жидкости в атоничном кишечнике). Далее присоединяются симптомы поливитаминной недостаточности (сухость кожи, стоматит, дистрофия зубов, ногтей, волос и др.). Как правило, при целиакии, особенно при длительном её течении, имеет место нарушенное всасывание дисахаров, жиров, витаминов, железа, кальция, нарушается транспорт цистина, обмен триптофана, то есть речь идет об универсальной мальабсорбции. В связи с этим понятен полиморфизм клинической картины. Дети страдают не только физически, но и психически (лабильность настроения, замкнутость, повышенная возбудимость, негативизм). Важным признаком заболевания при длительном его течении является низкорослость.
Течение целиакии волнообразное, нередко присоединяется вторичная инфекция, в ряде случаев - летальный исход. Диагностика Состояние часто диагностируется с большим опозданием, несмотря на принципиальную несложность: совокупность данных анамнеза, характерного вида больного, и, если на фоне безглютеновой диеты улучшается состояние больного, а отклонение от диеты приводит к появлению характерного для целиакии стула, предположительный диагноз может быть поставлен с определённой степенью надёжности. Для уточнения диагноза требуются: копрологическое исследование, показывающее наличие в кале большого количества жирных кислот и мыл; биохимическое исследование крови, показывающее гипопротеинемию, гипоальбуминемию, снижение концентрации холестерина и липидов, гипокальциемию, гипофосфатемию, гипосидеринемию, рентгенологическое исследование, показывающее остеопороз, горизонтальные уровни в петлях кишок, дискинезия кишечника. Окончательный диагноз устанавливается при металогическом анализе биоптатов слизистой оболочки тонкой кишки. Дифференциальный диагноз проводят с кишечной формой муковисцидоза, дисахаридазной недостаточностью, аномалиями желудочно-кишечного тракта. Чаще всего ложно-положительный диагноз встречается при таких заболеваниях, как диарея, синдром раздражённого кишечника. Лечение Лечение целиакии комплексное. Основа лечения — пожизненное соблюдение аглютеновой диеты (исключаются хлеб, сухари, печенье, кондитерские мучные и макаронные изделия, паштеты, колбасы). Дети хорошо переносят картофель, фрукты, овощи, кукурузную, рисовую и соевую муку, растительные жиры, мясо и рыбу и др. В мире налажен промышленный выпуск аглютеновых продуктов (фирмы «Dr. Shar» Италия, «Glutano» Германия, «Finax» Швеция, «Molias» Финляндия и др.)
При соблюдении аглютеновой диеты масса тела больных начинает восстанавливаться через 3 недели. Гистологические изменения в кишечнике начинают исчезать спустя 2-2,5 года. Одновременно с назначением аглютеновой диеты проводят симптоматическую терапию: витамины, препараты кальция, железа, ферментные препараты, пробиотики, массаж, гимнастика и др. Дети, страдающие целиакией, должны находиться на диспансерном наблюдении. Прогноз при соблюдении диеты и правильном лечении благоприятный. Следует учитывать, что крахмал, содержащий следы глютена, может быть компонентом многих пищевых продуктов и лекарственных средств. Поэтому при жёсткой диете необходим контроль и за отсутствием крахмала в составе оболочек таблеток, принимаемых для терапии тех или иных проблем.
|
||
|
Последнее изменение этой страницы: 2018-06-01; просмотров: 169. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |