Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
ПРОФИЛАКТИКА ПОСЛЕОПЕРАЦИОННЫХ ТРОМБОЭМБОЛИЧЕСКИХ ОСЛОЖНЕНИЙПрофилактика ТГВ и ТЭЛА производится в зависимости от риска развития этой патологии немедикаментозными, методами и путем назначения антикоагулянтной терапии. НЕСПЕЦИФИЧЕКИЕ МЕРОПРИЯТИЯ Для предотвращения послеоперационного венозного тромбоза предложены физические (механические) методы. К ним относят различные способы ускорения венозного кровотока, что препятствует одному из важнейших факторов в генезе тромбообразования: застою крови в венах нижних конечностей. Венозный застой предотвращают ранняя активизация пациентов в послеоперационном периоде; Одной из самых технически простых, и эффективных мер является статическая эластическая компрессия нижних конечностей (бинтование эластичным бинтом), приводящая к увеличению кровотока в глубоких венах ног. Проще в использовании и эффективнее специальные чулки дозированной компрессии, самостоятельно обеспечивающие необходимый градиент давления. Их применение позволяет снизить частоту развития ТГВ в 2 раза. Прекращать эластическую компрессию нижних конечностей следует после выздоровления больного. Важную роль играет лечебная физическая культура (ЛФК), которую также применяют у всех без исключения больных. Пациенты с сохраненным Определенный эффект может дать возвышенное положение голеней в постели (чтобы угол сгибания в коленных и тазобедренных суставах составлял 20-30°). Возможно применение перемежающейся пневматической компрессии голеней и интраоперационной электромиостимуляции с помощью специальной аппаратуры. Среди мероприятий неспецифической профилактики наряду с ранней активизацией больного большое значение имеют скорейшая нормализация показателей гемодинамики, адекватная анестезия при всех манипуляциях, предупреждение инфекционных осложнений. 
ФАРМАКОЛОГИЧЕСКИЕ СРЕДСТВА ПРОФИЛАКТИКИ Фармакологические средства, используемые с целью профилактики тромбоза глубоких вен, представлены: - низкомолекулярными декстранами (реополиглюкин, реомакродекс); - дезагреганатами (аспирин); - нефракционированным гепарином (НФГ); - низкомолекулярными гепаринами (НМГ): эноксапарин, надропарин и др. - непрямыми антикоагулянтами (варфарин и др.) Алгоритм профилактики венозных тромбоэмболических осложнений
Примечание: * - указанные мероприятия следует проводить всем без исключения пациентам Профилактические мероприятия необходимо начинать до операции в связи с тем, что в 50% случаев ТГВ начинает формироваться на операционном столе. Первая доза НФГ вводится за 2 часа до начала хирургического вмешательств В случаях опасности значительного интраоперационного кровотечения, гепаринотерапия может быть начата после завершения хирургического вмешательства, но не позже чем через 12 часов.. Профилактически антикоагулянтную терапию после операции следует проводить в течение не менее 7-10 дней.
Литература 1. Баешко А.А., Радюкевич А.А. Профилактика тромбэмболии легочной артерии.- Хирургия.- 2004.- №12.- С. 67-74. 2. Бокарев И.Н., Попова Л.В., Кондратьева Т.Б. Венозный тромбэмболизм.- Consilium medicum.-2005 г., приложение №1.- С.5-12. 3. Копенкин С.С. Профилактика венозных тромбэмболических осложнений в травматологии и ортопедии.- Consilium medicum.-2005 г., приложение №1.- С.15-20. 4. Отраслевой стандарт "Протокол ведения больных: профилактика ТЭЛА при хирургических и иных инвазивных вмешательствах", утвержден МЗ РФ 9 июня 2003 г. - Проблемы стандартизации в здравоохранении. – 2003.- №7. - С. 63-88. 5. Buller H.R. Antithrombotic Therapy for Venous Thromboembolic Disease. The Seventh ACCP Conference. CHEST 126/3 September 2004; Supplement.- р. 401-428. 6. Goldhaber S.Z. Echocardiography in the Management of pulmonary embolism. Ann. Intern. Med.-2002.- № 136.- p. 691-700. 7.Bates S.M., et al Conference on Antithrombotic and Thrombolytic Therapy Use of Antithrombotic Agents During Pregnancy: The Seventh ACCP // Chest – 2004. – Vol. 126. – P.627-644 8.Guidelines on diagnosis and management of acute pulmonary embolism. Task Force on Pulmonary Embolism, European Society of Cardiology. European Heart Journal (2000) 21, 1301–1336 9.Guidelines of British Society for Hematology. The diagnosis of deep vein thrombosis in symptomatic outpatients and the potential for clinical assessment and D-dimer assays to reduce the need for diagnostic imaging. British Journal of Hematology. 2004 Vol. 124., P. 15–25 10.Scottish Intercollegiate Guidelines Network (SIGN). Prophylaxis of Venous 11.Guidelines for the prevention and treatment of thromboembolic disease. Evidence-based report by the Italian College of Phlebology. International Angiology vol. 20 - suppl.2 to issue 2 - JUNE 2001 12.Hyers TM, Agnelli G, Hull RD, et al. Antithrombotic therapy for venous thromboembolic disease. Chest 2001;119:176S-193S. 13.V. Silva Vilela et al. Prevention of Thrombosis during Pregnancy. IMAJ . Vol 4. October 2002. 14.Clinical policy: Critical issues in the evaluation and management of adult patients presenting with suspected pulmonary embolism. Annals of Emergency Medicine. Volume 41., Number 2., February 2003
ОСТРАЯ КРОВОПОТЕРЯ Кровопотеря – это распространенное и эволюционно самое древнее повреждение организма человека, возникающее в ответ на потерю крови из сосудов и характеризующееся развитием ряда компенсаторных и патологических реакций. Состояние организма, возникающее вслед за кровотечением зависит от развития этих приспособительных и патологических реакций, соотношение которых определяется объемом потерянной крови. Повышенный интерес к проблеме кровопотери обусловлен тем, что практически все специалисты хирургического профиля встречаются с ней достаточно часто. Кроме того, показатели летальности при кровопотере до настоящего времени остаются высокими.Кровопотеря более 30% объема циркулирующей крови (ОЦК) менее чем за 2 часа считается массивной и опасной для жизни. Тяжесть течения кровопотери определяется ее видом, быстротой развития, объемом потерянной крови, степенью гиповолемии и возможным развитием шока, что наиболее убедительно представлено в классификации П.Г. Брюсова (1998), (табл.1).
Таблица 1. Классификация кровопотери
За рубежом наиболее широкое распространение нашла классификация кровопотери, предложенная Американской коллегией хирургов в 1982 году, согласно которой выделяют 4 класса кровотечений (табл.2)
Таблица 2. Классификация кровопотери Американской Коллегии хирургов
Острая кровопотеря приводит к выбросу надпочечниками катехоламинов, вызывающих спазм периферических сосудов и соответственно уменьшение объема сосудистого русла, что частично компенсирует возникший дефицит ОЦК. Перераспределение органного кровотока (централизация кровообращения) позволяет временно сохранить кровоток в жизненно важных органах и обеспечить поддержание жизни при критических состояниях. Однако впоследствии этот компенсаторный механизм может стать причиной развития тяжелых осложнений острой кровопотери. Критическое состояние называемое , шоком неизбежно развивается при потере 30% ОЦК, а так .называемый. «порог смерти» определяется не объемом кровотечения, а количеством эритроцитов, оставшихся в циркуляции. Для эритроцитов этот резерв составляет 30% глобулярного объема (ГО), для плазмы только 70%. Иначе говоря, организм может выжить при потере 2/3 циркулирующих эритроцитов, но не перенесет потерю 1/3 плазменного объема. Это обусловлено особенностями компенсаторных механизмов, развивающихся в ответ на кровопотерю и клинически проявляющихся гиповолемическим шоком. Под шоком понимают синдром, в основе которого лежит неадекватная капиллярная перфузия со сниженной оксигенацией и нарушенным потреблением кислорода органами и тканями. В основе его (шока) лежит периферический циркуляторно-метаболический синдром. Шок является следствием значительного уменьшения ОЦК (т.е. отношения ОЦК к емкости сосудистого русла) и ухудшения насосной функции сердца, которые могут манифестировать при гиповолемии любого генеза (сепсисе, травмах, ожогах, и т.д.). Конкретной причиной гиповолемического шока вследствие потери цельной крови может быть: - желудочно-кишечные кровотечения; - внутригрудные кровотечения; - внутрибрюшные кровотечения; - маточные кровотечения; - кровотечение в забрюшинное пространство; - разрывы аневризм аорты; - травмы и др. Патогенез Потеря ОЦК нарушает производительность сердечной мышцы, которая определяется: -минутным объемом сердца (МОС): МОС=УОС х ЧСС, (УОС – ударный объем сердца, ЧСС – частота сердечных сокращений) -давлением наполнения полостей сердца (преднагрузка); -функцией сердечных клапанов; -общим периферическим сосудистым сопротивлением (ОПСС) – постнагрузка. При недостаточной, сократительной способности сердечной мышцы в полостях сердца после каждого сокращения остается часть крови, и это ведет к увеличению преднагрузки. Часть крови застаивается в сердце, что называется сердечной недостаточностью. При острой кровопотере приводящей к развитию дефицита ОЦК, давление наполнения в полостях сердца первоначально уменьшается, вследствие чего снижаются УОС, МОС и АД. Поскольку уровень АД в значительной степени определяется минутным объемом сердца (МОС) и общим периферическим сосудистым сопротивлением (ОПСС), то для поддержания его на должном уровне при снижении ОЦК включаются компенсаторные механизмы, направленные на увеличение ЧСС и ОПСС. К компенсаторным изменениям, возникающим в ответ на острую кровопотерю, относят нейроэндокринные сдвиги, нарушения метаболизма, изменения со стороны сердечно-сосудистой и дыхательной систем. Активация всех звеньев свертывания обуславливает возможность развития диссеминированного внутрисосудистого свертывания крови (ДВС синдрома). В порядке физиологической защиты на свое самое частое повреждение организм отвечает гемодилюцией, улучшающей текучесть крови и снижающей ее вязкость, мобилизацией из депо эритроцитов, резким снижением потребности как в ОЦК, так и в доставке кислорода, увеличением частоты дыхания, сердечного выброса, отдачи и утилизации кислорода в тканях. Нейроэндокринные сдвиги реализуютсяактивацией симпатоадреналовой системы в виде повышенного выброса катехоламинов (адреналин, норадреналин) мозговым слоем надпочечников. Катехоламины взаимодействуют с α– и β – адренорецепторами. Стимуляция адренорецепторов периферических сосудов обуславливает вазоконстрикцию . Стимуляция β1 –адренорецепторов, локализующихся в миокарде, оказывает положительный ионотропный и хронотропный эффекты, стимуляция β2 -адренорецепторов, расположенных в кровеносных сосудах, вызывает легкую дилатацию артериол и констрикцию вен. Выброс катехоламинов при шоке приводит не только к уменьшению емкости сосудистого русла, но и перераспределению внутрисосудистой жидкости из периферических сосудов в центральные, что способствует поддержанию АД. Активируется система гипоталамус – гипофиз надпочечники, в кровь выбрасываются адренокортикотопный и антидиуретический гормоны, кортизол, альдостерон, следствием чего является увеличение осмотического давления плазмы крови, приводящее к усиление реабсорбции натрия и воды, уменьшению диуреза и увеличению объема внутрисосудистой жидкости. Нарушения метаболизма. Развившиеся нарушения кровотока и гипоксемия приводят к накоплению молочной и пировиноградной кислот. При недостатке или отсутствии кислорода пировиноградная кислота восстанавливается до молочной (анаэробный гликолиз), накопление которой ведет к метаболическому ацидозу. Аминокислоты и свободные жирные кислоты, также накапливаются в тканях и усугубляют ацидоз. Недостаток кислорода и ацидоз нарушают проницаемость клеточных мембран, в результате чего калий выходит из клетки, а натрий и вода поступают в клетки, обуславливая их набухание. Изменения со стороны сердечно-сосудистой и дыхательной системпри шоке весьма значительны. Выброс катехоламинов на ранних стадиях шока увеличивает ОПСС, сократимость миокарда и ЧСС - цель централизация кровообращения. Однако, возникшая тахикардия очень скоро уменьшает время диастолического наполнения желудочков и, следовательно, коронарный кровоток. Клетки миокарда начинают страдать от ацидоза. В случае затянувшегося шока респираторные механизмы компенсации оказываются несостоятельными. Гипоксия и ацидоз приводят к повышению возбудимости кардиомиоцитов, аритмиям. Гуморальные сдвиги проявляются высвобождением и других, кроме катехоламинов, медиаторов (гистамин, серотонин, простагландины, оксид азота, туморнекротизирующий фактор, интерлейкины, лейкотриены), которые обуславливают вазодилатацию и увеличение проницаемости сосудистой стенки с последующим выходом жидкой части крови в интерстициальное пространство и снижением перфузионного давления. Это усугубляет нехватку О2 в тканях организма, вызванную уменьшением его доставки вследствие микротромбообразования и острой потери переносчиков О2 - эритроцитов. В микроциркуляторном русле развиваются изменения носящие фазовый характер. 1 фаза – ишемической аноксии или сокращения пре- и посткапиллярных сфинктеров 2 фаза – капиллярного стаза или расширения прекапиллярных венул 3 фаза – паралича периферических сосудов или расширения пре- и посткапиллярных сфинктеров.. Кризисные процессы в капилляроне снижают доставку кислорода к тканям. Баланс между доставкой кислорода и потребностью в нем сохраняется до тех пор, пока обеспечивается необходимая тканевая экстракция кислорода. При промедлении с началом проведения интенсивной терапии нарушается доставка кислорода к кардиомиоцитам, нарастает ацидоз миокарда, который клинически проявляется гипотензией, тахикардией, одышкой. Снижение тканевой перфузии перерастает в глобальную ишемию с последующим реперфузионным повреждением тканей из-за повышенной выработки макрофагами цитокинов активацией перекисного окисления липидов, высвобождением нейтрофилами оксидов и дальнейшими нарушениями микроциркуляции. Последующее микротромбообразование формирует нарушение специфических функций органов и возникает риск развития полиорганной недостаточности. Ишемия изменяет проницаемость слизистой кишечника, особенно чувствительной к ишемически-реперфузионно-медиаторному воздействию, что обусловливает дислокацию бактерий и цитокинов в систему циркуляции и возникновение таких системных процессов, как сепсис, респираторный дистресс – синдром, полиорганная недостаточность. Их появление соответствует определенному временному интервалу или стадии шока, которая может быть начальной, обратимой (стадия обратимого шока) и необратимой. В значительной степени необратимость шока определяется количеством микротромбов образовавшихся в капиляроне и временным фактором кризиса микроциркуляции. Что же касается дислокации бактерий и токсинов вследствие ишемии кишечника и нарушения проницаемости его стенки то данное положение на сегодняшний день не является таким однозначным и требует дополнительных исследований. И все же шок можно определить как состояние при котором потребление кислорода тканями неадекватно их потребностям для функционирования аэробного метаболизма.
Клиника и диагностика Клиническая картина. При развитии геморрагического шока выделяют 3 стадии. • Компенсированный обратимый шок. Объём кровопотери не превышает 25% (700-1300 мл). Тахикардия умеренная, АД либо не изменено, либо незначительно понижено. Запустевают подкожные вены, снижается ЦВД. Возникают признаки периферической вазоконстрикции: похолодание конечностей. Количество выделяемой мочи снижается наполовину (при норме 1-1,2 мл/мин). • Декомпенсированный обратимый шок. Объём кровопотери составляет 25-45% (1300-1800 мл). Частота пульса достигает 120-140 в мин. Систолическое АД снижается ниже 100 мм.рт.ст., уменьшается величина пульсового давления. Возникает выраженная одышка, отчасти компенсирующая метаболический ацидоз путём дыхательного алкалоза, но способная быть также признаком шокового лёгкого. Усиливаются похолодание конечностей, акроцианоз. Появляется холодный пот. Скорость выделения мочи - ниже 20 мл/ч. • Необратимый геморрагический шок. Его возникновение зависит от длительности декомпенсации кровообращения (обычно при артериальной гипотензии свыше 12 ч). Объём кровопотери превышает 50% (2000-2500 мл). Пульс превышает 140 в мин, систолическое АД падает ниже 60 мм.рт.ст. или не определяется. Сознание отсутствует. Развивается олигоанурия. ДИАГНОСТИКА Диагностика основана на оценке клинических и лабораторных признаков. В условиях острой кровопотери чрезвычайно важно определить ее объем, для чего необходимо воспользоваться одним из существующих методов, которые подразделяют на три группы: клинические, эмпирические и лабораторные.. Клинические методы позволяют оценить объем кровопотери на основании клинических симптомов и гемодинамических показателей. Уровень АД и частота пульса до начала возместительной терапии в значительной степени отражают величину дефицита ОЦК. Отношение частоты пульса к систолическому АД позволяет рассчитать шоковый индекс Альговера. Величина его в зависимости от дефицита ОЦК представлена в таблице 3.
Таблица 3. Оценка на основании шокового индекса Альговера
Тест наполняемости капилляров, или симптом «белого пятна» позволяет оценить капиллярную перфузию. Его проводят путем нажатия на ноготь пальца, кожу лба или мочку уха. В норме цвет восстанавливается через 2 с, при положительной пробе – через 3 и более секунд. Центральное венозное давление (ЦВД) – показатель давления наполнения правого желудочка, отражает его насосную функцию.. В норме ЦВД колеблется от 6 до 12 см водного столба. Снижение ЦВД свидетельствует о гиповолемии. При дефиците ОЦК в 1 л ЦВД уменьшается на 7 см.вод.ст. Зависимость величины ЦВД от дефицита ОЦК представлена в таблице 4.
Таблица 4. оценка дефицита объема циркулирующей крови на основании величины центрального венозного давления
Почасовой диурез отражает уровень тканевой перфузии или степень наполнения сосудистого русла. В норме за час выделяется 0,5-1 мл/кг мочи. Снижение диуреза менее 0,5 мл/кг/ч свидетельствует о недостаточном кровоснабжении почек вследствие дефицита ОЦК. Эмпирические методы оценки объема кровопотери наиболее часто применяются при травмах и политравмах. В них используют средне-статистические значения кровопотери, установленные для того или иного вида повреждения. Таким же образом можно оценить ориентировочно кровопотерю при различных оперативных вмешательствах.
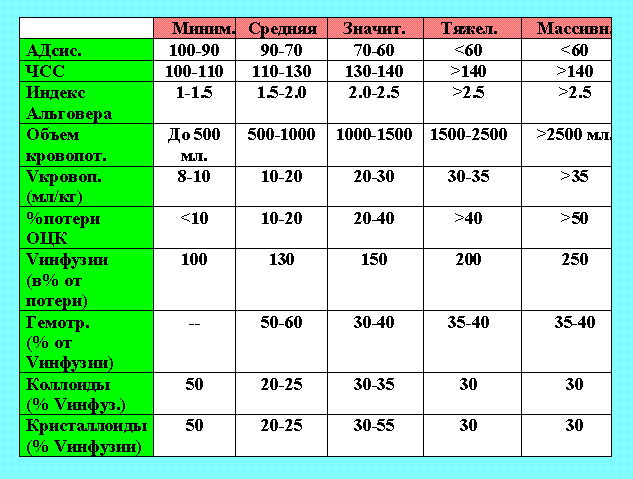
Средняя кровопотеря (л) -Гемоторакс – 1,5-2,0 -Перелом одного ребра – 0,2-0,3 -Травма живота – до 2,0 -Перелом костей таза (забрюшинная гематома) – 2,0-4,0 -Перелом бедра – 1,0-1,5 -Перелом плеча/голени – 0,5-1,0 -Перелом костей предплечья – 0,2-0,5 -Переломом позвоночника – 0,5-1,5 -Скальпированная рана размером с ладонь – 0,5 Операционная кровопотеря -Лапаротомия – 0,5-1,0 -Торакотомия – 0,7-1,0 -Ампутация голени – 0,7-1,0 -Остеосинтез крупных костей – 0,5-1,0 -Резекция желудка – 0,4-0,8 -Гастрэктомия – 0,8-1,4 -Резекция толстой кишки – 0,8-1,5 -Кесарево сечение – 0,5-0,6 Лабораторные методы предусматривают определение гематокритного числа (Ht), концентрации гемоглобина (Hb), относительной плотности (р) или вязкости крови. Они подразделяются на: -расчетные (применение математических формул); -аппаратные (электрофизиологические импедансометрические методы); -индикаторные (применение красителей, термодилюции, декстранов, радиоизотопов). Среди расчетных методов наибольшее распространение получила формула Moore: КВП=ОЦКд х Htд-Htф / Htд Где КВП – кровопотеря (мл); ОЦКд – должный объем циркулирующей крови (мл). В норме у женщин ОЦКд в среднем составляет 60 мл/кг, у мужчин – 70 мл/кг, у беременных женщин – 75 мл/кг; Htд – должный гематокрит (у женщин – 42%, у мужчин – 45%); Htф – фактический гематокрит больного. В этой формуле вместо гематокрита можно использовать показатель гемоглобина, принимая за его должный уровень 150 г/л. Можно также использовать величину плотности крови, однако эта методика применима только при небольших кровопотерях. Одним из первых аппаратных методов определения ОЦК был метод, в основу которого положено измерение базисного сопротивления тела с помощью реоплетизмографа (нашел применение в странах «постсоветского пространства»). Современные индикаторные методы предусматривают установление ОЦК по изменению концентрации применяемых веществ и условно подразделяются на несколько групп: 1.определение объема плазмы, а затем всего объема крови через Ht; 2.определение объема эритроцитов и по нему всего объема крови через Ht; 3.одновременное определение объема эритроцитов и плазмы крови. В качестве индикатора используют краску Эванса (Т-1824), декстраны (полиглюкин), человеческий альбумин, меченный йодом (131) или хлоридом хрома (51CrCl3). Однако, к сожалению, все методы определения кровопотери дают очень высокую погрешность (иногда до литра), а поэтому могут служить лишь ориентиром при проведении лечения. Тем не менее определение VO2 следует считать наиболее простым диагностическим критерием выявления шока. ЛЕЧЕНИЕ Стратегическим принципом трансфузионной терапииострой кровопотери, является восстановление органного кровотока (перфузии) путем достижения необходимого ОЦК. Поддержание уровня факторов свертывания в количествах, достаточных для гемостаза, с одной стороны, и для противостояния избыточному диссеминированному свертыванию – с другой. Восполнение количества циркулирующих эритроцитов (переносчиков кислорода) до уровня, обеспечивающего минимальное достаточное потребление кислорода в тканях.. Однако большинство специалистов считает наиболее острой проблемой кровопотери гиповолемию, и соответственно на первое место в схемах терапии ставят восполнение ОЦК, который является критическим фактором для поддержания стабильной гемодинамики. Патогенетическая роль снижения ОЦК в развитии тяжелых нарушений гомеостаза предопределяет значение своевременной и адекватной коррекции волемических нарушений на исходы лечения у больных с острой массивной кровопотерей Конечной целью всех усилий реаниматолога является сохранение адекватного потребления кислорода тканями для поддержания метаболизма. Общие принципы лечения острой кровопотери сводятся к следующему: 1.Остановка кровотечения, борьба с болью. 2.Обеспечение адекватного газообмена. 3.Восполнение дефицита ОЦК. 4.Лечение органной дисфункции и профилактика полиорганной несостоятельности: · лечение сердечной недостаточности; · профилактика почечной недостаточности; · коррекция метаболического ацидоза; · стабилизация обменных процессов в клетке; · лечение и профилактика ДВС-синдрома. 5.Ранняя профилактика инфекции. Остановка кровотечения и борьба с болью. При любом кровотечении важно как можно скорее устранить его источник. При наружном кровотечении – прижатие сосуда, давящая повязка, жгут, лигатура или зажим на кровоточащий сосуд. При внутреннем кровотечении – срочное оперативное вмешательство, проводимое параллельно с лечебными мероприятиями по выведению больного из шока. В табл.№5 представлены данные по характеру проведения инфузионной терапии, острой кровопотери.
1. Инфузия начинается с кристаллоидов, затем - коллоиды. Гемотрансфузия - при снижении Hb менее 70 г/л, Ht менее 25%. 2. Скорость инфузии при массивной кровопотере до 500 мл/мин!!! (катетеризация второй центральной вены, инфузия растворов под давлением). 3. -Коррекция волемии (стабилизация гемодинамических показателей). 4. Нормализация глобулярного объема (Hb, Ht). 5. Коррекция нарушений водно-солевого обмена
Борьба с болевым синдромом, защита от психического стресса осуществляется путем внутривенного (в/в) введения анальгетиков: 1-2 мл 1% раствора морфина гидрохлорида, 1-2 мл 1-2% раствора промедола, а также натрия оксибутирата (20-40 мг/кг массы тела), сибазона (5-10 мг), возможно использование субнаркотических доз калипсола и седация с помощью пропофола . Доза наркотических анальгетиков должна быть снижена на 50% из-за возможного угнетения дыхания, тошноты и рвоты, возникающих при внутривенном введении этих препаратов. Кроме того, следует помнить, что введение их возможно только после исключения повреждения внутренних органов. Обеспечение адекватного газообмена направлено как на утилизацию кислорода тканями, так и на удаление углекислого газа. Всем больным показано профилактическое введение кислорода через носовой катетер со скоростью не менее 4 л/мин. При возникновении дыхательной недостаточности основными задачами лечения являются: 1.обеспечение проходимости дыхательных путей; 2.профилактика аспирации содержимого желудка; 3.освобождение дыхательных путей от мокроты; 4.вентиляция легких; 5 восстановление оксигенации тканей.
Развившаяся гипоксемия может быть обусловлена: 1.гиповентиляцией (обычно в сочетании с гиперкапнией); 2.несоответствием между вентиляцией легких и их перфузией (исчезает при дыхании чистым кислородом); 3.внутрилегочным шунтированием крови (охраняется при дыхании чистым кислородом), вызванным респираторным дистресс-синдромом взрослых (РаО2 < 60-70 мм.рт.ст. FiО2 > 50%, двусторонние легочные инфильтраты, нормальное давление наполнения желудочков), отеком легких, тяжелой пневмонией; 4.нарушением диффузии газов через альвеоло – капиллярную мембрану (исчезает при дыхании чистым кислородом). Вентиляция легких осуществляемая после интубации трахеи проводится в специально подобранных режимах создающих условия оптимального газообмена и не нарушающих центральную гемодинамику. Восполнение дефицита ОЦК. Прежде всего, при острой кровопотере больному следует создать улучшенное положение Тренделебурга для увеличения венозного возврата. Инфузию проводят одновременно в 2-3 периферических или 1-2 центральных вены. Темп восполнения кровопотери определяется величиной АД. Как правило, вначале инфузию проводят струйно или быстро капельно (до 250-300 мл/мин). После стабилизации АД на безопасном уровне инфузию проводят капельно. Инфузионную терапию начинают с введения кристаллоидов. А в последнее десятилетие наблюдается возврат к рассмотрению возможности применения гипертонических растворов NaCI/
Гипертонические растворы натрия хлорида (2,5-7,5%), благодаря высокому осмотическому градиенту, обеспечивают быструю мобилизацию жидкости из интерстиция в кровеносное русло. Однако небольшая продолжительность их действия (1-2 ч) и относительно малые объемы введения (не более 4 мл/кг массы тела) обусловливают преимущественное применение их на догоспитальном этапе лечения острой кровопотери. Коллоидные растворы противошокового действия подразделяют на природные (альбумин, плазма) и искусственные (декстраны, гидроксиэтилкрахмалы). Альбумин и белковая фракция плазмы эффективно увеличивают объем внутрисосудистой жидкости, т.к.имеют высокое онкотическое давление. Однако они легко проникают через стенки легочных капилляров и базальные мембраны клубочков почек во внеклеточное пространство, что может привести к отеку интерстициальной ткани легких (респираторный дистресс-синдром взрослых) или почек (острая почечная недостаточность). Объем диффузии декстранов ограничен, т.к. они вызывают повреждение эпителия почечных канальцев («декстрановая почка»), неблагоприятно влияют на систему свертывания крови и иммунокомпонентные клетки. Поэтому сегодня «препаратами первого выбора» являются растворы гидроксиэтилкрахмала. Гидроксиэтилкрахмал – природный полисахарид, получаемый из амилопектинового крахмала и состоящий из высокомолекулярных поляризованных остатков глюкозы. Исходным сырьем для получения ГЭК служат крахмал из клубней картофеля и тапиока, зерна различных сортов кукурузы, пшеницы, риса. ГЭК из картофеля и кукурузы, наряду с линейными цепями амилазы, содержит фракцию разветвленного амилопектина. Гидроксилирование крахмала препятствует его быстрому ферментативному расщеплению, увеличивает способность удерживать воду и повышать коллоидно-осмотическое давление. В трансфузионной терапии используют 3%, 6% и 10% растворы ГЭК. Введение растворов ГЭК вызывает изоволемическое (до 100% при ведении 6% раствора) или даже первоначально гиперволемическое (до 145% от введенного объема 10% раствора препарата) объемозамещающее действие, которое сохраняется не менее 4 часов. Помимо этого растворы ГЭК обладают следующими свойствами, отсутствующими у других коллоидных плазмозаменяющих препаратов: -предотвращают развитие синдрома повышенной проницаемости капилляров, закрывая поры в их стенках; -модулируют действие циркулирующих адгезивных молекул или медиаторов воспаления, которые, циркулируя в крови при критических состояниях, увеличивают вторичные повреждения тканей, связываясь с нейтрофилами или эндотелиоцитами; -не влияют на экспрессию поверхностных антигенов крови, т.е. не нарушают иммунные реакции; -не вызывают активации системы комплемента (состоит из 9 сывороточных белков С1 – С9), связанной с генерализованными воспалительными процессами, которые нарушают функции многих внутренних органов. Следует отметить, что в последние годы появились отдельные рандомизированные исследования высокого уровня доказательности (А,Б) свидетельствую щие о способности крахмалов вызывать нарушения функции почек и отдающие предпочтение альбумину и даже препаратам желатина. Вместе с тем, с конца 70-х годов ХХ столетия начали активно изучаться перфторуглеродные соединения (ПФОС), положенные в основу нового поколения плазмозаменителей с функцией переноса О2, одним из которых является перфторан. Применение последнего при острой кровопотере позволяет влиять на резервы трех уровней обмена О2, а одновременное применение оксигенотерапии позволяет повысить и резервы вентиляции. Мы рекомендуем использовать препарат, начиная со II уровня кровезамещения, исходя из схемы, представленной ниже.
Табл. 6. доля применения перфторана в зависимости от уровня кровезамещения.
Клинически степень уменьшения гиповолемии отражают следующие признаки: -повышение артериального давления; -уменьшение частоты сердечных сокращений; -потепление и порозовение кожных покровов; -увеличение пульсового давления; -диурез свыше 0,5 мл/кг/ч.
Таким образом, суммируя вышеизложенное, подчеркнем, что показаниями для гемотрансфузии являются: -кровопотеря более20% должного ОЦК, -анемия, при которой содержание гемоглобина менее 75 г/л, а гематокритное число менее 0,25. Лечение органной дисфункции и профилактика полиорганной недостаточности. Одной из наиболее важных задач является лечение сердечной недостаточности. Если пострадавший до несчастного случая был здоров, то для нормализации сердечной деятельности обычно достаточно быстро и эффективно восполнит дефицит ОЦК. Если же в анамнезе у пострадавшего есть хронические заболевания сердца или сосудов, то гиповолемия и гипоксия усугубляет течение основного заболевания, поэтому проводят специальное лечение. Прежде всего, необходимо добиться повышения преднагрузки, что достигается увеличением ОЦК, а затем усилить сократимость миокарда. Чаще всего вазоактивные и инотропные средства не назначают, но если гипотензия приобретает стойкий характер, не поддающийся инфузионной терапии, то эти препараты могут быть применены. Причем применение их возможно только после полного возмещения ОЦК. Из вазоактивных средств препаратом первого ряда для поддержания деятельности сердца и почек является дофамин, 400 мг которого разводят в 250 мл изотонического раствора. Скорость инфузии выбирают в зависимости от желаемого эффекта: 2-5 мкг/кг/мин («почечная» доза) расширяет мезентериальные и почечные сосуды без увеличения частоты сердечных сокращений и АД; 5-10 мкг/кг/мин дает выраженный ионотропный эффект, мягкую вазодилатацию вследствие стимуляции β2 – адренорецепторов либо умеренную тахикардию; - 10-20 мкг/кг/мин приводит к дальнейшему усилению ионотропного эффекта, выраженной тахикардии; Более 20 мкг/кг/мин – резкая тахикардия с угрозой тахиаритмий, сужение вен и артерий вследствие стимуляции α1_ адренорецепторов и ухудшение перфузии тканей. Вследствие артериальной гипотензии и шока, как правило, развивается острая почечная недостаточность (ОПН). Для того чтобы предупредить развитие олигурической формы ОПН, необходимо осуществлять контроль почасового диуреза (в норме у взрослых составляет 0,5-1 мл/кг/ч, у детей – более 1 мл/кг/ч) Измерение концентрации натрия и креатина в моче и плазме (при ОПН креатин плазмы крови превышает 150 мкмоль/л, скорость клубочковой фильтрации – ниже 30 мл/мин); Инфузию дофамина в «почечной» дозе; В настоящее время в литературе нет рандомизированных многоцентровых исследований свидетельствующих об эффективности применения «почечных доз» симпатомиметиков. Стимуляцию диуреза на фоне восстановления ОЦК (ЦВД более 30-40см.водн.ст.) и удовлетворительного сердечного выброса (фуросемид, в/в в первоначальной дозе 40 мг с увеличением при необходимости в 5-6 раз). Нормализацию гемодинамики и возмещения объема циркулирующей крови (ОЦК) следует проводить под контролем ДЗЛК (давление заклинивания легочных капилляров), СВ (сердечный выброс) и ОПСС. При шоке два первых показателя прогрессивно снижаются а последний повышается. Методики определения этих критериев и их нормы достаточно хорошо описаны в литературе, но к сожалению рутинно используются в клиниках зарубежья и редко в нашей стране.. Шок, как правило, сопровождается тяжелым метаболическим ацидозом. Под его влиянием снижается сократимость миокарда, уменьшается сердечный выброс, что способствует дальнейшему снижению АД. Реакции сердца и периферических сосудов на эндо- и экзогенные катехоламины снижаются. Ингаляция О2 , ИВЛ, инфузионная терапия восстанавливают физиологические компенсаторные механизмы и в большей части случаев устраняют ацидоз. Натрия бикарбонат вводят при тяжелом метаболическом ацидозе (рН венозной крови ниже 7,25), рассчитав его по общепринятой формуле, после определения показателей КЩС. Болюсно можно сразу ввести 44-88 мэкв (50-100 мл 7,5% НСО3), остальное количество в течение последующих 4-36 часов. Следует помнить, что излишнее введение натрия бикарбоната создает предпосылки для развития метаболического алкалоза, гипокалиемии, аритмий. Возможно резкое увеличение осмолярности плазмы, вплоть до развития гиперосмолярной комы. При шоке, сопровождающемся критическим ухудшением гемодинамики, необходима стабилизация обменных процессов в клетке. Лечение и профилактику ДВС-синдрома, как и раннюю профилактику инфекций, проводят, руководствуясь общепринятыми схемами. Обоснованным, с нашей точки зрения, является патофизиологический подход к решению проблемы показаний к гемотрансфузиям, основывающийся на оценке транспорта и потребления кислорода. Транспорт кислорода является производным сердечного выброса и кислородной емкости крови. Потребление кислорода зависит от доставки и способности ткани забирать кислород из крови. При восполнении гиповолемии, коллоидными и кристаллоидными растворами количество эритроцитов снижено и кислородная емкость крови уменьшена. За счет активации симпатической нервной системы компенсаторно повышается сердечный выброс (иногда превышая нормальные величины в 1.5-2 раза), "раскрывается" микроциркуляция и снижается сродство гемоглобина к кислороду, ткани забирают из крови относительно больше кислорода (увеличивается коэффициент экстракции кислорода). Это позволяет сохранять нормальное потребление кислорода при низкой кислородной емкости крови. Увеличение кислородной емкости крови переливанием консервированной крови и ее компонентов имеет свои отрицательные стороны. Во-первых, увеличение гематокрита ведет к увеличению вязкости крови и ухудшению микроциркуляции, создает дополнительную нагрузку на миокард. Во-вторых, низкое содержание 2,3-ДФГ в эритроцитах донорской крови сопровождается увеличением сродства кислорода к гемоглобину, смещением кривой диссоциации оксигемоглобина влево и, как результат, - ухудшению оксигенации тканей. В-третьих, в переливаемой крови всегда присутствуют микросгустки, которые могут "забивать" капилляры легких и резко увеличить легочный шунт, ухудшая оксигенацию крови. К тому же перелитые эритроциты начинают полноценно участвовать в транспорте кислорода лишь через 12-24 часа после гемотрансфузии. Проведенный нами анализ литературы показал, что выбор средств для коррекции кровопотери и постгеморрагической анемии не является решенным вопросом. Это связано, в основном, с отсутствием информативных критериев оценки оптимальности тех или иных способов компенсации транспорта и потребления кислорода. Современная тенденция к уменьшению переливаний крови обусловлена, в первую очередь, возможностью осложнений связанных с гемотрансфузиями, ограничением донорства, отказом пациентов от гемотрансфузии по каким-либо соображениям. В то же время, количество критических состояний связанных с кровопотерей различного генеза возрастает. Этот факт диктует необходимость дальнейшей разработки способов и средств заместительной терапии. Интегральным показателем, который позволяет объективно оценить адекватность тканевой оксигенации является насыщение гемоглобина кислородом в смешанной венозной крови (SvO2). Снижение этого показателя менее 60% в течении короткого периода времени ведет к появлению метаболических признаков тканевой кислородной задолженности (лактоацидоз и др.). Следовательно, увеличение содержания лактата в крови может быть биохимическим маркером степени активации анаэробного метаболизма и характеризовать эффективность проведенной терапии.
Литература
ШОК Шок - крайне тяжелое состояние, характеризующееся расстройствами центрального и периферического кровообращения с резким уменьшением кровоснабжения органов и тканей. В основе шока лежит нарушение газообмена между кровью и тканями с последующей гипоксией и расстройством обмена в клетках. В патогенетическом аспекте "шок" - специфический циркуляторно-метаболический синдром, во время которого нарушение микроциркуляции и последующее повреждение метаболизма клеток является ведущими звеньями в патогенезе, независимо от причин, вызвавших это нарушение. Шок-это состояние при котором потребление кислорода тканями не соответствует его поставке для поддержания аэробного метаболизма. Различают следующие виды шока: 1. Гиповолемический (геморрагический, травматический, ожоговый, дегидратический). 2. Токсико-инфекционный. 3. Анафилактический. 4. Кардиогенный. В основе всех видов шока лежит- нарушение соотношения между потребностью организма в кислороде и возможностью его доставки органам и тканям. При травмах, кровопотере, сепсисе и других критических состояниях увеличивается потребность миокарда в О2, а условия доставки его ухудшаются. ФИЗИОЛОГИМЯ КРОВООБРАЩЕНИЯ В клинико-физиологическом аспекте систему кровообращения целесообразно рассматривать состоящей из ряда функциональных отделов: 1. Сердечный насос - главный механизм циркуляции. 2. Сосуды-буферы или артерии (некоторые авторы называют их иначе - сосуды "котла", подразумевая под ними аорту и крупные артерии) - выполняют преимущественно пассивную транспортную функцию посредника между насосом и системой микроциркуляции. 3. Сосуды-емкости или вены, также выполняют транспортную функцию возврата крови к сердцу. Это более активная, чем артерии часть системы кровообращения, поскольку вены способны изменять свой объем в десятки раз, активно участвуя в регуляции венозного возврата и объема циркулирующей крови; 4. Сосуды-сопротивления - артериолы м венулы, включая сфинктеры, регулирующие кровоток через капилляры и являющиеся главным физиологическим средством распределения сердечного выброса по органам и тканям, в связи с чем их называют сосудами распределения; 5.Сосуды-обмена - капилляры, присоединяющие систему кровообращения к общему сокообращению организма; 6. Сосуды-шунты - артерио-венозные анастомозы, регулирующие периферическое сопротивление при спазме артериол прекапиллярного и посткапиллярного сфинктеров, сокращением кровотока через капилляры. Три первые функциональные части кровообращения (сердечный насос, сосуды-буферы и сосуды-емкости) образуют систему макроциркуляции - хорошо зримую и потому кажущуюся самой главной в кровообращении организма. Но на самом деле в клинико-физиологическом аспекте гораздо важнее знать о состоянии системы микроциркуляции, состоящей из трех последних разделов схемы (сосуды-сопротивления, сосуды обмена и шунты). Система микроциркуляции важнее для изучения патофизиологии кровообращения потому, что она поражается при критическом состоянии любой этиологии, тогда как система макроциркуляции - при первичной патологии самих органов кровообращения, а при критических состояниях она страдает вторично из-за поражения системы микроциркуляции. Главная функциональная цель системы макроциркуляции - обеспечить движение и транспорт крови. Задача микроциркуляции - присоединить систему кровообращения в общему сокообращению организма и распределить сердечный выброс между разными органами соответственно их потребности.
СЕРДЦЕ Ни один из известных механике насосов не работает так долго, как сердце. Этот маленький орган, весящий приблизительно 300 г, снабжает кровью "среднего человека" весом 70 кг в течение 70 лет. У человека в покое каждый желудочек сердца выбрасывает 5-5,5 л крови в минуту, таким образом за 70 лет производительность обоих желудочков составляет приблизительно 400 млн литров, даже если человек находиться в состоянии покоя. По существу сердце состоит из двух насосов - правого сердца (предсердие и желудочек) и левого сердца (предсердие и желудочек). Во время систолы левое сердце выбрасывает 70-80 мл крови за одно сокращение в аорту, а кровь, поступающая из полых вен, нагнетается правым желудочком в легочной круг. Во время тяжелой физической нагрузки сердце может нагнетать 25 л/мин и даже более в результате увеличения частоты и силы сокращений. Некоторые из этих изменений обусловлены нервными воздействиями на волокна сердечной мышцы, а некоторые являются простым физическим следствием воздействия "растягивающей силы" венозного возврата на диастолическое растяжение, таким образом, на сократительную силу волокон сердечной мышцы; каждый насос должен быть наполнен, чтобы он мог работать. Кровь в сердце поступает под давлением, лишь незначительно превышающем нулевой уровень, во время диастолы. Сокращение и связанное с ним смещение желудочков сердца вниз приводит к пассивному расширению предсердий и оказывают некоторое присасывающее действие на кровь в центральных венах, что увеличивает эффективность сил, обеспечивающих наполнение вен ("заправка насоса"). ОБЩАЯ ОРГАНИЗАЦИЯ СОСУДОВ Во время систолы внутрижелудочковое давление повышается от уровня близкого к нулю до 120 мм рт ст в левом желудочке и до 25 мм рт ст в правом. В результате этого систолическое давление в аорте повышается до 120 мм рт ст, а в легочной артерии до 25 мм рт ст. По окончании фазы сокращения миокард расслабляется и внутрижелудочковое давление круто падает почти до нуля, полулунные клапаны захлопываются, отделяя аорту и легочную артерию от желудочков. Благодаря эластичности больших артерий и сопротивлению току крови в периферических сосудах АД колеблется в значительно меньшей степени, чем давление в желудочках, в результате чего диастолическое давление составляет приблизительно 80 мм рт ст в системном сосудистом ложе (большом круге кровообращения). Поэтому фазовое изменение давления в левом желудочке - от 120 до 0 мм рт ст - превращается в артериальное пульсовое давление, равное (120 - 80) = 40 мм рт ст. В малом круге эти показатели равны приблизительно 25/10, так как пульсовое давление составляет 15 мм рт ст. Таким образом, оба желудочка соответственно обеспечивают энергией кровообращение в обоих кругах кровообращения, образуя градиент давления, который приводит в движение кровь. Аналогия с законом Ома дает возможность понять факторы, которые в этом участвуют: 1 = Е/Р (ом), где Е - градиент давления, приводящий в движение кровь, равен средней разнице между давлением в артериальном и венозном отделах каждого круга; Р - общее сопротивление, оказываемое сосудами системного и легочного круга, наибольшая часть которого приходится на долю артериол. Приток крови к каждому кругу (1) определяется частным от деления градиента давления на региональное сопротивление кровотоку. ДИФФЕРЕНЦИАЦИЯ СОСУДОВ СОСУДЫ-БУФЕРЫ. Они оказывают незначительное сопротивление току крови и поэтому смягчают пульсирующий систолический выброс желудочка. Выброс левого желудочка растягивает аорту и ее крупные ветви. После захлопывания аортальных клапанов эластичная аорта и ее ветви сокращаются, поддерживая этим градиент давления и делая поступление крови на периферию более равномерным. Старение эластических элементов артериальной стенки является причиной высокого пульсового давления в результате снижения функции сосудов-буферов. ПРЕКАПИЛЛЯРНЫЕ СОСУДЫ СОПРОТИВЛЕНИЯ. Это в основном мелкие артерии и артериолы, на долю которых приходится большая часть сопротивления кровотоку. Снабжение кровью любого участка, а также гидростатическое давление в капиллярах этого участка определяются главным образом изменениями радиуса этих сосудов. Прекапиллярным сосудам сопротивления свойственна высокая степень внутреннего (миогенного) базального тонуса, который постоянно изменяется под влиянием местных физических и химических факторов. Изменения базального миогенного тонуса в результате таких местных воздействий являются почти единственным механизмом приспособления регионарного сопротивления сосудов, снабжающих кровью сердце и головной мозг. В других местах сосуды сопротивления регионарных цепей находятся также под влиянием симпатических нервов. Влияние этой иннервации в состоянии равновесия в покое относительно незначительно, но при стрессовых обстоятельствах оно может стать выраженным. ПРЕКАПИЛЛЯРНЫЕ СФИНКТЕРЫ. Эти сосуды, хотя они и являются частью прекапиллярных сосудов сопротивления, определяют в основном площадь обменной поверхности капилляров, изменяя число капилляров, перфузируемых в каждый определенный момент. Они находятся главным образом под местным контролем, т.е. под контролем внутренней миогенной активности, непрерывно изменяющейся под влиянием местных сосудорасширяющих метаболитов. КАПИЛЛЯРНЫЕ ОБМЕННЫЕ СОСУДЫ Эти сосуды - ключевой пункт сердечно-сосудистой системы - представляют собой трубочки, состоящие из одного слоя эндотелиальных клеток. Растворенные вещества проходят через их стенку в обеих направлениях. Сами капилляры не оказывают активного влияния ни на скорость кровотока, ни на чрезвычайно важные обменные механизмы диффузии и фильтрации-абсорбции. ПОСТКАПИЛЛЯРНЫЕ СОСУДЫ СОПРОТИВЛЕНИЯ. Венулы и мелкие вены не играют большой роли в общем сопротивлении сосудов. Тем не менее они имеют большое значение, т.к.от соотношения между прекапиллярным и посткапиллярным давлением зависит гидростатическое давление в самих капиллярах, а от него в свою очередь зависит транспорт жидкой фазы между кровью и межтканевой жидкостью. Таким образом, изменения градиента пре- и посткапиллярного сопротивления оказывает влияние на ток крови, а изменения соотношения между пре- и посткапиллярным сопротивлением влияют на объем крови. СОСУДЫ-ЕМКОСТИ. Эти сосуды, т.е. все венозное ложе, играют незначительную роль в создании на емкость сосудистого русла изменением своей конфигурации и диаметра просвета. Минутный объем крови зависит от венозного возврата, в соответствии с этим изменения емкости сосудистого русла, вызываемые в основном активностью внешних сосудосуживающих симпатических волокон, могут оказывать глубокое влияние на наполнение сердечного насоса. Венозный отдел можно считать своего рода "форкамерой" насоса. СОСУДЫ-ШУНТЫ. В большинстве целей эти сосуды являются скорее исключением. Они осуществляют прямые связи между мелкими артериями и венами в обход капиллярного ложа. Поэтому они не выполняют обменной функции и локализуются в изобилии в участках кожи (пальцы рук, ног, уха и т.д.), выполняющих в основном терморегуляторную функцию. Их тонус находится в большой зависимости от влияния симпатических сосудосуживающих нервов. МАССООБМЕН В КАПИЛЛЯРОНЕ. Конечной функциональной ячейкой системы микроциркуляции является капиллярон, состоящий из артериолы, венулы, капилляров и артериовенозного анастомоза (шунта). Основные законы гемодинамики капиллярона можно сформулировать следующим образом: 1) регуляция кровотока через капилляры осуществляется в соответствии с местными потребностями путем изменения тонуса сосудов-сопротивлений; 2) анатомическое строение капиллярона соответствует общему назначению системы микроциркуляции, но детали структуры его приспособлены к функциональным задачам данного органа и специфичны именно для него; 3) реологические свойства крови и связанный с ними транскапиллярный массообмен зависит от скорости кровотока. Местной тканевой регуляцией кровоток может быть направлен через капилляры или через артериовенозные шунты. От такого распределения зависит собственный метаболизм органа, в котором расположен капиллярон. Сокращение артериол увеличивает общее периферическое сопротивление (ОПС) и ухудшает кровоток в капилляроне. Сокращение венул задерживает повышенный объем крови в нем. Существуют два биофизических механизма, регулирующих массообмен в капилляроне: изменение тонуса мышечных сосудов и изменение проницаемости капиллярной стенки. Регуляция мышечного тонуса осуществляется нейрогенным путем (быстрый процесс), а также через местные метаболиты и биологически активные вещества (медленный процесс). Регуляция массообмена через капиллярную стенку может быть описана уравнением Старлинга для полупроницаемых мембран: 1у = Кф х (/Рс - Рт/ - л /Пс - Пт), где 1у - объем жидкости, движущейся через капиллярную стенку; Кф - коэффициент фильтрации; Рс - внутрикапиллярное давление; Рт -интерстициальное давление; л - коэффициент отражения макромолекул; Пс - онкотическое давление крови; Пт -онкотическое давление интерстициальной жидкости. Условия критического состояния могут воздействовать на все эти параметры микроциркуляции многочисленными факторами. Например, гипоксия, респираторный и метаболический ацидоз могут влиять на них непосредственно или через определенные вещества. Нервные окончания альфа и бета-адренергических систем также могут стимулироваться естественными медиаторами или метаболитами и экзогенными веществами. Накопление кислых продуктов вызывает вазодилятацию с увеличением кровотока через капиллярон, благодаря чему ацидоз снижается, т.к. избыток кислых продуктов удаляется. РЕОЛОГИЧЕСКИЕ СВОЙСТВА КРОВИ. Кровь - суспензия клеток и частиц, взвешенный в коллоидах плазмы. Это типично неньютоновская жидкость, вязкость которой, в отличие от ньютоновской, в различных частях системы кровообращения различается в сотни раз, в зависимости от изменения скорости кровотока. Для вязкостных свойств крови имеет значение белковый состав плазмы. Так, альбумины снижают вязкость и способность клеток агрегации, тогда как глобулины действуют противоположно. Особенно активен в повышении вязкости и наклонности клеток к агрегации фибриноген, уровень которого меняется при любых стрессовых состояниях. Гиперлипидемия и гиперхолестеринемия также способствует нарушению реологических свойств крови. Гематокрит - один из важных показателей, связанных с вязкостью крови. Чем выше гематокрит, тем больше вязкость крови и хуже ее реологические свойства. Геморрагия, гемодилюция и, наоборот, плазмопотеря и дегидратация значительно отражаются на реологических свойствах крови. Поэтому, например, управляемая гемодилюция является важным средством профилактики реологических расстройств при оперативных вмешательствах. При гипотермии вязкость крови возрастает в 1,5 раза по сравнению с таковой при 37 град.С, но, если снизить гематокрит с 40% до 20%, то при таком перепаде температур вязкость не изменится. Гиперкапния повышает вязкость крови, поэтому она в венозной крови меньше, чем в артериальной. При снижении рН крови на 0,5 (при высоком гематокрите) вязкость крови увеличивается втрое. ПАТОФИЗИОЛОГИЯ КРОВООБРАЩЕНИЯ РАССТРОЙСТВА РЕОЛОГИЧЕСКИХ СВОЙСТВ КРОВИ. Основной феномен реологических расстройств крови - агрегация эритроцитов, совпадающая с повышением вязкости. Чем медленнее поток крови, тем более вероятно развитие этого феномена. Так называемые ложные агрегаты ("монетные столбики") носят физиологический характер и распадаются на здоровые клетки при изменении условий. Истинные агрегаты, возникающие при патологии, не распадаются, порождая явление сладжа (в переводе с английского как "отстой"). Клетки в агрегатах покрываются белковой пленкой, склеивающей их в глыбки неправильной формы. Главным фактором, вызывающим агрегацию и сладж, является нарушение гемодинамики - замедление кровотока, встречающееся при всех критических состояниях - травматическом шоке, геморрагии, клинической смерти, кардиогенном шоке и т.д. Очень часто гемодинамические расстройства сочетаются и с гиперглобулинемией при таких тяжелых состояниях, как перитонит, острая кишечная непроходимость, острый панкреатит, синдром длительного сдавления, ожоги. Усиливают агрегацию состояние жировой, амниотической и воздушной эмболии, повреждение эритроцитов при искусственном кровообращении, гемолиз, септический шок и т.д., то есть все критические состояния. Можно сказать, что основной причиной нарушения кровотока в капилляроне является изменение реологических свойств крови, которые в свою очередь зависят главным образом от скорости кровотока. Поэтому нарушения кровотока при всех критических состояниях проходит 4 этапа. 1 этап - спазм сосудов-сопротивлений и изменение реологических свойств крови. Стрессовые факторы (гипоксия, страх, боль, травма и т.д.) ведут к гиперкатехоламинемии, вызывающей первичный спазм артериол для централизации кровотока при кровопотере или снижении сердечного выброса любой этиологии (инфаркт миокарда, гиповолемия при перитоните, острой кишечной непроходимости, ожогах и т.д.). Сужение артериол сокращает скорость кровотока в капилляроне, что меняет реологические свойства крови и ведет к агрегации клеток сладжу. С этого начинается 2 этап нарушения микроциркуляции, на котором возникают следующие явления: а) возникает ишемия тканей, что ведет к увеличению концентрации кислых метаболитов, активных полипептидов. Однако явление сладжа характерно тем, что происходит расслоение потоков и вытекающая из капиллярона плазма может уносить в общую циркуляцию кислые метаболиты и агрессивные метаболиты. Таким образом функциональная способность органа, где нарушалась микроциркуляция, резко снижается. б) на агрегатах эритроцитов оседает фибрин, вследствие чего возникают условия для |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 317. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |