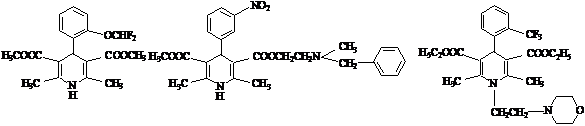Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Будова та загальні способи одержання похідних 1,4-дигідро- піридинуСтр 1 из 3Следующая ⇒ МІНІСТЕРСТВО ОСВІТИ І НАУКИ, МОЛОДІ ТА СПОРТУ УКРАЇНИ ХЕРСОНСЬКИЙ ДЕРЖАВНИЙ УНІВЕРСИТЕТ ФАКУЛЬТЕТ ПРИРОДОЗНАВСТВА, ЗДОРОВʼЯ ЛЮДИНИ І ТУРИЗМУ
ЛИСАК ЮЛІЯ АНДРІЇВНА
СИНТЕЗ ТА ДОСЛІДЖЕННЯ БІОЛОГІЧНОЇ АКТИВНОСТІ ПОХІДНИХ 1,4-ДИГІДРОПІРИДИНУ НА ОСНОВІ о-ТРИФЛУОРОМЕТИЛБЕНЗАЛЬДЕГІДУ 6.040101. Хімія*
Випускна робота освітньо-кваліфікаційного рівня “бакалавр”
Херсон – 2012 ЗМІСТ
ВСТУП……………………………………………………….………………3 РОЗДІЛ 1. Методи синтезу та біологічна активність похідних 1,4-дигідропіридину з флуоровмісними замісниками 1.1. Будова та загальні способи одержання похідних 1,4-дигідропіридину…………………………………………..………5 1.2. Біологічна активність похідних 1,4-дигідропіридину з флуоровмісними замісниками……..……………………………..…10 РОЗДІЛ 2. Синтез та дослідження рістрегулюючої активності похідних 4-арил-1,4-дигідропіридину з флуоровмісними замісниками 2.1.Одержання похідних 4-арил-1,4-дигідропіридину на основі о-трифлуорометилбензальдегіду….....…………………………..…20 2.2. Експериментальна частина…….…………..…………………...26  2.3. Дослідженнярістрегулюючої активності похідних 4-(о-трифлуорометилфеніл)-1,4-дигідропіридину……..………….31 ВИСНОВКИ..……………………………………………………………...43 СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ……………………………….45
ВСТУП Актуальність теми.Хімія гетероциклічних сполук – одна з галузей органічної хімії, яка інтенсивно розвивається в останній час. Число синтезованих та досліджених речовин гетероциклічного ряду набагато переважає число відомих аліциклічних та карбоциклічних сполук. Зростає значення нітрогеновмісних гетероциклів, завдяки високій та специфічній реакційній здатності та виявленої в них біологічної активності. Особливий інтерес викликають гетероциклічні сполуки ряду 4-феніл-1,4-дигідропіридину. Значне місце серед нових біологічно активних речовин займають препарати, що містять флуоровані замісники. Це пов’язано з тим, що як правило введення перфлуороалкільних та деяких інших флуоровмісних замісників в молекулу лікарського препарату призводить до зменшення токсичності та збільшення стійкості сполуки, при цьому біологічна активність лишається незмінною, або навіть зростає. Нітрогеновмісні гетероцикли з флуорованими замісниками вже зараз використовуються в медицині у якості регуляторів транспорту йонів кальцію через біологічні мембрани. Мета – здійснити синтез похідних 1,4-дигідропіридину на основі Завдання: 1) провести аналіз літератури з питання синтезу похідних 1,4-дигідропіридину з флуорованими замісниками; 2) визначити основні способи одержання похідних 1,4-дигідропіридину; 3) синтезувати 4-арилфуро-, 4-арилдифуро-, 4-арилпіроло-, 4-арилдипіроло- та 4-арилфуро-піроло-1,4-дигідропіридини на основі о-трифлуорометилбензальдегіду; 4) дослідити біологічну активність синтезованих сполук. Об’єкт роботи: методи синтезу нітрогеновмісних гетероциклічних сполук та їх біологічна активність. Предмет роботи: синтез похідних 1,4-дигідропіридину на основі о-трифлуорометилбензальдегіду. Структура роботи – робота складається із вступу, двох розділів, висновків, списку використаних джерел (48 найменувань). Робота представлена на 50 сторінках, містить 8 таблиць та 6 рисунків. Перший розділ – це літературний огляд, в якому описана будова, загальні способи одержання та біологічна активність похідних Другий розділ – це безпосередній синтез похідних 1,4-дигідро- піридину на основі о-трифлуорометилбензальдегіду та визначення рістрегулюючої активності синтезованих сполук. Як базові реакції для одержання вихідних сполук нами використовувався синтез Ганча. Даний метод полягає у конденсації відповідного альдегіду з β-кетоестером і амоніаком. Наступним бромуванням та замиканням фуранового або пірольного циклу були одержані 4-арилфуро-, 4-арилдифуро-, 4-арилпіроло- та 4-арилдипіроло-1,4-дигідропіридини. Було проведено вивчення рістрегулюючої активності похідних 1,4-дигідропіридину. Дослідження показали, що синтезовані сполуки проявляють біологічну дію різного ступеня вираженості. Результати дослідження опубліковані у статті «Синтез та біологічна активність похідних 1,4-дигідропіридину», яка була включена до програми конференції «Сучасні проблеми природничих наук».
РОЗДІЛ 1 МЕТОДИ СИНТЕЗУ ТА БІОЛОГІЧНА АКТИВНІСТЬ ПОХІДНИХ 1,4-ДИГІДРОПІРИДИНУ З ФЛУОРОВМІСНИМИ ЗАМІСНИКАМИ Будова та загальні способи одержання похідних 1,4-дигідро- піридину
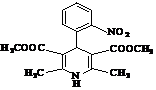
Похідні 1,4-дигідропіридину (1,4-ДГП) відомі людству більш ніж сто років, з того часу як Ганч розробив методи їх синтезу. Найбільшого розвитку хімія 1,4-дигідропіридинів досягла після використання в клінічній практиці високоефективного коронародилататора ніфедипіну (адалату, фенігідину) – 2,6-диметил-3,5-диметоксикарбоніл-4-(2ʼ-нітро- феніл)-1,4-дигідропіридину (1.1) [1, 2]. 1.1
Для одержання 1,4-ДГП загальної формули (1.2) використовують синтез Ганча [1], що являє собою конденсацію альдегіду, b-кетоестеру і амоніаку у співвідношенні 1 : 2 : 1[1, 3]: 1.2
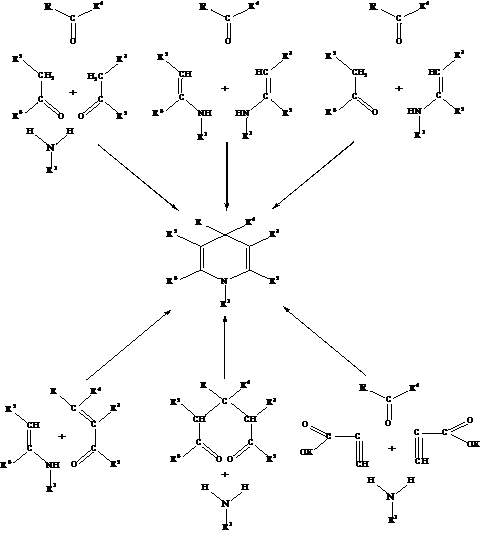
R1 = CH3, C2H5; R = 2-CF3, 3-CF3, 2-OCHF2, 4-OCHF2, 2-SCHF2, 2-SO2CF3, 2-OSO2CHF2, 2-OSO2CHF3, 4-OSO2CHF2. Також застосовуються різні модифікації синтезу Ганча, основні з яких представлено на рис. 1.1.
Рис. 1.1 Способи одержання 1,4-ДГП Синтезовано велику кількість похідних 1,4-дигідропіридину з різноманітними варіаціями замісників, що володіють високою серцево- судинною активністю. Найбільш активними за дією на серцево-судинну систему є 1,4-ДГП з арильними замісниками у положенні 4, найчастіше арил – це заміщений феніл. Такі сполуки одержують конденсацією естерів ацетооцтової кислоти, відповідного альдегіду і амоніаку в розчині етанолу. За таким само способом було отримано сполуку (1.2). Вказано, що 1,4-ДГП типу (1.2) проявляють коронарнорозширювальну та гіпотензивну дію [1, 4, 5]. У порівнянні з ніфедипіном (1.1) вони більш стійкі при зберіганні в твердому вигляді та окисненні у розчинах. 1,4-ДГП з пара-замісниками в арильному радикалі значно менш токсичні, однак їх гіпотензивна та коронаророзширювальна активність дуже мала. Замісники в 3 та 5 положеннях 1,4-дигідропіридинового кільця мають дуже великий вплив на фармакологічну дію похідних 1,4-ДГП. Не лише заміна однієї естерної групи на іншу, але й заміна її на інші групи призводить до якісних та кількісних змін біологічної активності. Це пов’язано із будовою молекули 1,4-ДГП. 1,4-ДГП, що містять неідентичні замісники у положеннях 3 та 5, володіють такою властивістю, як хіральність. Два енантіомери можуть досить сильно відрізнятися за своєю активністю. Але на прикладах енантіомерно чистих 1,4-ДГП було показано, що несиметричні у положеннях 3 та 5 сполуки є більш активними, ніж симетричні; цікаво те, що більш активні з них ті сполуки в яких більш об’ємна естерна група зліва [6, 7]. В останній час стали отримувати 1,4-ДГП з нетрадиційними замісниками в положеннях 3,5, наприклад з залишками фосфатної кислоти. Фосфорильовані 4-алкіл-1,4-дигідропіридини одержують з фосфорильованих енамінів і α,β-ненасичених карбонільних сполук. Пізніше були синтезовані багаточисленні похідні фосфорильованих 1,4-ДГП з різноманітними замісниками в дигідропіридиновому кільці (1.3) [1, 8, 9]:
1.3 R = -CH3, -C2H5, -C3H7, -CH2CH2OC3H7, -(CH2)2N(CH3)CH2C6H5; R1 = -CH3, -NHR³, -C6H5, -CH2SC6H5, -цикло-(CH2)6, -(CH2)6, -CH2OC6H4CF3-м
В результаті розрахунків та рентгеноструктурних аналізів різних похідних 1,4-ДГП типу ніфедіпіну (1.1) вказується, що такі сполуки мають конформацію ванни з 4-арильним замісником, який знаходиться в аксіальному положенні і є ортогональним по відношенню до площини дигідропіридинового кільця (1.4). Окрім того, замісник X має знаходитись по той же бік зв’язку C(4)–Ar, що й атом Гідрогену у C(4), тобто перевага надається синперепланарному ротамеру. Естерні групи знаходяться в екваторіальному положенні. При цьому для оптимальної активності необхідно, щоб карбоніли естерних груп були в цис-трансформації по відношенню до замісників в положенні 2 та 6 дигідропіридинового кільця.
1.4 Велике значення має наявність орто-замісника в 4-арильному ядрі. Він сприяє синперипланарному та ортогональному розміщенню арильного залишку, а також цис/цис конформації естерних груп в 3 та 5 положеннях. Нещодавно було вказано, що в серії 1,4-ДГП (1.5) зі зростанням розміру орто-заміснику в бензеновому кільці найбільш активним як судинорозширюючий агент є 1,4-ДГП із найбільш об’ємним атомом йоду в орто-положенні 4-фенільного кільця [10].
1.5 Hal = F, Cl, Br, I. Якщо замісники у положеннях 3 та 5 різні, для біологічної активності необхідно, щоб у цис-конформації була ліва по відношенню до дигідропіридинового кільця естерна група. 1,4-ДГП, що містять неідентичні замісники у положеннях 3 та 5, володіють такою властивістю, як хіральність. Два енантіомери можуть досить сильно відрізнятися за своєю активністю. Але на прикладах енантіомерно чистих 1,4-ДГП було показано, що несиметричні у положеннях 3 та 5 сполуки є більш активними, ніж симетричні; цікаво те, що більш активні з них ті сполуки в яких більш об’ємна естерна група зліва. При зв’язуванні з рецептором права менша естерна група є важливою для утворення водневого зв’язку з звʼязуючою ділянкою, а більша ліва естерна група завдяки своїй ліпофільності повинна розміщуватися поруч з ліпофільною частиною звʼязуючої ділянки [11].
В основі синтезусполукз замісниками в положеннях 2 та 6 тлежить або прямий синтез, або реакції заміщення. Наприклад, 2-метил-3-(2ʼ-нітрооксипропокси-карбоніл)-4-(3ʼ-нітрофеніл)-5-метоксикарбоніл-6-аміно-1,4-дигідро-піридин отримують конденсацією відповідного похідного бензиліденацетооцтової кислоти і амідину (1.6). 1.6 В деяких випадках використовують реакції нуклеофільного заміщення. Наприклад, бромують 1,4-дигідропіридини бромідом перброміду піридинію і в результаті заміщення брому в отриманому 6-бромметилпохідному (іноді без виділення останнього) отримують різні 1,4-дигідропіридини. Як приклад можна привести одержання 2-метил-3,5-диметоксикарбоніл-4-(2ʼ-хлорфеніл)-6-(2-аміноетилтіометил)- 1,4-дигідропіридину (1.7).
1.7
До сполук, що виявляють позитивний інотропний ефект і є агоністами кальцію, відносяться й 1,4-ДГП, що містять лактонну групу (1.8) [12, 13]. 1.8 Ar = C6H5-, 2-CF3C6H4-, 3-CF3C6H4-, 2-CHF2C6H4-, 2-CHF2OC6H4-, 2-CHF2SC6H4-; R = Me, Et, Pr-i. Міркування щодо 1,4-ДГП, які містять в положенні 3 нітрогрупу, підходять й до даного випадку – лактонну групу можна розглядати, як невеликий за розміром негативно заряджений замісник [14, 15]. Ті ж міркування можна віднести і до сполук, що містять у своєму складі ціаногрупу. 1.2. Біологічна активність похідних 1,4-дигідропіридину з флуоровмісними замісниками Флуоровмісні лікарські препарати з’явилися біля 50 років тому. Фармацевтичні фірми в Японії, ФРН, США та Франції наполегливо працюють над створенням лікарських препаратів, що містять флуор. Дякуючи успіхам хімії флуороорганічних речовин велика кількість флуорованих проміжних продуктів стали доступні та виробляються у промислових масштабах. Це сприяє інтенсивному розвитку хімії флуоровмісних лікарських речовин. З кінця 1960-х років у лікуванні хвороб, пов’язаних з високим кров’яним тиском і порушеннями в серцево-судинній системі, почались серйозні позитивні зрушення, так як в цей час на фармацевтичному ринку з’явились перші представники блокаторів кальцієвих каналів. Найцікавішими серед них є похідні 1,4-дигідропіридину, особливо найбільш ефективні препарати були синтезовані в 1980-1990-х роках. На сьогоднішній день вони складають великй фармацевтичний блок вазодилаторів і антигіпертензивних засобів [17, 18] . Похідні 1,4-ДГП володіють кардіоваскулярною, гепатопротекторною, протипухлинною, антимутагенною активністю. Як гіпотензивні засоби із цього класу використовують ніфедіпін (1.1), нітрендипін, ріодипін (форидон) (1.9), нікардипін (1.10) і флуордипін (1.11):
1.9 1.10 1.11 Механізм біодії дигідропіридинів заснований на перекриванні каналів кліткової мембрани, через які із навколишньго середовища клітини (де концентрація йонів кальцію 3·10-3 М) всередині клітини В результаті досліджень, проведених різними авторами, залежності активності похідних 1,4-ДГП від їх структури для ряду модельних систем, у тому числі для гладкої мускулатури стінок судин та серцевого м’яза, вдалося знайти загальні закономірності, які є необхідними для того, щоб похідні 1,4-ДГП виявляли біологічну активність [1, 21]: 1. Необхідна наявність 1,4-дигідропіридинового ядра. 2. Для максимальної активності сполука не повинна містити в першому положенні, тобто біля атому нітрогену 1,4-дигідропіридинового кільця, замісник. 3. Замісники у положеннях 2 або 6 повинні бути низькомолекулярними алкілами, але можлива і заміна алкільної групи на аміно-, ціано- або формільну групи. 4. Оптимальними замісниками у положеннях 3 та 5 є естерні групи, але це можуть бути й інші електронно-акцепторні замісники. 5. У положенні 4 для оптимальної активності має знаходитись арильний залишок. При цьому велике значення має положення замісника у фенільному кільці. Пара-замісники знижують активність, а орто- та мета-замісники підвищують ії. 6. Якщо замісники у 3 та 5 положеннях 1,4-дигідропіридинового кільця різні, положення 4 стає хіральним, внаслідок чого енантіомери виявляють різні, а інколи навіть протилежні властивості. Також було висунете припущення що, найбільш високою активністю володіють 1,4-ДГП, які містять: 1) карбоксильні групи в положеннях 3,5 (переважно метилові або етилові ефіри карбонових кислот); 2) метильні групи в положеннях 2,6; 3) орто-заміщений арильний залишок в положенні 4 1,4-дигідропіридинового кільця. Синтезовано велику кількість 1,4-ДГП з різними варіаціями замісників, які володіють високою серцево-судинною активністю [1, 23]. Але в подальшому було показано, що наявність цих ознак в молекулі 1,4-ДГП необов’язкова [1, 24]. За останні роки синтезовано ряд флуоровмісних аналогів ніфедипіну та інших похідних 1,4-ДГП, що мають фармакологічну дію. В наш час накопичена велика кількість даних про вплив заміни атомів гідрогену флуором в молекулах сполук на їх біологічні властивості. Введення атомів флуора не завдає помітних стеричних перепон, які змінюють конформацію молекул, і не викликає труднощів їх взаємодії з активними центрами біосубстрату. Заміщення атомів гідрогену в біологічних системах на флуоровмісні аналоги на певній стадії метаболізму призводить до інгібування процесів життєдіяльності патологічних клітин, призупиняє їх розвиток. Великі можливості для модифікації властивостей лікарських препаратів з’явились в результаті розроблення зручних методів синтезу ароматичних і гетероциклічних сполук з флуоровмісними замісниками. Визначення їх електронної природи, параметрів гідрофобності відкрило нові шляхи напрямленого синтезу біологічно активних сполук. Введення флуоровмісних замісників в препарати призводить до збільшення їх розчинності в ліпідах, що в багатьох випадках підвищує ефективність лікарських препаратів внаслідок полегшення їх транспорту в організмі, проникнення через мембрани, збільшення їх концентрації в ліпідних ділянках [25, 26]. Атом флуору володіє найбільш близькими до атома гідрогену ковалентним та ван-дер-ваальсовим радіусами – 7,2∙10-2 та 3,7∙10-2 нм; 13,5∙10-2 та 12,1∙10-2 нм відповідно. Ван-дер-ваальсовий радіус флуоровмісного замісника, який найбільш часто зустрічається, групи -CF3 також мало відрізняється від радіусу метильної. Тому введення атомів флуора не створює помітних стеричних перешкоджень, які змінюють конформацію молекул, та не утруднюють їх взаємодію з активними центрами біосубстрату. Значна енергія зв’язку C-F обумовлює виключну хемо- та біостійкість флуорованих сполук. При правильному визначенні місця введення атомів флуора у молекулу, що володіє біологічною активністю, і мало відбивається на її кислотно-основних та інших властивостях, організм не може відрізнити сполуку, яка містить флуор, від її аналога та засвоює його. Великі можливості для модифікації властивостей лікарських препаратів з’явилися у результаті розробки зручних методів синтезу ароматичних та гетероциклічних сполук з флоуровмісними замісниками. Введення флуоровмісних замісників звичайно приводить до збільшення їхньої розчинності у ліпідах, що у багатьох випадках підвищує ефективність лікарських препаратів внаслідок полегшення їхнього транспорту в організмі, проникнення крізь мембрани [27, 28, 39]. Електронна природа замісника – один з важливих факторів, які необхідно враховувати при створенні лікарських препаратів. Введення флуоровмісних замісників дозволяє, досягати необхідних параметрів, що визначають кислотно-основні властивості сполуки: замість нітрогрупи – групи -SO2CHF2 або -SO2CF3, замість атомів галогенів – групи -ОCF3, -ОCF2Н, -SCF3, -SCHF2 або трифлуорометильні групи. Сьогодні синтезовано багато аналогів левоміцетину і висловлено припущення, що для досягнення високої бактерицидної дії необхідна наявність сильного електронноакцепторного замісника в пара-положенні до бокового ланцюга, який дорівнює або перевищує вплив нітрогрупи. Синтез 4-SO2CF3- аналога препарату підтвердив це припущення. Нещодавно при пошуку більш ефективних антигіпертензивних засобів в низці похідних 1,4-ДГП несподівано було відкрита нова нейропротекторна лікарська речовина цереброкраст (1.12) [22, 29, 30]:
1.12 Цереброкраст (1.12) (2,6-диметил-3,5-біс[(2-пропоксиетокси- карбоніл-4-(2-дифторметоксифеніл)]-1,4-дигідропіридин) володіє високою спорідненістю до ДГП-рецепторів, але основним ефектом його дії є посилення функцій головного мозку. Він проявляє нотропну дію, покращуючи пізнавальні здібності і пам’ять, а також нейропротекторну активність (коректуючи вікові, антигіпоксичні і антиалкогольні порушення в нейронах). Цереброкраст відрізняється від німодипіну та інших відомих похідних дигідропіридину наявністю в структурі дифторометоксигрупи, яка підсилює ліпофільність молекули і церебральну селективність вазодилуючої дії. Виявлено його відносна безпека і добра переносимість. Форидон (1.9) (ріодипін, 2,6-диметил-3,5-дикарбметокси- 4-(о-дифторметоксифеніл)-1,4-дигідропіридин) за хімічною структурою близький до препаратів фенігідину (ніфедипіну) і SKF-24260, які відомі як ефективні гіпотензивні речовини [34]. Детально вивчена дія форидону на функцію серцево-судинної системи різних видів тварин, вивчено механізм дії препарату і проведені його клінічні дослідження. Під впливом форидону знижується загальний периферійний опір. Опір судин серця і мозку знижується в першу чергу. Форидон (1.7) зменшує прояви гострої ішемії міокарда. За механізмом дії форидон є антагоністом йонів кальцію як в дослідах на цілісних тваринах, так і на ізольованих органах. В клінічній практиці форидон проявляє сприятливий терапевтичний ефект при гіпертонічній, ішемічній хворобі серця, не викликаючи істотних побічних явищ. Можливе використання форидону в комбінаціях з іншими судинорозширюючими засобами [35, 36].
Крім того було вивчено вплив сполук (1.13 а-в), (1.14 а-в) на серцево-судинну систему. Скрінінг проведено за загальноприйнятими методиками на інотропну (ізольований міокард), гіпотензивну та гіпертензивну, антимікробну дію (системний рівень, наркотизовані пацюки) [5, 37]. 1.13 1.14 а: 2 – NHSO2CF3, R = CH3; б: 2 – NHSO2CF3, R = C2H5; в: 3 – NHSO2CF3, R = C2H5. Результати наведено в таблиці 1.1. Таблиця 1.1 Вплив сполук (1.13 а-в), (1.14 а-в) на серцево-судинну систему
Знак «+» або «-» біля відносних значень фармакологічних показників вказує на характер їх змін (порівнюючи з контролем) в результаті дії досліджуваних сполук. Дослідження показують, що всі сполуки проявляють гіпотензивну дію різного ступеня вираженості. Сполука (1.13 в) не проявляє помітної дії на серцево-судинну систему. Інші сполуки проявляють гіпотензивну та негативну інотропну дію різної вираженості: сполуки (1.13 б, в) – помірний; сполуки (1.13, б) та (1.14 а) – виражений ефект. Характерною особливістю фармакологічного ефекту 2,6-диметил- 3,5-дикарбометокси-4-[2-N,N-біс(трифлуорметил)амінофеніл]-1,4-ДГП є довготривалість та стійкість ефекту (більше 2 годин). Враховуючи подібність фармакологічного профілю сполук даної групи та еталонного препарату (ніфедипіну) можливе припущення щодо загального механізму їх дії – блокування входу йонів кальцію до клітини. Таким чином 2,6-диметил-3,5-дикарбометокси-4-[2-N,N-біс(трифлуоро- метил)-амінофеніл]-1,4-дигідропіридин подібний до еталонних антагоністів йонів кальцію не лише за фармакологічним профілем, але й за рівнем активності. Найбільш відоме похідне 1,4-ДГП, що має здатність відкривати кальцієві канали – препарат BAY K 8644 (1.15). BAY K 8644 посилює напругу ізольованої артерії морської свинки. Вказується, що він посилює струм йонів кальцію особливо за умови негативного потенціалу мембран. За силою дії BAY K 8644 відповідає ніфедипіну, але дія його протилежна за напрямком.
Однак за великої концентрації BAY K 8644 діє, як слабкий вазодилятор. Було знайдено, що властивості агоніста кальція має енантіомер (S) (-) BAY K 8644 (1.15 а), (R) (+) BAY K 8644 (1.15 б) є слабким антагоністом [39]. 1.15 а 1.15 б
Як уже говорилось, 1,4-ДГП є антагоністами йонів кальцію і володіють серцево-судинною активністю. Деякі з них діють селективно, наприклад, 1.16 найбільш активний як переферійний вазодилатор [1]. 1.16 R1 = о- або м-NO2; R2 = -СН3 або -С2Н5
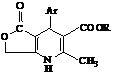
Відомо, що фуро-[3,4-b]піридини мають позитивну інотропну дію. З метою пошуку нових кардіотонічних засобів в ряду дифуропіридинів синтезовані невідомі раніше сполуки 1.17-1.22 [16]. 1.17-1.22 R = 3-Br (1.17), 4-Br (1.18), 2-F (1.19), 4-I (1.20), 4-OCH3 (1.21), 2,4-Cl2 (1.22). Вплив сполук 1.17-1.22 на силу та частоту серцевих скорочень досліджували в дослідах на ізольованих спонтанно скорочувальних передсердях кролів. Вплив на параметри гемодинаміки досліджували в дослідах на наркотизованих хлоралозою кішках. Сполука 1.19 з замісником 2-F в арильному кільці викликало збільшення сили скорочень на 75% в концентрації 10-5 моль. Сполуки 1.17, 1.18 і 1.22 викликали невелику стимуляцію сили скорочень, а сполука 1.18 і 1.21 не змінювали скорочень передсердя. Таким чином, найбільш активним кардіотонічною сполукою є дифуропіридин 1.19, однак він поступається відомому препарату – строфантину [16]. Із усього вище згаданого, можна зробити висновок, що найбільшою біологічною активністю володіють флуоровмісні похідні
РОЗДІЛ 2 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-05-29; просмотров: 308. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |