
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Приготовление питательных сред из промышленноМетоды холодной стерилизации Механическая стерилизация (фильтрование). Этот способ применяется для стерилизации сред в тех случаях, когда их нельзя подвергать нагреванию. При механической стерилизации стерилизуемые жидкости фильтруют через специальные фильтровальные приборы, которые имеют настолько мелкие поры, что на своей поверхности задерживают взвешенные в жидкости частицы, в том числе и микробы. Для фильтрации в микробиологической практике применяют различные фильтровальные приборы (фильтры Зейтца, свечи Шамберлана, Мандлера, Беркефельда и др.). Химическая стерилизация. Этот вид стерилизации в практике приготовления питательных сред имеет ограниченное применение. В лабораторной практике используют некоторые химические вещества, такие как толуол, хлороформ, эфир и другие, для предупреждения бактериального загрязнения питательных сред. Для освобождения от консерванта среду нагревают на водяной бане при 56 0С. Химическая стерилизация используется также для дезинфекции оборудования, помещений, использованной посуды и отработанного микробиологического материала. В качестве дезинфицирующих веществ широкое применение нашли химические соединения, содержащие активный хлор (хлорамин, хлорная известь). Стерилизация ультрафиолетовыми лучами. Этот способ стерилизации используется для стерилизации воздуха в микробиологическом боксе и в лаборатории перед проведением микробиологических исследований. Стерилизацию ультрафиолетовыми лучами проводят с помощью бактерицидных ламп.
1.1.3 Устройство парового стерилизатора и принцип его работы 
Устройство стерилизатора Основными частями стерилизатора являются: стерилизационная камера -служит для размещения стерилизуемых объектов; парогенератор – служит для выработки пара (в парогенераторе находятся нагревательные элементы - тэны, используемые для нагрева воды и получения пара, и датчики уровня, которые нужны для предотвращения выхода из строя нагревательных элементов); система трубопроводов – для соединения сборочных единиц стерилизатора; электрошкаф – для управления электрической системой стерилизатора; манометр электроконтактный – для наблюдения за давлением в парогенераторе и поддержания его работы в автоматическом режиме; моновакуумметр – для наблюдения за давлением и разряжением в стерилизационной камере; клапан предохранительный - для сброса пара при превышении давления в парогенераторе; колонка водоуказательная (водомерная трубка) – для наблюдения за уровнем жидкости в парогенераторе; вентили – для управления работой стерилизатора.
Принцип действия пневмогидравлической и электрической систем парового стерилизатора Заключается в следующем: Вода поступает по водопроводу в парогенератор. Контроль за уровнем жидкости в парогенераторе осуществляют с помощью водомерной трубки. После включения стерилизатора, начинают нагреваться тэны, благодаря чему вода нагревается до рабочей температуры. В результате образуется пар. При достижении в парогенераторе давления пара 0,11 МПа открывается вентиль «Пар в камеру» и вентиль «Слив конденсата». Происходит продувка и прогрев стерилизационной камеры, после чего вентиль «Слив конденсата» закрывается. При достижении в стерилизационной камере рабочего давления (контролируется электроконтактным манометром) происходит отчет времени стерилизации. В процессе стерилизации происходит автоматическое включение и отключение стерилизатора с помощью электроконтактного манометра. Контроль за давлением в стерилизационной камере осуществляется моновакуумметром. После проведения стерилизации аппарат отключают от сети и перекрывают вентиль «Пар в камеру». Далее, по мере падения давления в стерилизационной камере до 0,06 МПа (контроль осуществляется по моновакуумметру) открывается вентиль «Вакуум». В стерилизационной камере создается разряжение. Происходит процесс сушки стерилизуемого материала. По истечении сушки открывается вентиль «Воздух в камеру». При этом происходит выравнивание давления в стерилизационной камере с атмосферным давлением.
ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ Студенты знакомятся с принципами составления и классификацией питательных сред, методами стерилизации питательных сред, посуды, инвентаря, изучают устройство парового стерилизатора и принцип его работы и кратко конспектируют изложенный в теоретической части материал. Затем готовят посуду, питательные среды и ватно-марлевые пробки для проведения микробиологического анализа. Приготовление посуды для проведения микробиологического Анализа Для проведения микробиологического анализа используют чашки Петри, которые герметично упаковываются в пергаментную бумагу и стерилизуются. Пипетки на 1 см3 закрывают ватными тампонами и также заворачивают в бумагу. Колбы закрывают ватно-марлевыми пробками и сверху делают колпачки из пергаментной бумаги. Стерилизация посуды осуществляется в автоклаве при избыточном давлении 0,1 МПа в течение 30-40 минут или сухим жаром в сушильном шкафу или печи Пастера при 165-170 0С в течение 1-1,5 часа. Стерильную посуду следует хранить в плотно закрывающихся шкафах или ящиках с крышками в течение не более 30 суток.
Приготовление питательных сред из промышленно выпускаемых сухих сред Заключается в растворении определенного количества порошка в воде, доведении полученной смеси до кипения и кипячении в течение 5 минут. Далее (при необходимости) среда фильтруется через ватно-марлевый фильтр и разливается в пробирки или колбы, которые закрываются ватно-марлевыми пробками. Далее среды стерилизуют в автоклаве. С использованием сухих сред готовят мясопептонный бульон (МПБ), мясопептонный агар (МПА), среду Сабуро, среду Кесслера, среду для определения мезофильный аэробных и факультативно-анаэробных микроорганизмов (среда для определения КМАФАнМ), среду Эндо и др.
1.2.3 Приготовление питательных сред из отдельных компонентов Проводится по методикам, описанным в приложении 2 данного лабораторного практикума.
Контрольные вопросы 1. Что такое питательные среды? 2. Микроорганизмы, которые встречаются в пищевых продуктах, являются хемоорганогетеротрофами. Что это значит? 3. Охарактеризуйте пищевые потребности хемоорганогетеротрофов. 4. Какие требования предъявляются к питательным средам? 5. Каким образом готовятся плотные питательные среды и для чего они используются? 6. Почему в качестве уплотнителя для питательных сред лучше использовать агар-агар, а не желатин? 7. На какие группы делятся питательные среды по происхождению и составу? 8. Что такое синтетические среды и в каких случаях они применяются? 9. Для каких целей используются универсальные, избирательные и дифференциально-диагностические среды? 10. Приведите примеры универсальных, избирательных и дифференциально-диагностических питательных сред. 11. Что такое стерилизация? Какие методы стерилизации Вам известны? 12. Какими способами можно стерилизовать посуду? 13. Какими из известных Вам способов можно стерилизовать питательные среды? 14. Как готовятся питательные среды и посуда для стерилизации? 15. Каково устройство и принцип работы парового стерилизатора? ЛАБОРАТОРНАЯ РАБОТА №2
УСТРОЙСТВО МИКРОСКОПА И ПРАВИЛА РАБОТЫ С НИМ. ВИДЫ МИКРОСКОПИИ. ПРИГОТОВЛЕНИЕ ФИКСИРОВАННЫХ ПРЕПАРАТОВ БАКТЕРИЙ И ОКРАСКА ИХ ПРОСТЫМИ МЕТОДАМИ
Цель работы: Изучить устройство светового биологического микроскопа и освоить правила работы с ним. Ознакомиться с различными видами микроскопии. Приобрести навыки по приготовлению фиксированных препаратов бактерий и освоить технику окраски препаратов бактерий простыми методами.
Оборудование, материалы: Микроскоп; бактериологические петли; предметные стекла; спиртовка; иммерсионное масло; фильтровальная бумага; краска Муромцева; фуксин; лоток с рельсами; промывалка; кефир; чистые культуры бактерий: Staphylococcus albus, Sarsina flava; 96 %-ный этиловый спирт.
2.1 КРАТКИЕ ТЕОРЕТИЧЕСКИЕ ПОЛОЖЕНИЯ
2.1.1 Устройство микроскопа и правила работы с ним Микроскоп (от греч. micros – малый и scopio – смотрю) – это оптический прибор, состоящий из трех основных частей: механической, оптической и осветительной. Устройство микроскопа Схема светового биологического микроскопа представлена на рис. 1. Механическая часть или штатив состоит из ножки, основания, тубусодержателя, предметного столика, монокулярной насадки (тубуса), револьверного устройства, рукоятки грубой фокусировки (макрометрического винта), рукоятки тонкой фокусировки (микрометрического винта). Тубус – зрительная труба микроскопа. В верхнее отверстие тубуса свободно вставляется окуляр, на нижнем конце тубуса находится вращающееся вокруг своей оси револьверное устройство (револьвер), в которое ввинчиваются объективы. Вращая револьвер, можно быстро сменить объективы во время работы с микроскопом, подводя любой объектив под тубус. Объектив должен быть центрирован, т.е. установлен на оптическую ось микроскопа. Для этого револьвер поворачивают вокруг своей оси до появления щелчка. Предметный столик служит для размещения на нем изучаемого препарата. Препарат закрепляют на столике зажимами (клеммами). В центре предметного столика находится отверстие для прохождения лучей света и освещения препарата. В некоторых конструкциях микроскопа предметный столик может передвигаться с помощью винтов, расположенных по периферии предметного столика. Это дает возможность рассмотреть препарат в различных полях зрения.
Рис. 1 Схема устройства светового биологического микроскопа
Рукоятки грубой и тонкой фокусировки (макро- и микровинты) служат для перемещения тубуса вверх и вниз, что позволяет установить его на необходимом расстоянии от препарата. При вращении винтов по часовой стрелке тубус опускается, а при вращении против часовой стрелки – поднимается. При вращении макрометрического винта объектив ориентировочно устанавливается на фокус, т.е. на то расстояние от препарата, при котором он делается видимым. Оборот макровинта позволяет переместить тубус на 20 мм. Микрометрический винт служит для точной установки на фокус. Полный оборот его перемещает тубус на 0,1 мм. С микровинтом следует обращаться очень осторожно: допустимо вращение микровинта не более чем на 180 0С в ту или иную сторону.
Оптическая часть является наиболее ценной частью микроскопа. Она состоит из объективов и окуляра. Окуляр (от лат. oculus – глаз) состоит их двух плосковыпуклых линз, заключенных в общую металлическую оправу. Верхняя линза – глазная (увеличивающая), нижняя – собирающая. Расстояние между линзами равно полусумме их фокусного расстояния. У окуляров с большим увеличением фокус короче, поэтому меньше и длина окуляра. Между линзами имеется диафрагма, ограничивающая поле зрения и задерживающая краевые лучи света. Отечественные микроскопы снабжены тремя сменными окулярами, увеличение которых указано на корпусе окуляра (х7; х10; х15). Объективы ввинчиваются в гнезда револьверного устройства и состоят из системы линз, заключенных в металлическую оправу. Передняя (фронтальная) линза объектива является самой маленькой и единственной, дающей увеличение. Остальные линзы в объективе только исправляют недостатки полученного изображения (явления сферической и хроматической аберрации) и называются коррекционными. В гнезда револьверного устройства ввинчиваются четыре объектива, увеличение которых указано на корпусе объектива (х8; х20; х40; х90 или 100). Каждый объектив характеризуется своим фокусным расстоянием (расстоянием между предметным стеклом и фронтальной линзой): объектив х8 имеет фокусное расстояние около 9 мм, объектив х40 – 0,65 мм, объектив х90 – 0,15 мм. Объективы подразделяются на сухие и иммерсионные. При работе с сухими объективами (х8, х20, х40) между фронтальной линзой и препаратом находится воздух. В этом случае лучи света проходят среды с различными показателями преломления (покровное стекло, воздух), часть их отклоняется и не попадает в объектив. При работе с иммерсионными объективами (х90 или х100) для устранения светорассеяния расстояние между фронтальной линзой объектива и препаратом заполняют иммерсионным (кедровым) маслом, показатель преломления лучей света которого близок к показателю преломления лучей света, проходящего через стекло. Общее увеличение микроскопа определяется как произведение увеличения объектива на увеличение окуляра. Например, если в работе используют окуляр х15, а под тубусом находится объектив х90, то увеличение рассматриваемого с помощью микроскопа объекта составит х1350. Осветительная часть микроскопа состоит из двухлинзового конденсора, ирис-диафрагмы и патрона с низковольтной лампочкой накаливания, питающейся через понижающий трансформатор от сети напряжения 120…220 В. Конденсор служит для лучшего освещения препарата. Он собирает световые лучи в пучок и направляет их через отверстие предметного столика на препарат. С помощью рукоятки для перемещения кронштейна конденсора его можно перемещать вверх и вниз, благодаря чему меняется угол сходимости лучей и, следовательно, степень освещения объекта. Чем выше положение конденсора, тем лучше освещен препарат. Ирис-диафрагма располагается под конденсором и служит для регулировки потока света, поступающего в конденсор. Она состоит из металлических серповидных пластинок. Расширить или сузить отверстие диафрагмы можно с помощью специального рычажка. При вращении его по часовой стрелке отверстие ирис-диафрагмы увеличивается и, следовательно, увеличивается степень освещения объекта. При работе с иммерсионными объективами степень освещения препарата должна быть максимальной, поэтому шторку ирис-диафрагмы открывают, а конденсор поднимают в крайнее верхнее положение. При работе с сухими объективами, как правило, рассматривают неокрашенные объекты. Для достижения контрастности конденсор опускают вниз, а отверстие ирис-диафрагмы уменьшают.
Правила работы с микроскопом 1. На рабочем столе микроскоп ставят тубусодержателем к себе на расстоянии 3…5 см от края стола; 2. Включают микроскоп в сеть и устанавливают правильное освещение (см. раздел 2.1.1); 3. На предметный столик помещают исследуемый препарат и закрепляют его клеммами; 4. Под тубус помещают нужный объектив и с помощью макро и микровинтов устанавливают фокусное расстояние. Так, при работе с иммерсионными объективами на препарат предварительно наносят каплю иммерсионного масла и осторожно опускают тубусодержатель макровинтом до соприкосновения со стеклом. Затем, внимательно смотря в окуляр, очень медленно поднимают тубусодержатель, вращая его против часовой стрелки, до тех пор, пока не увидят изображение. Точную наводку объектива на фокус производят микрометрическим винтом. При работе с сухими объективами препарат вначале рассматривают с объективом х8. Поднимая с помощью макровинта тубусодержатель и внимательно смотря в окуляр, устанавливают фокусное расстояние (около 9 мм) и добиваются четкости изображения, используя микрометрический винт. Далее, двигая предметный столик или предметное стекло, устанавливают в центр поля тот участок препарата, в котором лучше всего виден изучаемый объект. Затем, вращая револьверное устройство вокруг своей оси, под тубус помещают объектив на х20 или х40. При этом под тубус не должен попасть объектив х90. В револьверном устройстве объективы располагаются таким образом, что если найдено изображение с объективом х8, то при рассмотрении препарата с объективами большего увеличения нужно слегка подрегулировать четкость изображения с помощью макро- и микрометрических винтов; 5. Во время микроскопирования необходимо держать оба глаза открытыми и пользоваться ими попеременно; 6. После окончания работы следует убрать препарат с предметного столика, опустить вниз конденсор, поставить под тубус объектив х8, удалить мягкой тканью или марлей, смоченной в спирте, иммерсионное масло с фронтальной линзы объектива х90, под объектив положить марлевую салфетку, опустить тубусодержатель. 2.1.2 Виды микроскопии Основными характеристиками микроскопа являются общее увеличение и разрешающая способность. Общее увеличение не характеризует качества изображения, которое может быть четким и нечетким. Четкость получаемого изображения определяется разрешающей способностью микроскопа, т.е. той наименьшей величиной объектов или их деталей, которые можно увидеть с помощью этого прибора. Разрешающая способность зависит от длины проходящего через объект света, показателя преломления оптической среды (показатель преломления воздуха равен 1,0; иммерсионного масла – 1,516; стекла –1,520) и апертурного угла объектива. Эту зависимость вывел немецкий физик Эрнст Аббе во второй половине XIX века: d = l / 2 n sin a, где: d – минимальное расстояние между двумя точками, видимыми раздельно; l - длина волны света, проходящего через исследуемый объект; n sina - числовая апертура, где n –показатель преломления светом оптической среды, a - апертурный угол объектива.
На рис.2 представлена схема, иллюстрирующая понятие апертурного угла микроскопа (стрелками обозначен ход световых лучей).
Рис. 2 Схема, иллюстрирующая понятие апертурного угла
Э. Аббе доказал, что нет смысла беспредельно повышать увеличение светового микроскопа. Минимальное расстояние между двумя точками при освещении объекта светом с длиной волны 550 нм, к которому наиболее чувствителен глаз, при использовании микроскопа, апертурный угол которого 900 (это предельный угол для которого sina=1), для сухой системы составляет около 300 нм, а для иммерсионной системы – около 200 нм. Таким образом, повысить разрешающую способность микроскопа можно путем: - снижения длины волны света, проходящего через объект; - использования иммерсионной системы; - повышения апертурного угла до предельного (до 900). - Микроскопия в темном поле Используется для исследования слишком малых и слабоконтрастных живых объектов. При микроскопии этим методом используют специальный конденсор темного поля, центр которого затемнен. Поэтому центральный пучок световых лучей не попадает в объектив и поле зрения микроскопа остается темным. Объект освещается только лучами, попадающими на него под углом. Рассеиваясь на объекте, часть лучей изменяет направление и попадает на объектив. Объект становится видимым как светящаяся точка на темном фоне. Метод темного поля позволяет получить представление о внешней форме живых неокрашенных объектов и их движении. Микроскопия в темном поле позволяет увеличить разрешающую способность объектива примерно в 10 раз и рассматривать объекты, размеры которых находятся за пределами обычного микроскопа. Повышение разрешающей способности достигается за счет увеличения апертурного угла.
Фазово-контрастная микроскопия Дает возможность изучать живые объекты без окраски и фиксирования. Глаз человека реагирует на изменения амплитуды световой волны (интенсивность, контрастность) и ее длины (цвет), но не воспринимает различий по фазе. В биологических препаратах чередуются места, которые в разной степени поглощают свет. Проходя через них, световые волны изменяют свою амплитуду. Такие участки объекта называют амплитудными, и под микроскопом они выглядят более темными. Прозрачные в видимом свете структурные элементы объектов пропускают лучи одинаковой длины и амплитуды, но смещают их фазу. Величина смещения зависит от толщины и показателя преломления структур, но видимых изменений практически не дает. Такие препараты являются неконтрастными. С помощью фазово-контрастного устройства фазовые изменения световых волн, проходящих через прозрачные объекты, превращаются в амплитудные, благодаря чему детали рассматриваемых объектов становятся видимыми и контрастными. Фазово-контрастное устройство дает возможность изучать структуры клеток: жгутики и оболочки бактерий, ядра и митохондрии дрожжей и грибов. Таким образом, хотя разрешающая способность при использовании фазово-контрастной микроскопии не меняется при сравнении со светопольной, качество изображения улучшается за счет повышения контрастности. Люминесцентная микроскопия Люминесцентная микроскопия позволяет изучать клетки в живом виде, выявлять мембранные структуры и получать высококонтрастные цветные изображения микроорганизмов. Сущность явления люминесценции заключается в том, что некоторые молекулы структурных элементов клетки (пигменты, витамины, алкалоиды и др.) способны поглощать часть энергии падающего света определенной длины волны, переходить в электронно-возбужденное состояние и испускать свет с другой длиной волны. Источником возбуждения могут быть ультрафиолетовые лучи (300-400 нм) и видимый свет коротковолновой области спектра (400-460 нм). Клетки микроорганизмов обладают слабой собственной (первичной) люминесценцией. Ее можно усилить предварительным окрашиванием препаратов нетоксическими красителями – флуорохромами (акридин оранжевый, нейтральный красный, аурамин, флуоресцин и др.). В результате возникает вторичная люминесценция. Для ее возбуждения достаточно использовать сине-фиолетовую часть спектра. В результате возникает высококонтрастное цветное изображение рассматриваемого объекта. Таким образом, при использовании люминесцентной микроскопии разрешающая способность микроскопа возрастает по сравнению со светопольной микроскопией за счет уменьшения длины волны проходящего через объект света. Электронная микроскопия Максимальная разрешающая способность оптических микроскопов составляет около 0,2 мкм и зависит от длины волны используемых лучей света. Увеличить разрешение в 100 и более раз можно, если вместо световых или ультрафиолетовых лучей применять поток движущихся электронов, обладающих волновыми свойствами (длина волны около 0,04 нм). Поток электронов движется в безвоздушном пространстве от источника электронов (раскаленная нить вольфрамовой пушки) по направлению к флуоресцентному экрану и вызывает равномерное свечение его. Если же на пути электронов поместить какой-либо объект, то в зависимости от его плотности электроны будут больше или меньше задерживаться, а соответствующие места на экране окажутся более или менее затемненными. Этот простой принцип работы современного электронного микроскопа дополнен принципом отклонения электронных лучей в магнитном поле подобно тому, как световые лучи отклоняются увеличивающими стеклянными линзами. При этом используются электромагнитные линзы. Высокая разрешающая способность современных электронных микроскопов позволяет наблюдать и изучать объекты, невидимые в оптических микроскопах: вирусы и фаги, микоплазмы, строение клеток прокариотов и эукариотов, их макро- и микроструктурные элементы. Препараты для электронной микроскопии готовят в виде очень тонких срезов на специальных ультрамикротомах или на тончайших пленках – подложках из коллодия. Следовательно, в электронных микроскопах микроорганизмы исследуют не в живом состоянии, а в виде фиксированных препаратов.
2.2 ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ
На занятии студенты знакомятся с устройством микроскопа и правилами работы с ним, видами микроскопии, основными особенностями их устройства и принципами их работы. Затем они осваивают технику отбора чистых культур микроорганизмов и методику приготовления фиксированных препаратов бактерий. Готовят фиксированные препараты из чистых культур (Staphylococcus albus, Sarsina flava) и естественных мест обитания (кефира, зубного налета). Далее окрашивают эти препараты простыми методами (чистые культуры и зубной налет – фуксином, а кефир – краской Муромцева) и рассматривают их с использованием иммерсионной системы с объективом х90 или х100 при максимальном освещении.
2.2.1 Техника отбора чистых культур микроорганизмов Отбор проб чистых культур бактерий и дрожжей, которые вырастают на поверхности плотной среды в виде мазеобразного налета или в жидкой среде ведут в следующей последовательности: 1. Зажигают спиртовку. 2. Пробирку с культурой помещают в левую руку между большим и указательным пальцами в наклонном положении. Поверхность с налетом микроорганизмов должна быть обращена вверх и хорошо видна. 3. Петлю держат вертикально в пламени горелки и прокаливают докрасна, затем наклоняют и обжигают примыкающую к ней часть петледержателя. 4. Мизинцем и безымянным пальцем правой руки прижимают к ладони наружную часть ватной пробки, вынимают ее из пробирки и держа в таком положении, не касаясь окружающих предметов. 5. Края открытой пробки обжигают в пламени горелки. 6. Осторожно вводят стерильную петлю в пробирку с культурой и охлаждают ее о стенки пробирки или прикоснувшись к питательной среде, свободной от микроорганизмов. Немного отстранив пробирку с культурой от пламени горелки, легким движением осторожно отбирают небольшое количество микробной массы с поверхности среды или каплю жидкости с клетками. Вынимая петлю из пробирки, следят за тем, чтобы отобранный материал не касался стенок и петля не оказалась над пламенем горелки. 7. Снова обжигают в пламени горелки край пробирки, затем, легким круговым движением, обжигают ватно-марлевую пробку и закрывают пробирку. 8. Пробирку с культурой ставят в штатив, а извлеченный материал используют для приготовления препарата. 9. Клетки микроорганизмов, оставшиеся не петле, сжигают в пламени горелки. Отбор чистых культур микроскопических грибов ведут с использованием препаровальной иглы в той же последовательности, что и отбор одноклеточных организмов. Из пробирки отбирают кусочек мицелия, слегка погружая иглу в питательную среду таким образом, чтобы не нарушить структуру мицелия.
2.2.2 Приготовление препаратов фиксированных клеток Фиксированными считают клетки микроорганизмов, в которых прерваны жизненные процессы, но полностью сохранена тонкая структура. Для получения фиксированных препаратов важно правильно подготовить предметные стекла. Они должны быть чистыми и тщательно обезжиренными. Для этого стекла, бывшие в употреблении, выдерживают 1-2 часа в хромовой смеси (в 1 л воды вносят 50 г бихромата калия и 100 г технической серной кислоты), после чего ополаскивают теплой водой и спиртом. Можно также кипятить стекла в течение 15 мин. в растворе соды или мыльной воды. Для проверки чистоты стекла на его поверхность наносят каплю воды. При достаточном обезжиривании капля растекается равномерно и не собирается в выпуклые, медленно высыхающие пузырьки. Берут стекла пинцетом или аккуратно за грани, так как пальцы оставляют на поверхности жирные пятна. Приготовление фиксированных препаратов ведут в следующей последовательности: 1. На середину чистого обезжиренного предметного стекла стерильной петлей наносят небольшую каплю воды. В нее вносят исследуемый материал, отобранный по методике, описанной в разделе 2.2.1. Полученную суспензию равномерно распределяют по поверхности стекла тонким слоем таким образом, чтобы препарат распределился на площади примерно 2…3 см2. 2. Полученный мазок высушивают при комнатной температуре на воздухе. 3. Производят фиксацию мазка. Для этого стекло с высохшим мазком проводят 3-4 раза над пламенем горелки той стороной, где мазок отсутствует. Цель фиксации: - умертвить клетки микроорганизмов и сделать их безопасными (что особенно важно при работе с патогенными микроорганизмами); - зафиксировать (закрепить) мазок на стекле (чтобы они не смывались при окрашивании); - улучшить окрашивание, поскольку мертвые клетки лучше адсорбируют на своей поверхности различные красители. Приготовление фиксированных препаратов из естественных мест обитания микроорганизмов проводится так же, как и из чистых культур. Помимо термической обработки, применяют также фиксацию химическими веществами: погружают предметное стекло с мазком в мензурку с 96 %-ным этанолом на 15-20 мин, с ацетоном на 5 мин, со смесью 96 % -ного этанола и 40%-ного формалина (соотношение 95:5) на 2 мин. и др.
2.2.3 Окраска фиксированных препаратов микроорганизмов простыми методами Фиксированные препараты нельзя рассмотреть под микроскопом, так как они являются бесцветными и пропускают световые лучи. Поэтому их окрашивают, используя простые или сложные методы. При окрашивании фиксированных мазков простыми методами используют один краситель (фуксин, краска Муромцева, генцианвиолет, метиленовая синь и др.). Последовательность окрашивания мазка простыми методами следующая: 1. На фиксированный препарат наносят несколько капель красителя таким образом, чтобы он покрывал всю поверхность мазка и выдерживают в течение определенного времени. Так, при окраске фуксином на мазок наносят несколько капель красителя и выдерживают его на мазке 2…3 мин. При окрашивании препарата из кефира на него краску Муромцева наносят на мазок через полоску фильтровальной бумаги на 3…5 мин. 2. Краску смывают с мазка слабой струей до бесцветной смывной воды. При этом стекло держат в наклонном положении над лотком. 3. Мазок подсушивают фильтровальной бумагой, которую осторожно прикладывают к стеклу, и досушивают на воздухе. 4. На окрашенный мазок наносят каплю иммерсионного масла и рассматривают препарат с объективом х90 или х100.
Оформление и анализ результатов исследований В отчете студенты должны кратко законспектировать теоретических материал. Наблюдаемые под микроскопом картины нужно зарисовать и сделать заключение о морфологии исследованных чистых культур, а так же микрофлоры кефира и зубного налета. Под рисунками необходимо указать увеличение и подписать название изучаемого объекта.
Контрольные вопросы 1. Каково устройство биологического микроскопа? 2. Из каких частей и механизмов состоит механическая часть микроскопа? 3. Назовите основные характеристики микроскопа. 4. Что понимают под разрешающей способностью микроскопа? Как она определяется? 5. Что составляет оптическую систему микроскопа? 6. Объективы бывают сухие и иммерсионные. Что это значит? 7. Как определяется общее увеличение микроскопа? 8. Что входит в состав осветительной системы микроскопа? 9. Как следует настроить осветительную систему при работе с иммерсионным объективом? 10. Какие существуют правила работы с микроскопом? 11. Какие особенности устройства и принципы работы темнопольного, фазово-контрастного, люминесцентного и электронного микроскопов? 12. Чем определяется четкость получаемого изображения? 13. Перечислить основные правила работы с микроскопом. 14. Как проводится отбор проб чистой культуры микроорганизма? 15. Перечислите основные этапы приготовления фиксированного окрашенного препарата. ЛАБОРАТОРНАЯ РАБОТА №3
ИЗУЧЕНИЕ МОРФОЛОГИИ БАКТЕРИЙ. СЛОЖНЫЕ И ДИФФЕРЕНЦИАЛЬНЫЕ МЕТОДЫ ОКРАСКИ БАКТЕРИЙ
Цель работы: Ознакомиться с морфологическим разнообразием бактерий и основными признаками, используемыми при их идентификации. Изучить различные сложные и дифференциальные методы окраски бактерий и их структур и разобраться в сущности этих методов и цели их использования. Освоить технику окраски бактерий по Граму и спор бактерий по Шефферу-Фултону.
Оборудование, материалы: Микроскоп; бактериологические петли; предметные стекла; спиртовка; иммерсионное масло; фильтровальная бумага; набор красок для окраски по Граму (фильтровальные бумажки с генцианвиолетом, растворы Люголя и фуксина рабочего) и окраски спор по Шефферу-Фултону (растворы бриллиантовой зелени и сафранина); 96 %-ный этиловый спирт: лоток с рельсами для предметных стекол; промывалка; чистые культуры бактерий: Staphylococcus albus; Sarsina flava; Escherichia coli; Bacillus subtilis.
КРАТКИЕ ТЕОРЕТИЧЕСКИЕ ПОЛОЖЕНИЯ
Основные признаки, используемые при идентификации микроорганизмов Определение систематической принадлежности микроорганизмов – сложная задача, требующая длительных наблюдений, значительного количества специфических исследований и биохимических анализов. При идентификации микроорганизмов учитывают: - морфолого-цитологические признаки. К ним относятся строение, форма и размеры клеток, их взаимное расположение, тинкториальные свойства (особенности при окрашивании различными красителями), способность к образованию спор и капсул, подвижность, наличие жгутиков, образование в клетках некоторых включений, особенности размножения; - физиолого-биохимические признаки. При изучении физиолого-биохимических признаков устанавливают отношение микроорганизмов к различным источникам углерода и азота, потребность в кислороде, температурные границы роста, солеустойчивость, чувствительность к антибиотикам, ферментативные тесты; - культуральные признаки. К таким признакам относятся особенности роста микроорганизмов на плотных и жидких питательных средах. При идентификации бактерий рекомендуется также учитывать дополнительные признаки: серологические свойства, фагоустойчивость, химический состав клеточных стенок, содержание отдельных нуклеотидов в нуклеоиде (единственной хромосоме бактерий – молекуле ДНК, состоящей из двух спирально закрученных цепочек нуклеотидов, замкнутых в кольцо). Чем больше у различных микроорганизмов общих признаков, тем ближе они находятся друг к другу по степени родства. Основными признаками, позволяющими распределить микроорганизмы на группы, являются морфологические признаки, которые легко и достаточно быстро можно определить с помощью микроскопа.
Морфологические признаки бактерий Бактерии объединяют обширную группу в основном одноклеточных микроорганизмов, разнообразную по форме, размерам и обмену веществ. Они являются прокариотными микроорганизмами. При дифференциации бактерий путем микроскопии учитывают размеры и формы клеток, их взаимное расположение, химический состав и строение клеточных стенок, способность образовывать споры и капсулы, подвижность. Основными формами бактерий, которые присутствуют в пищевом сырье, а также в продуктах растительного и животного происхождения, являются сферические бактерии (кокки) и палочковидные бактерии (палочки). К основным морфологическим признакам кокков относятся их размеры (диаметр кокков в среднем составляет 1…2 мкм) и взаимное расположение. Взаимное расположение кокков определяется направлением образования перегородок при делении клеток. Если после деления клетки расходятся и располагаются поодиночке, то такие формы называются монококками или микрококками. Если при делении образуются скопления, напоминающие виноградные грозди, их относят к стафилококкам. Кокки, остающиеся после деления в одной плоскости связанными парами, называются диплококками, а образующие разной длины цепочки – стрептококками. Сочетания из четырех кокков, появляющиеся после деления клетки в двух взаимно перпендикулярных плоскостях представляют собой тетракокки. Если кокки делятся в трех взаимно перпендикулярных плоскостях, то они образуют скопления кубической формы - сарцины. Как выглядят различные скопления кокков под микроскопом изображено на рис. 3.
Рис. 3 Взаимные расположения кокков: а - микрококки; б - диплококки; в - стрептококки; г - тетракокки; д - стафилококки; е - сарцины Основными морфологическими признаками палочковидных бактерий, которые определяются путем микроскопии, являются размеры палочек (средняя длина палочек – 2…7 мкм, диаметр в поперечнике - 0,5…1 мкм), взаимное расположение клеток, способность образовывать споры, подвижность. Палочковидные бактерии могут располагаться поодиночке, попарно (диплобактерии) и цепочками (стрептобактерии). При микроскопии легко можно определить спорообразующие и не спорообразующие формы палочковидных бактерий. Вегетативные клетки хорошо адсорбируют красители на своей поверхности и полностью окрашиваются. Оболочка споры малопроницаема, краски в них почти не проникают и под микроскопом споры имеют вид округлых или овальных блестящих зерен. Палочки, образующие споры называются бациллами и клостридиями. У бацилл размер споры не превышает ширину клетки и поэтому при образовании споры форма клетки не меняется. У клостридий диаметр споры больше толщины клетки и поэтому при созревании споры клетка приобретает форму веретена (если спора располагается в центре клетки) или барабанной палочки (если спора располагается на одном из полюсов клетки). На рис. 4 представлены морфологические разновидности палочковидных бактерий.
Рис. 4 Морфология палочковидных бактерий: а - диплобактерии; б - стрептобактерии; в - бациллы; г - клостридии
При идентификации палочек диагностическое значение имеют также расположение спор в клетках бацилл и клостридий, наличие и расположение жгутиков, способность образовывать капсулы.
3.2.3 Сложные и дифференциальные методы окраски бактерий
Различают простые, сложные и дифференциальные методы окраски бактерий. При простой окраске используют один краситель и прокрашивают всю клетку. Сложное окрашивание предусматривает применение двух или нескольких красителей (например, при определении отношения бактерий к окраске по Граму). Дифференциальное окрашивание основано на индивидуальном отношении биологических структур клетки к различным красителям (окраска спор, оболочки, капсул, метахроматина и др.). При этом так же, как и в сложных методах, как правило, используется несколько красителей. Сложные методы окраски позволяют распределить бактерии на группы, что имеет важное диагностическое значение при их идентификации. Среди сложных методов наиболее широкое применение нашел метод окраски бактерий по Граму, позволяющий разделить бактерии в зависимости от химического состава и структуры клеточной стенки на две основные группы - грамположительные (грам+; Г+) и грамотрицательные (грам-; Г-). Грамположительные бактерии по этому методу окрашиваются в сине-фиолетовый цвет, а грамотрицательные – в розовый. К сложным методам относится и метод окраски по Цилю-Нильсену, позволяющий дифференцировать бактерии на две группы по кислотоустойчивости. Этот метод позволяет выявить туберкулезную палочку, бактерии паратуберкулезного энтерита крупного рогатого скота и другие кислотоустойчивые микроорганизмы. При использовании дифференциальных (специальных) методов можно окрасить споры, определить наличие в клетках запасных питательных веществ, выявить клеточные структуры. При окраске спор, например, можно использовать различные методы (методы Шеффера-Фултона, Пешкова, Златогорова, Меллера и др.), основанные на разрыхлении малопроницаемой для красителей оболочки спор различными способами (путем нагревания, обработки препарата кислотами, щелочами) с одновременным или дальнейшим их окрашиванием концентрированным красителем. После такой обработки препарат промывают водой (при этом клетки обесцвечиваются, а споры остаются окрашенными) и докрашивают вегетативные клетки красителем контрастного цвета. Большое значение с диагностической точки зрения имеет окрашивание капсул. Капсульные вещества слабо окрашивается и при простом методе окраски выступает в виде бледной каймы бесцветного или слабоокрашенного ореола вокруг микробной клетки. Для того чтобы лучше рассмотреть капсулы, используют методы Михина, Муромцева, Ольта, Бурри-Гинса и др. В этих методах используют один или несколько красителей. Так, для окраски капсул по Бурри-Гинсу, суспензию слизеобразуюших бактерий смешивают на краю предметного стекла с каплей туши и с помощью другого предметного стекла распределяют тонким слоем по поверхности. Далее препарат фиксируют над пламенем горелки и окрашивают фуксином или сафранином. При микроскопии такого препарата на темном фоне отчетливо выделяются окрашенные в красный цвет бактерии, окруженные бесцветными капсулами. С другими специальными методами, позволяющими определить наличие и содержание запасных веществ в клетках (определение гликогена и волютина), студенты ознакомятся при исследовании качества производственных дрожжей (лабораторная работа №6).
ПОРЯДОК ВЫПОЛНЕНИЯ РАБОТЫ
На занятии студенты знакомятся с основными признаками, которые учитываются при идентификации микроорганизмов, обращают внимание на морфологические признаки кокков и палочек, диагностическое значение сложных и дифференциальных методов окраски бактерий. Осваивают технику окраски бактерий по методу Грама. Определяют, какие из представленных для исследования бактерии относятся к грамположительным, а какие к грамотрицательным. Готовят фиксированный мазок из чистой культуры спорообразующих бактерий Bacillus subtilis и окрашивают его по Шефферу-Фултону.
3.2.1 Окраска бактерий по методу Грама
Сущность метода заключается в различии химического состава и строения клеточной стенки грамположительных и грамотрицательных бактерий. Клеточная стенка грам+ бактерий толстая, но однослойная, содержит много пептидогликана – муреина, а также тейховые кислоты, которые образуют прочное соединение с красителями - генцианвиолетом и йодом и поэтому остаются окрашенными после обработки мазка спиртом. Таким образом, грам+ бактерии по методу Грама окрашиваются в сине-фиолетовый цвет. У грам - бактерий клеточная стенка тонкая, но двухслойная. Муреина мало, причем он содержится во внутреннем слое клеточной стенки, тейхоевые кислоты отсутствуют. Внешний слой клеточной стенки содержит, главным образом, вещества, обладающие гидрофобными свойствами – липополисахариды и липопротеиды. Эти вещества не образуют прочного комплекса с красками генцианвиолетом и йодом и поэтому клетки обесцвечиваются после обработки 96 %-ным этиловым спиртом и после дополнительной окраски красителем фуксином окрашиваются в бледно-розовый цвет. Техника окраски по Граму 1. На предметном стекле готовят фиксированный мазок исследуемой чистой культуры; 2. Мазок окрашивают красителем генцианвиолетом через полоску фильтровальной бумаги. Можно также использовать заранее приготовленные фильтровальные бумажки, смоченные 1 %-ным спиртовым раствором кристаллвиолета и высушенные (метод Грама в модификации А.В. Синева). В этом случае бумажки помещают на фиксированный мазок и смачивают несколькими каплями воды. Окраску препарата проводят в течение 2…3 мин; 3. Фильтровальную бумагу снимают с мазка, краску сливают и наносят на мазок раствор Люголя на 2 мин; 4. Раствор Люголя сливают с мазка и обрабатывают 96 %-нам спиртом в течение 30…60 сек. Затем препарат промывают водой и подсушивают фильтровальной бумагой; 5. Мазок окрашивают красителем фуксином 2…3 мин, второй раз промывают водой и подсушивают фильтровальной бумагой. Затем на стекло наносят каплю иммерсионного масла и рассматривают препарат с объективом х90 или х100 при максимальном освещении.
3.2.2 Окраска спор бактерий по Шефферу-Фултону
Сущность метода заключается в комбинированном действии концентрированного раствора красителя бриллиантового зеленого и температуры на малопроницаемую оболочку спор с дальнейшим обесцвечиванием цитоплазмы вегетативной клетки и ее контрастным докрашиванием сафранином. Таким образом, споры окрашиваются в зеленый цвет, а клетки – в красный. Техника окраски по Шефферу-Фултону 1. На краю предметного стекла (на расстоянии примерно 1,5-2,0 см от края) готовят густой нефиксированный мазок из чистой культуры спорообразующих бактерий; 2. На раствор наносят водный раствор бриллиантовой зелени, и мазок с краской нагревают над пламенем горелки до появления пара. Нельзя допускать прикипания краски к мазку. Поэтому препарат периодически отстраняют от пламени. Нагревание мазка с краской проводят в течение 3 мин; 3. Краску сливают, препарат быстро промывают водой и просушивают фильтровальной бумагой; 4. Окрашивают мазок раствором сафранина 2…3 мин, затем краску сливают, мазок вторично промывают водой и подсушивают фильтровальной бумагой. Далее на мазок наносят каплю иммерсионного масла и рассматривают под объективом на х90 или х100 при максимальном освещении.
Оформление и анализ результатов исследований В отчете студенты кратко конспектируют теоретический материал и переписывают сущность и технику окраски бактерий по Граму и спор бактерий по Шефферу-Фултону. Зарисовывают микроскопические картины исследованных чистых культур бактерий с учетом морфологических особенностей каждого микроорганизма. Под каждым рисунком подписывают латинское название микроорганизма, отношение его к окраске по Граму, увеличение исследованного объекта. Контрольные вопросы 1. Какие признаки учитывают при идентификации микроорганизмов. Какие признаки являются основными при дифференциации бактерий? 2. Как провести дифференциацию кокковых форм бактерий по их взаимному расположению? 3. Каким образом можно провести дифференциацию палочковидных бактерий по их внешнему виду? 4. Каково назначение сложных методов окраски бактерий? Какие сложные методы окраски бактерий Вам известны? 5. Для чего используются дифференциальные (специальные) методы окраски бактерий? Привести примеры. 6. В чем заключается сущность метода окраски бактерий по Граму? 7. Каким образом проводят окрашивание фиксированных препаратов бактерий по методу Грама? 8. В чем заключается сущность метода окрашивания бактериальных спор по Шефферу-Фултону? 9. Какова техника окраски спор бактерий по методу Шеффера-Фултона? 10.Какими методами можно выявить капсулы у бактерий? Как осуществляют окраску капсул по Бурри-Гинсу?
ЛАБОРАТОРНАЯ РАБОТА №4
ИЗУЧЕНИЕ МОРФОЛОГИЧЕСКИХ И КУЛЬТУРАЛЬНЫХ ПРИЗНАКОВ МИКРОСКОПИЧЕСКИХ ГРИБОВ И ДРОЖЖЕЙ. ПРИГОТОВЛЕНИЕ ПРЕПАРАТОВ «РАЗДАВЛЕННАЯ КАПЛЯ»
Цель работы: Ознакомиться с морфологическими особенностями грибов и дрожжей, встречающихся при производстве пищевых продуктов. Освоить технику микроскопического исследования грибов и дрожжей в препаратах «раздавленная капля».
Оборудование, материалы: Микроскоп; препаровальные иглы и бактериологические петли; предметные и покровные стекла; фильтровальная бумага; спиртовка; лоток с рельсами для предметных стекол; культуры грибов родов Mucor, Aspergillus, Penicillium, Alternaria; чистая культура дрожжей Saccharomyces cerevisiae.
КРАТКИЕ ТЕОРЕТИЧЕСКИЕ ПОЛОЖЕНИЯ
Морфология и культуральные признаки микроскопических грибов Микроскопические грибы относятся к надцарству эукариот, царству грибов, отделу истинных грибов и являются представителями трех из четырех классов: фикомицетов, аскомицетов и дейтеромицетов. Представители царства грибов являются аэробными микроорганизмами и по типу питания относятся к хемоорганогеторотрофам. Большинство грибов – сапрофиты, но некоторые вызывают заболевания и являются паразитами. Вегетативное тело грибов называется мицелием. Мицелий состоит из множества переплетающихся нитей-трубочек, называемых гифами. Диаметр гифов, колеблется от 5 до 50 мкм. В зависимости от строения мицелия грибы делятся на высшие и низшие. У высших грибов гифы разделены перегородками (септами) в центре которых имеется большая пора. В класс фикомицетов объединяются низшие грибы, представители классов аскомицетов и дейтеромицетов являются высшими грибами. Грибы – это циноцитные микроорганизмы. Это значит, что они растут и при этом происходят деления ядер, но не происходит клеточных делений. Таким образом, вегетативное тело гриба представляет собой одну большую многоядерную клетку. Все микроскопические грибы могут размножаться вегетативно кусочком мицелия. При бесполом размножении у фикомицетов образуются спорангиеносцы, а у аскомицетов – конидиеносцы. Дейтеромицеты могут размножаться многоклеточными конидиями. Фикомицеты и аскомицеты являются совершенными грибами. Это значит, что представители этих классов могут размножаться половым путем. Дейтеромицеты относятся к несовершенным грибам. Культуральные признаки микроскопических грибов Колонии микроскопических грибов по размерам во много раз превосходят колонии одноклеточных организмов (бактерий, грибов) и нередко разрастаются по всей поверхности питательной среды в чашках Петри. Консистенция грибных колоний различная. Чаще образуются войлокообразные и кожистые колонии, реже крошковатые. Поверхность колоний может быть пушистой, как вата, бархатистой, мучнистой, паутинообразной, нитевидной, кожистой или гладкой. При росте на плотных и жидких средах часть гифов врастает в питательную среду, образуя субстратный мицелий, а другая часть гифов образует воздушный мицелий в виде пушистого налета, видимого невооруженным глазом. Мицелий может быть также бесцветным (белым, сероватым) или окрашенным (черным, бурым, зеленым, желтым и т.д.). Пигментирован только плодоносящий мицелий. Характеристика микроскопических грибов различных классов Морфологические особенности грибов различных классов представлены на рис. 5. Род Mucor относится к классу фикомицетов. Эти грибы имеют несептированный мицелий. Они могут размножаться бесполым и половым путем с образованием спорангиеносцев (рис. 5). Снаружи спорангий покрыт тонкими шипами из кристаллов щавелевокислого кальция. При созревании спорангий разрывается, спорангиеспоры высвобождаются и разносятся воздушными потоками. На спорангиеносце после освобождения спорангия от спор остается колонка, а в нижней ее части – воротник. Цвет мицелия мукоровых грибов вначале белый, затем серовато-оливковый, вид – войлокоподобный.
Рис. 5 Морфологические особенности грибов различных классов: а - Mucor; б - Penicillium; в - Aspergillus; г - Alternaria
Мукоровые грибы растут на поверхности влажного зерна, солода, корнеплодов, на пищевых продуктах, на стенах сырых помещений в виде сероватого пушистого налета. Mucor nigricans является возбудителем кагатной гнили сахарной свеклы. Многие мукоровые грибы используются в промышленности для производства различных органических кислот и спирта (грибы видов Mucor javanicus, Mucor racemosus), ферментных препаратов, каротиноидов, стероидов. Представители родов Aspergillus и Penicillium относятся к классу аскомицетов, который объединяет высшие микроскопические совершенные грибы. При бесполом размножении с помощью спор эти грибы образуют конидиеносцы (рис. 5). Аспергиллы и пенициллы относятся к плодосумчатым грибам. Это значит что при половом размножении у них на специальных плодовых телах образуются аски (сумки), в которых находятся 8 аскоспор. К роду Penicillium относится около половины всех плесневых грибов. Они широко распространены в почве, в воздухе плохо проветриваемых помещений и вызывают порчу различных продуктов и материалов. Этот гриб имеет ветвящийся септированный мицелий (диаметр гифов – 2…3 мкм) и септированные конидиеносцы (напоминают кисточки), которые на конце разветвляются в виде отростков – стеригм. От них отходят конидии, состоящие из цепочек спор. В зависимости от вида конидии могут быть разного цвета (белые, зеленые и др.). Многие пенициллы используются в промышленности для получения различных ценных продуктов. Среди выделенных штаммов этого рода 25 % обладают антибиотической активностью, а такие виды как Penicillium notatum, Penicillium chrysogenum используются как продуценты пенициллина. Некоторые виды пенициллов используются как продуценты ферментов и липидов. В производстве мягких сыров рокфор и камамбер используются благородные плесени Penicillium roqueforti и Penicillium camamberti. Грибы рода Aspergillus насчитывают более 200 видов. Эти грибы имеют хорошо развитый ветвящийся мицелий с многочисленными септами. Конидиеносцы несептированы, верхние их концы грушевидно или шаровидно расширены в виде небольшой головки. На головке располагаются кеглеобразные стеригмы с цепочками конидий, которые напоминают струйки воды, выливающиеся из лейки. Отсюда возникло название «леечная плесень» (aspergere по латыни – поливать, опрыскивать). Конидии аспергиллов при созревании приобретают различную окраску, что наряду с другими признаками определяет их видовую принадлежность. Так же как и пенициллы, представители рода Aspergillus широко распространены в природе и играют важную роль в минерализации органических веществ. Они вызывают плесневение многих пищевых продуктов. Эти грибы являются продуцентами многих ценных веществ и широко используются в промышленности. Так, Aspergillus niger, применяют в промышленности для производства лимонной кислоты; Aspergillus terreus – итаконовой кислоты Aspergillus flavus и Aspergillus terricola образуют наиболее активный комплекс протеолитических ферментов; Aspergillus oryzae и Aspergillus awamori являются лучшими продуцентами амилолитических ферментов. Грибы рода Alternaria относятся к классу несовершенных грибов – дейтеромицетов. Это высшие грибы. Они имеют септированный мицелий и короткие несептированные конидиеносцы, на которых находятся многоклеточные конидии грушевидной или лимоновидной формы (рис. 5). Гриб является возбудителем черной гнили – болезни корнеплодов и плодов, а также возбудителем порчи пищевых продуктов.
Морфология дрожжей и их характеристика Дрожжи – это высшие одноклеточные грибы. Большинство дрожжей относится к двум классам грибов – аскомицетам и дейтеромицетам. Дрожжи по отношению к кислороду делятся на факультативные анаэробы (в аэробных условиях осуществляют дыхание и активно накапливают биомассу, а в анаэробных условиях вызывают спиртовое брожение) и аэробы. Морфологически дрожжи разнообразны. Они отличаются друг от друга размерами и формой клеток. Размеры клеток дрожжей в зависимости от вида варьируют в следующих пределах; от 2,5 до 10 мкм в поперечнике и от 4 до 20 мкм в длину. Морфологическое разнообразие форм дрожжей изображено на рис. 6. |
|||||||||||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 328. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |

 р
р



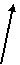










 a 2
g
a 2
g
 3
3

 4
5
4
5

 р1
р1

 а
а
 б
б
 в
в
 г
г