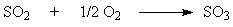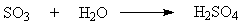Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Физико-химические основы производстваСтр 1 из 2Следующая ⇒ Серная кислота находит разнообразное применение в нефтяной, металлургической и других отраслях промышленности. Она широко используется в производстве различных солей и кислот, всевозможных органических продуктов, красителей, дымообразующих и взрывчатых веществ и др. Применяется в качестве водоотнимающего и осушающего средства, используется в процессах нейтрализации, травления и многих других. Одно из основных применений серной кислоты — это производство фосфорных и некоторых азотных удобрений (суперфосфат, преципитат, аммофос, сульфат аммофоса и другие). Наполучение 1 т. Р2О5 в концентрированных фосфорных удобрениях расходуется 2,2 – 2,5 т, а на получение 1 т. сульфата аммония – 0,75 т серной кислоты. Много кислоты расходуется на очистку нефтепродуктов от ненужных примесей. Сернокислотной обработке подвергается большая часть бензина и смазочного масла. Серная кислота отработанная (отход) применяется в химической, металлургической, деревообрабатывающей и других отраслях промышленности. Серная кислота аккумуляторная применяется в производстве свинцово-кислотных источников тока. В России основное количество серной кислоты получают из железного колчедана. Сжигают FeS2 в печах, где он находится в состоянии кипящего слоя. Свыше 1500 промышленных установок во всем мире вырабатывают этот ценнейший продукт химической промышленности. Мировое производство серной кислоты достигает примерно 150 млн.т. в год. Производят серную кислоту двумя способами: контактным и нитрозным (башенным). Оба метода имеют свои достоинства и недостатки. Но в современное время контактный метод вытесняет нитрозный. Это обусловлено тем, что благодаря усовершенствованию контактного способа производства себестоимости более чистой и высококонцентрированной контактной серной кислоты выше, чем башенной. Поэтому строят в России в основном контактные цехи. В настоящее время свыше 90% всей кислоты производится контактным способом.  Поэтому производство серной кислоты из колчедана контактным методом является основным производством и будет рассмотрено в данной работе.
2. Характеристика сырья и готового продукта В данной работе рассматривается получение серной кислоты из железного колчедана. Железный колчедан. Основные константы: Молекулярный вес: 119,975 Температура плавления (размягчения) °С: 642 Плотность, г/см3: Чистого: 5,02; Природного: 4,9 – 5,2 В соответствии с ГОСТ 444-75 «Колчедан серный флотационный», в зависимости от массовой доли сульфидной серы устанавливают 5 марок флотационного серного колчедана. По физико-химическим показателям флотационный серный колчедан должен соответствовать нормам, указанным в таблице 1. Таблица 1. Физико-химические показатели серного колчедана
Флотационный колчедан получается как отход при флотационном обогащении сернистых руд содержащих медь. Главной составной частью железного колчедана является сульфид железа (II), содержащий 53,46% серы и 46,54% железа. Сернокислотное производство потребляет следующие виды колчедана: рядовой, флотационный и углистый. Рядовой колчедан добывается непосредственно из его залежей попутно при разработке комплексных сульфидных руд.Практически в добываемом рядовом колчедане содержится от 25 до 52% серы и от 35 до 44% железа. Содержание других примесей в рядовом колчедане различных месторождений колеблется в больших пределах. К основным примесям относятся: сернистые соединения меди, цинка, свинца, мышьяка, никеля, кобальта, селена, теллура; углекислые и сернокислые соли кальция, магния и др.; тальк, кварц и часто в незначительных количествах серебро и золото. К железному колчедану по свойствам близки пирротины, в состав которых входят сернистые соединения железа типаFenSn+1. Cодержание серы в пирротинах (например, карело-финских месторождений) колеблется от 32 до 40%. Температура воспламенения железного колчедана около 400 °С. Температура воспламенения колчедана зависит от его химического состава и размера частиц. Флотационный колчедан получается в виде отходов при обогащении руд цветных металлов (меди, цинка и др.) и называется также флотационными хвостами. Физические свойства флотационных колчеданов зависят от их химического и гранулометрического состава, а также от влажности. Серная кислота H2SO4 Основные константы: Молекулярный вес: 98,078 Плотность при 20 °С, г/см3: 1,8305 Температура плавления 100%, %: 10,37±0,05 Температура кипения, °С:100%: 275±5; 98,479%: 326±5 В соответствии с ГОСТ 2184-77 «Кислота серная техническая.Технические условия», по физико-химическим показателям серная кислота должна соответствовать нормам, указанным в таблице 2. Таблица 2. Физико-химические показатели серной кислоты
Серная кислота обладает типичными свойствами сильных кислот, а также окислительным, водоотнимающим и сульфирующим действием. Серную кислоту следует рассматривать как соединение одной молекулы ангидрида серной кислоты SO3 с одной молекулой воды; следовательно, безводная серная кислота содержит 81,63% SO3 и 18,37% Н2О. Безводная серная кислота – тяжелая маслянистая бесцветная жидкость, смешивающаяся с водой и ангидридом серы в любом соотношении. Физические свойства серной кислоты, такие, как плотность, температура кристаллизации, температура кипения, зависят от ее состава. Серная кислота – одна из самых активных неорганических кислот. Она реагирует почти со всеми металлами и их оксидами, вступает в реакции обменного разложения, энергично соединяется с водой, обладает окислительными и другими важными химическими свойствами. Высокая химическая активность серной кислоты обусловила ее широкое применение в различных отраслях промышленности. Физико-химические основы производства Производство серной кислоты включает в себя следующую последовательность стадий: Обжиг железного колчедана.
Окисление диоксида серы.
Абсорбция триоксида серы.
3.1 Физико-химические основы процесса получения сернистого ангидрида Первой стадией процесса является окисление сырья с получением обжигового газа, содержащего диоксид серы. 4FeS2 +11O2 = 2Fe2O3 + 8SO2 Реакция экзотермическая, необратимая, некаталитическая, гетерогенная. При протекании реакции, помимо газообразного продукта реакции SO2 образуется твердый продукт Fe2O3, который может присутствовать в газовой фазе в виде пыли. Поэтому реакционный газ после стадии обжига колчедана должен быть предварительно направлен на стадию подготовки к контактному окислению (вторая стадия). Процессобжига колчедананепрерывный и механизированный. Колчедан подается ленточным транспортером в бункер и из него в печь. Огарок, образующийся в процессе обжига, частично уносится печным газом, частично выводится через боковое отверстие в печи. Желательно эту реакцию проводить при таких условиях, когда содержащаяся в колчедане сера наиболее полно используется для получения SO2 и реакция протекает быстро. Производительность печи растет с увеличением скорости реакции обжига. Этого добиваются, применяя оптимальные условия для данной реакции. Оптимальные условия: 1. t = 800°С. Именно при этой температуре увеличивается число активных молекул, с достаточной кинетической энергиейскорость реакции увеличивается. Но реакция экзотермическая, идет с выделением тепла, а значит, температура будет повышаться и произойдет спекание частиц колчедана. Чтобы избежать этого избыток теплоты отводят. В реакционный аппарат встраивают трубки, по которым пускают холодную воду. Нагреваясь, вода забирает лишнее тепло и превращается в водяной пар, который используется для производства электроэнергии или других целей. 2. Измельчение колчедана. Колчедан перед обжигом измельчают до оптимальных размеров, увеличивая площадь его соприкосновения с кислородом воздуха. Частицы не должны быть крупными иначе они будут обжигаться только на поверхности, а внутри останется непрореагировавший колчедан – это приведет к потерям сырья. Но и слишком мелкими тоже не должны быть, т.к. в этом случае произойдет слеживание, уплотнение слоя, через который кислород почти не проходит и площадь соприкосновения уменьшается, что приведет к уменьшению скорости реакции. 3. Обогащение воздуха кислородом. Таким образом, увеличивается концентрация одного из реагирующих веществ, что также способствует увеличению скорости реакции. 4. Противоток пирита и воздуха. Чтобы увеличить скорость обжига используют принцип противотока – сверху в печь подают измельченный пирит, а снизу - воздух, обогащенный кислородом. 5. Обжиг пирита в «кипящем слое». Частицы оказываются в подвешенном состоянии, создавая иллюзию кипящей жидкости. Поэтому такой слой мелких частиц называется – кипящим. Таким образом, увеличивается площадь соприкосновения пирита и кислорода, каждая твердая частица омывается воздухом увеличивается скорость реакции. 6. Теплообмен. Промежуточными стадиями являются очистка, осушение, теплообмен. Колчедан, применяемый для обжига, предварительно обогащают флотацией. Флотационный колчедан, кроме FeS2 содержит ряд примесей (в частности, соединения мышьяка, селена, теллура, фтора), которые при обжиге переходят в состав обжигового газа в виде оксидов As2O3, SeO2, TeO2 и фторосодержащих газообразных соединенийHF, SiF4. Наличие этих соединений обуславливает необходимость последующей очистки газа. 3.2 Физико-химические основы процесса очистки Перед подачей обжигового газа в контактный аппарат необходимо отделить примеси, являющиеся ядами для контактной массы (мышьяк, фтор), или примеси, присутствие которых при контактировании нежелательно (пыль, пары воды), а также извлечь ценные металлы (селен, теллур и др.). Поэтому вначале необходимо этот газ очистить от пыли. Это осуществляется при помощи 2 аппаратов: циклона и электрофильтра. Вначале газ направляют на очистку от крупной пыли в циклон. Он состоит из двух цилиндров, вставленных один в другой. Газ подается сбоку в наружный цилиндр и перемещается сверху вниз по спирали. Под действием центробежной силы частицы пыли отбрасываются к стенкам наружного цилиндра и падают в бункер, откуда затем удаляются. Очищенный газ по внутреннему цилиндру из аппарата уходит. Циклон не очищает газ от мелких пылинок. От мелкой пыли газ очищают в электрофильтре. Он состоит из мелких сеток, между которыми протянута проволока. К ней подведен ток высокого напряжения(60000 В). При этом проволока заряжается «-», сетки «+». Газ поступает в камеру снизу. Под действием сильного электрического поля частицы пыли ионизируются и притягиваются к сеткам. Там они теряют свой заряд и падают вниз, в специальный бункер. Но газ еще насыщен водяным паром, поэтому далее его направляют в сушильную башню. Сушильная башня заполнена керамическими кольцами, чтобы увеличить площадь соприкосновения газа и концентрированной серной кислоты. Сернистый газ поступает в башню снизу, а сверху разбрызгивается концентрированная серная кислота (принцип противотока). Кислота, стекая по кольцам вниз, образует на их поверхности пленку. При этом площадь соприкосновения кислоты и газа многократно увеличивается. Очищенный газ подогревают в теплообменнике, используя тепло II стадии процесса: газовую смесь перед началом реакции окисления сернистого газа нужно нагреть. Поэтому перед контактным аппаратом помещают теплообменник. Горячий газ из контактного аппарата пропускают по трубам теплообменника, а между ними в противоположном направлении пропускают подогреваемую смесь газов и происходит теплообмен между продуктами реакции и исходными веществами, поступающими в контактный аппарат. Оксиды селена (Se) и мышьяка (As) присутствуют в обжиговом газе в виде паров. При понижении температуры газовой смеси в промывных башнях пары мышьяковистого и селенистого ангидридов тумана не образуют. Присутствующие в обжиговом газе фтористый водород HF и четыреххлористый кремний SiFe4 по-разному отмываются серной кислотой. HF плохо растворяется в кислоте. Лишь при концентрации H2SO4 более 95% и температуре ниже 800°С растворимость HF возрастает настолько, что очистка газа возможна до содержания в нем HF 3 мг/м3. SiFe4 хорошо растворяется в серной кислоте при концентрации менее 60% H2SO4. Если в газе присутствует большое количество фтористого водорода, разрушаются футеровка и насадки промывных башен в результате взаимодействия HF с кремнеземом, входящим в состав футеровочных материалов и насадки. Поэтому при использовании серного сырья, содержащего много фтора, футеровки и насадки должны быть выполнены из графитовых материалов, иначе фтор необходимо выводить из системы каким-либо способом. Осушка обжигового газа – это очистка его от паров воды. Хотя пары воды безвредны для контактной массы, присутствие их в газе, поступающем на абсорбцию серного ангидрида, приводит к образованию тумана в абсорбционном отделении. При этом уменьшается коэффициент использования серы, значительное количество ее оказывается в выбросах. Поэтому пар перед абсорбцией очищают от паров воды. Для этого газ направляют в сушильную башню с керамической насадкой, орошаемой концентрированной серной кислотой. Содержание паров воды в газе, поступающем в сушильную башню, определяется температурой газа после увлажнительной башни. На выходе из сушильной башни содержание влаги не должно превышать 0,08 г/м3. Температуру газа перед сушильными башнями поддерживают такой, чтобы содержание влаги в газе не превышало количества воды, необходимого для образования в абсорберах серной кислоты заданной концентрации. 3.3 Физико-химические процессы окисления сернистого ангидрида до серного Процесс окисления сернистого ангидрида до серного протекает по реакции: 2SO2+O2↔SO3+ΔH, где ΔH – тепловой эффект реакции. Процесс окисления SO2 проводят на ванадиевом катализаторе при высокой температуре. При этом нагревание газа до заданной температуры связано с большими затратами топлива, поэтому на практике поступают следующим образом. Нагревают газ до температуры, при которой процесс начинает протекать в достаточной для практических целей скоростью и направляют его на первый слой катализатора. При окислении SO2 выделяется тепло, за счет которого повышается температура газа по прямолинейному закону. Скорость реакции повышается с ростом концентрации кислорода, поэтому процесс в промышленности проводят при его избытке. Процесс проводят в контактном аппарате, представляющем собой цилиндр. В нем, на специальных полках, слоями размещен катализатор (V2O5). Между полками с катализатором размещаются трубки теплообменника. При этом одновременно решается проблема нагревания сернистого газа и охлаждения до необходимой температуры серного газа (принцип теплообмена). Оптимальные условия: 1. t= 400 – 500 °С.Так как реакция окисления SO2 относится к типу экзотермических, температурный режим ее проведения должен приближаться к линии оптимальных температур. На выбор температурного режима дополни- тельно накладываются два ограничения, связанные со свойствами катализатора. Нижним температурным пределом является температура зажигания ванадиевых катализаторов, составляющая в зависимости от конкретного вида катализатора и состава газа 400-440 °C. Верхний температурный предел составляет 600-650 °C и определяется тем, что выше этих температур происходит перестройка структуры катализатора и он теряет свою активность. 2. Повышение давления. Увеличение давления оказывает на реакцию превращения SO2 в SO3 благоприятное действие, поскольку в результате реакции из 1 ½ молекулы получается одна, т.е. происходит сокращение объема. 3. Окисление в «кипящем слое» катализатора. Реакция окисления SO2 до SO3 идет в присутствии катализатора. Ранее в качестве катализатора при получении контактной серной кислоты применяли платину. Теперь она полностью вытеснена ванадиевым катализатором, более дешевым и менее чувствительным к ядам (мышьяк, селен, хлор и др.). 4. Состав газа. Состав газа также влияет на реакцию окисления SO2 до SO3, а именно: понижение концентрации сернистого ангидрида и увеличение концентрации кислорода повышает степень превращения SO2 в SO3. 3.4 Физико-химические процессы абсорбции серного ангидрида Абсорбция серного ангидрида из газовой смеси – последняя стадия процесса получения контактной серной кислоты. nSO3 + H2O = H2SO4 + (n-1)SO3+Q, если n> 1, то получается олеум (раствор SO3 в 100 % H2SO4), если n = 1 , то получается моногидрат (98,3% H2SO4), если n< 1, то получается разбавленная серная кислота. Процесс осуществляют в специальныхпоглотительных башнях, по устройству напоминающих сушильные. При этом используют принцип противотока – пары серного ангидрида подаются снизу, а навстречу ему сверху течет серная кислота. Оптимальные условия: 1. t до 300 °С. Повышение температуры также снижает степень абсорбции. 2. Противоток газа и кислоты 3. Использование 98% серной кислоты. Серный ангидрид полнее всего поглощается 98,3% серной кислотой. Если серная кислота более разбавлена, то над ней в газовой фазе есть пары воды. Часть серного ангидрида соединяется с этими парами, образуя пары серной кислоты, которые при охлаждении конденсируются с образованием сернокислотного тумана. Осушенный газ, содержащий SO3, проходит последовательно олеумный и моногидратный абсорберы, орошаемые кислотой. Серный ангидрид поглощается из газа этой кислотой, а остальная часть газа выбрасывается в атмосферу. Тепло реакции, выделяющееся при абсорбции и поглощаемое орошаемой кислотой, отводится в холодильники. Вывод продукционной серной кислоты в контактной системе производят в виде олеума из олеумного абсорбера и в виде контактной кислоты. Для этого в одной из сушильных башен поддерживают концентрацию кислоты, соответствующую стандартным требованиям на контактную техническую серную кислоту, и по мере накопления передают кислоту из сборника на склад. Сернокислотные заводы способны нанести серьезный ущерб окружающей среде. Во избежание этого отходящие газы подвергают тщательной очистке от следов сернистого газа, серного ангидрида и других вредных примесей. С каждым годом проблемам охраны природы уделяется все больше внимания.
4. Выбор и описание технологической схемы производства Для обжига колчедана существуют печи различных конструкций: механические полочные (многоподовые), вращающиеся цилиндрические, печи пылевидного обжига, печи для обжига в кипящем слое. Механические полочные печи довольно просты в обслуживании: колчедан подается и огарок выгружается механически. Механически осуществляется также перемешивание колчедана и передача его со свода на свод. Для печи характерны довольно постоянная концентрация сернистого газа и достаточно высокая степень выгорания серы. Вращающиеся цилиндрические печи. Печи этого типа не получили распространение в нашей стране. Они просты по устройству, в них нет металлических частей, требующих частой замены. Печи КС (для обжига колчедана в кипящем слое). Кипящий слой называют также взвешенным, псевдоожиженным слоем. В настоящее время новые сернокислотные системы оборудуются преимущественно печами КС. Механические печи на действующих заводах постепенно заменяются печами этого типа. Существенными достоинствами метода обжига в печах КС являются: а) возможность получения концентрированного сернистого газа с низким содержанием серного ангидрида и мышьяка в обжиговом газе. б) высокая интенсивность печей. Интенсивность печей КС в 80 раз выше интенсивности механических печей, в 4 раза - печей пылевидного обжига. К недостаткам печей КС следует отнести повышенное содержание пыли в газе обжига, что затрудняет его очистку. Существуют печи КС с одинарным и двойным кипящим слоем. Большой практический интерес представляет печь КС с двумя кипящими слоями ДКСМ (конструкции А. М. Мальца). Ведутся опыты по обжигу колчедана в циклонных печах, в которых подогретый воздух со взвешенным тонкоизмельченным колчеданом подается по касательной (тангенциально) с большой скоростью. Обычно его подают в несколько бункеров ленточным транспортером или элеватором. Из бункера колчедан насыпают в подвесные вагонетки, взвешивают и доставляют к печам. Делают это вручную или с помощью электротяги. Из вагонетки колчедан выгружают в бункер. Применяют различные системы удаления и охлаждения огарка: - при помощи холодильных шнеков. Огарок подают в вагоны или машины-самосвалы для отправки на переработку или в отвал. Достоинство этого способа состоит в простоте устройств и надежности их в работе. Недостаток – испарение большого количества воды, подаваемой на охлаждение. - при помощи холодильно-транспортной трубы, установленной под небольшим углом и вращающейся на роликах. Такие трубы просты и надежны в работе и могут быть установлены около печей с низким фундаментом. - при помощи холодильно-транспортного барабана, представляющего собой вращающийся цилиндр с внутренней винтовой насадкой для передвижения огарка. -скребковым транспортером, состоящим из желоба, по которому движется цепь со скребками, захватывающими огарок. Технологическая схема производства серной кислоты из FeS2 с использованием принципа двойного контактирования показана на рис.1. Колчедан через дозатор подают в печь 1 кипящего слоя. Полученный запыленный обжиговый газ, содержащий 13 % SO2 и имеющий на выходе из печи температуру около 700°С, подают сначала в котел-утилизатор 3, а затем на стадию сухой очистки от огарковой пыли (в циклоны 4 и в сухой электрофильтр 5). В котле-утилизаторе 3 происходит охлаждение газа с одновременным получением энергетического водяного пара (давление 4 МПа и температура 450 °С), который может быть использован как в самой установке для компенсации затрат энергии на работу компрессоров и насосов, так и в других цехах завода. В очистном отделении, состоящем из двух промывных башен 6 и 7, двух пар мокрых электрофильтров 8 и 9 и сушильной башни 10, происходит очистка газа от соединений мышьяка, селена, фтора и его осушка. Первая полая промывная башня 6 работает в испарительном режиме: циркулирующая кислота охлаждает газ, при этом теплота затрачивается на испарение воды из кислоты, поступающей на орошение. Концентрацию орошающей кислоты в первой башне, равную 40-50%-ной H2SO4, поддерживают постоянной путем разбавления 10-15%-ной кислотой из второй промывной башни 7. Кислота из второй башни поступает в сборник 18 и после охлаждения возвращается на орошение.После второй промывной башни газ проходит последовательно две пары мокрых электрофильтров 8 и 9, затем насадочную сушильную башню 10, орошаемую 93-94%-ной серной кислотой при температуре 28- 30°С. Кислота циркулирует между сушильной башней 10 и сборником 18, часть кислоты отводится как готовая продукция на склад. Для поддержания постоянной концентрации H2SO4 в сборник кислоты 18 вводят 98-99%-ную кислоту из моногидратных абсорберов 17 и 20. Для поддержания постоянной температуры на стадии осушки циркулирующую кислоту охлаждают в холодильнике воздушного охлаждения 22. Перед сушильной башней обжиговый газ разбавляют воздухом для снижения в нем концентрации SO2 до 9 % и увеличения избытка кислорода в соответствии с оптимальными условиями окисления диоксида серы. После сушильной башни обжиговый газ проходит через фильтр-брызгоуловитель 11 и поступает в турбогазодувку 12. В теплообменниках 13 газ нагревается за счет теплоты продуктов реакции до температуры зажигания катализатора (420-440°С) и поступает на первый слой контактного аппарата, где происходит окисление 74 % SO2 с одновременным повышением температуры до 600°С. После охлаждения до 465°С газ поступает на второй слой контактного аппарата, где степень превращения достигает 86%, а температура газа возрастает до 514ºС. После охлаждения до температуры 450ºС газ поступает на третий слой контактного аппарата, где степень превращения SO2 увеличивается до 94-94,5 %, а температура повышается до 470°С. Затем реакционный газ охлаждают в теплообменниках 13 до 100°С и направляют на абсорбцию первой ступени: сначала в олеумный абсорбер 21, затем в моногидратный абсорбер 20. После моногидратного абсорбера и фильтра-брызгоуловителя газ вновь нагревают до температуры 430°С и подают на четвертый слой катализатора. Концентрация SO2 в газе составляет теперь 0,75-0,85 %. В четвертом слое происходит окисление остаточного SO2 с конверсией ≈ 80 %, сопровождающееся повышением температуры до 449°С. Реакционную смесь вновь охлаждают до температуры 409°С и направляют на последний (пятый) слой контактного аппарата. Общая степень превращения после пяти стадий контактирования составляет 99,9%. Газовую смесь после охлаждения направляют в моногидратный абсорбер второй ступени абсорбции 17. Непоглощенный газ, состоящий в основном из воздуха, пропускают через фильтр 11 для выделения брызг и тумана и выбрасывают в атмосферу через выхлопную трубу. Производительность установки составляет до 1500 т/сут по моногидрату. Расход на 1 т моногидрата: колчедана 0,82 т, воды 50 м3, электроэнергии 82 кВт -ч. Вредные выбросы сернокислых заводов следует оценивать не только по действию содержащегося в них оксида серы на расположенные вблизи предприятия зоны, но и учитывать другие факторы - увеличение количества случаев респираторных заболеваний человека и животных, гибель растительности и подавление ее роста, разрушение конструкций из известняка и мрамора, повышение коррозионного износа металлов. По вине “кислых” дождей повреждены памятники архитектуры. В зоне до 300 км от источника загрязнения (SO2) опасность представляет серная кислота, в зоне до 600 км - сульфаты. Серная кислота и сульфаты замедляют рост с/х культур. Закисление водоемов - весной при таянии снега, вызывает гибель икр и молоди рыб. Помимо экологического ущерба налицо экономический ущерб - громадные суммы каждый год теряются при раскислении почв. Рассмотрим химические метода отчистки от наиболее распространенных газообразных загрязняющих воздух веществ. Наиболее перспективны методы, основанные на поглощение оксида серы известняком, раствором сульфита - гидросульфита аммония и щелочным раствором алюмината натрия. Интерес также представляют каталитические методы окисления оксида серы в присутствии оксида ванадия. Особое значение имеет очистка газов от фторсодержащих примесей, которые даже в незначительной концентрации вредно влияют на растительность. Выявлены важнейшие тенденции развития производства серной кислоты контактным способом: 1) интенсификация процессов проведением их во взвешенном слое, применением кислорода, производством и переработкой концентрированного газа, применением активных катализаторов; 2) упрощение способов очистки газа от пыли и контактных ядов (более короткая технологическая схема); 3) увеличение мощности аппаратуры; 4) комплексная автоматизация производства; 5) снижение расходных коэффициентов по сырью и использование в качестве сырья серосодержащих отходов различных производств; 6) обезвреживание отходящих газов.
5. Материальные и тепловые расчеты Обжиг колчедана в кипящем слое Исходные данные: -сырье колчедан -производительность печи по колчедану, кг/сут 450000 -массовая доля серы во влажном колчедане, % 44 -влажность колчедана, % 0,7 -объемная доля SO2в сухом газе, % (об.) 14,5 -объемная доля SO3в сухом газе, % (об.) 0,15 -температура воздуха, поступающего печь, К 283 -относительная влажность воздуха, % 70
В материальном и тепловом расчетах буквенные обозначения величин снабжены индексами. Верхние левые цифровые индексы обозначают: 1-условный 45%-ный колчедан; 2-влажный колчедан; 3-сухой колчедан; 4-воздух; 5-двуокись серы в сухом обжиговом газе; 6-серный ангидрид в сухом обжиговом газе; 7-сухой обжиговый газ; 8-влажный обжиговый газ; 9-пыль в обжиговом газе; 10-огарок, удаляемый через спускную трубу; 11-потери тепла в окружающую среду; 12-тепло, отводимое охлаждающими элементами.
Материальный расчет: 1. Расход влажного колчедана: 2m=450000/24=18750 кг/ч 2. Расход сухого колчедана: 3m=18750-(18750*0,7/100)=18619 кг/ч 3. Количество серы в колчедане: 2ms=18619*44/100=8192,3 кг/ч 4. Выход огарка из 1 кг колчедана: Х=(160-44)/(160-0,8)=0,729 кг/кг 5. Суммарный выход огарка и пыли: 9m+10m=18619*0,729=13566 кг/ч 6. Потери серы с огарком: 9ms+10ms=13566*0,8/100=108,6 кг/ч 7. Выгорело серы с колчеданом с образованием SO2и SO3: 5ms+6ms=8192,3-108,6=8083,7 ≈ 8084 кг/ч 8. Образовалось SO2и SO3 по объему: 5v+6v=8084*21,895/32,066=5520 нм3/ч 9. Образовалось SO3: По объему: 6v=5520*0,15/(14,5+0,15)=57 нм3/ч По массе: 6m=57*80,066/22,416=202 кг/ч 10. Содержание серы в SO3: 6ms=202*32,066/22,416=81 кг/ч 11. Использовано серы на образование SO2: 5ms=8084-81=8003 кг/ч 12. Образовалось SO2: По массе: 5m=8003*64,066/32,066=15989 кг/ч По объему: 5v=15989/2,927=5463 нм3/ч 13. Объем полученного сухого обжигового газа: 7v=5463*100/14,5=37674 нм3/ч 14. Кислород в обжиговом газе: Концентрация кислорода в обжиговом газе. Выводим формулу, связывающую концентрацию кислорода в обжиговом газе со следующими параметрами: а) с концентрацией кислорода в дутье; б) с концентрацией SO2и SO3 в обжиговом газе; в) со стехиометрическими отношениями израсходованного числа молей O2к образовавшимся числам молей SO2и SO3. При выводе формулы необходимо особо отметить, что мольные объемы реальныхO2,SO2и SO3 не равны друг другу. Обозначим: n-концентрацияO2 в сухом дутье, % об.; РSO2-стехиометрическое отношение числа израсходованных молей O2к числу молей образовавшегося SO2; РSO3-то же для SO3; KSO2=VO2/VSO2-отношение мольных объемов O2и SO2; KSO3=VO2/VSO3-отношение мольных объемов O2и SO3; На образование 100 объемов сухого обжигового газа уйдет 100-7cSO2+PSO2*KSO2*7cSO2-7cSO3+PSO3*KSO3*7cSO3=100+(PSO2*KSO2-1)* 7cSO2+(PSO3*KSO3-1)* 7cSO3 объемов дутья, в которых содержится n/100[100+(PSO2*KSO2-1)* 7cSO2+(PSO3*KSO3-1)* 7cSO3] объемов кислорода. При образовании SO2и SO3 из указанного количества расходуется PSO2*KSO2*7cSO2+ PSO3*KSO3*7cSO3 объемов кислорода. Оставшийся кислород содержится в 100 объемах обжигового газа. Поэтому 7cO2= n/100[100+(PSO2*KSO2-1)* 7cSO2+(PSO3*KSO3-1)* 7cSO3]- PSO2*KSO2* *7cSO2 - PSO3*KSO3*7cSO3=n-[(1-n/100)*PSO2*KSO2+n/100]*7cSO2-[(1-n/100)* *PSO3*KSO3+n/100]* 7cSO3 Для упрощения формулы найдем зависимость между PSO2 и PSO3. Если при образовании SO2и SO3 начальные твердые вещества и конечные твердые продукты одинаковы, то на получение 1 моль SO3 будет уходить на 0,5 моль O2больше, чем на образование 1 моль SO3, т. е. PSO3=PSO2+0,5. С другой стороны, если допустить, что SO3 образуется в печи из SO2 по реакции 2SO2+O2=2SO3, то и в этом случае PSO3=PSO2+0,5. Численные значения KSO2 и KSO3 найдем из соответствующих мольных объемов KSO2= VO2/VSO2=22,393/21,895=1,023 KSO3=VO2/VSO3=22,393/22,416=0,999 (Приняли, что мольный объем SO3 равен нормальному мольному объему, т. е. 22,416 нм3/кмоль.) Значение n для обычного воздушного дутья, не обогащенного кислородом, равно 4сО2=21 %. Подставляя эти данные в предыдущую формулу, получим 7cO2=21-[(1-21/100)*PSO2*1,023+21/100]*7cSO2-[(1-21/100)*(PSO2+0,5)* *0,999 +21/100]*7cSO3=21-(0,8079PSO2+0,21)*7cSO2-(0,7892PSO2+0,605)*7cSO3 Можно считать, что в условиях кипящего слоя обжиг в основном идет по уравнению 4FeS2+11O2=2Fe2O3+8SO2 ТогдаPSO2=11/8=1,375 Окончательно получаем следующую формулу для определения концентрации кислорода в сухом обжиговом газе при работе на воздушном дутье: 7cO2=21-1,3217cSO2-1,6917cSO3 Зная, что 7cSO2=14,5 % и 7cSO3=0,15 %, получим 7cO2=21-1,321*14,5-1,691*0,15=1,59% Если считать, что мольные объемы O2,SO2и SO3 равны друг другу, то KSO2=KSO3=1, и рассчитанная концентрация кислорода составит 1,95 %. А это значит, что допускается относительная ошибка (1,95-1,59)*100/1,59=22,6% Кислород по объему: 7vО=37674*1,59/100=599 нм3/ч Кислород по массе: 7mО=599*1,429=856 кг/ч 15. Азот в обжиговом газе: По объему: 7vN=37674-(5463+57+599)=31555 нм3/ч По массе: 7mN=31555*1,257=39665 кг/ч 16. Расход сухого воздуха при обжиге: По объему: 4vсух=39665*100/(100-21)=39944 нм3/ч По массе: 4mсух=39944*1,293=51647 кг/ч 17. Количество влаги, поступающей с воздухом: Для 283-273=10 °С и ɤ=70 % влагосодержание на 1 кг сухого воздуха 0,00543 кг 7mвлаги=51647*0,00543=280 кг/ч 18. Влажный воздух По массе: 4m=51647+280=51928 кг/ч По объему: 4v=39944+(280/0,804)=40292 нм3/ч 19. Пары воды в обжиговом газе: По массе: 4mпаров=(18750-18619)+280=412 кг/ч По объему: 4vпаров=412/0,804=512 нм3/ч 20. Общее количество обжигового газа: 8m=15898+202+39665+856+412=57124 кг/ч 21. Пыль, уносимая с газом: Принимаем, что унос равен 90% от общего количества огарка. 9m=13566*90/100=12209 кг/ч 22. Крупный огарок, удаляемый через спускную трубу: 10m=13566-12210=1356 кг/ч Таблица 3. Материальный баланс печи обжига колчедана в кипящем слое
Тепловой расчет Приход тепла: 1. При сгорании 5msсеры выделится тепла: qSO2=8003*12900=103237073 кдж/ч 2. При сгорании 6msсеры выделится тепла: qSO3=81*16000=1293515 кдж/ч 3. Физическое тепло воздуха: Для 283-273=10 °С и ɤ=70 % энтальпия влажного воздуха в расчете на 1 кг сухого воздуха iв=23,7 кдж/кг 4Q=51647*23,7=1224037 кдж/ч 4. Физическое тепло колчедана: 3Q=18619*0,54*8=80433 кдж/ч 5. Физическое тепло воды, поступающей с колчеданом: 2Q-3Q=(18750-18619)*33,66=4418 кдж/ч 6. Физическое тепло влажного колчедана: 2Q=80433+4418=84851 кдж/ч 7. Общий приход тепла: Qпр=103237073+1293515+1224037+84851=105839476 кдж/ч Расход тепла: 1. Физическое тепло влажного обжигового газа: 8Q =(15989*0,768+202*0,887+856*1,019+39665*1,102)*820+412*4204= =48505322 кдж/ч 2. Физическое тепло пыли в газе: 9Q=12210*1,256*820=12575100 кдж/ч 3. Физическое тепло запыленного обжигового газа: 8Q+9Q=48505322+12575100=61080422 кдж/ч 4. Физическое тепло крупного огарка, удаляемого через спускную трубу: 10Q=1357*1,256*820=1397233 кдж/ч 5. Потери тепла во внешнюю среду: Принимаем, что потери тепла во внешнюю среду равны 3 %. 11Q=105839476*0,03=3175084 кдж/ч 6. Тепло, отводимое от кипящего слоя: 12Q=105839476-(61080422+1397233+3175084)=40186636 кдж/ч
Таблица 4. Тепловой баланс печи обжига колчедана в кипящем слое
6. Заключение В ходе данной курсовой работы был рассмотрен процесс получения серной кислоты из флотационного колчедана контактным способом. В производстве серной кислоты контактным способом соблюдены основные направления развития химической промышленности и основные принципы химической технологии: - рациональное использование сырья – переход сырья в целевой продукт достигает 99,9%; - рациональное использование энергии - процесс обеспечивает сам себя необходимой энергией; - высокая интенсивность процесса – большое количество продукта с 1 объема аппарата. На основании этого делается вывод, что процесс получения серной кислоты из железного колчедана контактным способом экономичен, многотоннажен, прост, эффективен и хорошо отработан в производстве.
7. Список использованной литературы 1. ГОСТ 444-75 «Колчедан серный флотационный» |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 435. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||