Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
ПЕРЕТРАВЛЕННЯ І ОБМІН БІЛКІВСтр 1 из 3Следующая ⇒ Правила Чаргаффа 1. Вміст аденіну дорівнює вмісту тиміну, а вміст гуаніну − кількості цитозину: А = Т, G = C 2. Кількість пуринових основ дорівнює кількості піримідинових основ: А + G = Т + C 3. Кількість основ з 6 аміногруп дорівнює кількості основ з 6 кетогруп: А + C = G + Т Для кожного типу ДНК сумарний вміст гуаніну та цитозину не дорівнює сумарному вмісту аденіну й тиміну, тобто (G + C) / (A + T), як правило, відрізняється від 1 (може бути як > 1, так і < 1). За цією ознакою розрізняють два основних типи ДНК: АТ-тип з переважним вмістом аденіну й тиміну і GC-тип з переважним вмістом гуаніну та цитозину.
За допомогою біуретової реакції можна виявити в гідролізаті дріжджів: а) рибозу і дезоксирибозу б) білок в) залишок фосфорної кислоти г) пуринові основи
Дослід. Виявлення в гідролізаті дріжджів білка за допомогою біуретової реакції Хід роботи.У пробірку до 5 крапель гідролізату дріжджів доливають
Ферменти, які приймають участь в розщепленні внутрішньо молекулярних зв’язків за участю води: а) гідролази б) лігази в) ліази г) ізомерази
Ферменти– специфічні органічні каталізатори, що синтезуються живими клітинами і прискорюють протікання біохімічних реакцій в організмі. Вони є білками (Дж. Самнер, 1926) з різними молекулярними масами: від 9 кДа (АОМ) до 1000 кДа. Кожен фермент каталізує певну хімічну реакцію.
Ферменти поділяються на 6 класів відповідно до типу реакції, яку вони каталізують (Комісія Міжнародного біохімічного союзу, 1961).  3-й клас. Гідролази − ферменти, які каталізують реакції гідролізу, тобто розкладання субстратів за участю молекули води. Гідролази здатні розщеплювати складноефірні, пептидні, глікозидні та інші зв’язки − естерази, пептидази та протеази, глікозидази.
До жиророзчинних вітамінів відносять: а) А, D, В1, В2 б) В1, К, Е, В2 в) С, Н, РР, А г) А, D, Е, К
Вітаміни –низькомолекулярні органічні сполуки, які виконують функції біологічних каталізаторів самостійно або в складі ферментів як кофактори. Основне джерело В. – рослини, у яких можуть міститися і так звані провітаміни (каротини та ін.), що перетворюються в В. у тваринному організмі. Важлива роль в утворенні В. належить мікроорганізмам (наприклад, мікрофлора рубця забезпечує жуйних В. групи В). Розрізняють водо- і жиророзчинні В. До водорозчинних В. відносяться: аскорбінова кислота (вітамін С), В. групи В – тіамін (вітамін В1), рибофлавін (вітамін В2), пантотенова кислота (вітамін В3), нікотинамід (ніацин, вітамін РР або В5), вітамін В6, вітамін В12 (кобаламін), біотин (вітамін Н), фолацин; до жиророзчинних: вітамін А, D (кальциферол), Е (токоферол) і К. Є група вітаміноподібних сполук – деякі флавоноїди (рутин), холін, інозит, ліпоєва, оротова, пангамова кислоти. На відміну від інших незамінних факторів харчування (амінокислоти, жирні кислоти та ін.), В. не є матеріалом для біосинтезів чи джерелом енергії. Однак вони беруть участь практично в усіх біохімічних і фізіологічних процесах, які складають сукупності обміну речовин.
В заданій долі гіпофізу секретується: а) інсулін б) вазопресин в) глюкагон г) тироксин
Гормони –біологічно активні речовини, що синтезуються в малих кількостях у спеціалізованих клітинах ендокринної системи і через циркулюючі рідини (наприклад, кров) доставляються до клітин-мішеней, де виконують свою регулюючу дію. Гормони, як і інші сигнальні молекули, володіють деякими загальними властивостями: утворюються з клітин, що виділяють їх у позаклітинний простір; не є структурними компонентами клітин і не використовуються як джерело енергії; здатні специфічно взаємодіяти з клітинами, що мають рецептори для даного гормону; мають дуже високу біологічну активність – ефективно діють на клітини в дуже низьких концентраціях (близько 10-6 - 10-11 моль/л). Будова гормонів буває різною. За хімічною будовою гормони можна класифікувати за трьома класами: 1) білково-пептидні гормони (гормони гіпоталамуса і гіпофіза (у цих залозах синтезуються пептиди і деякі білки), а також гормони підшлункової і паращитовидної залоз і один з гормонів щитовидної залози); 2) похідні амінокислот (аміни, що синтезуються в мозковому шарі наднирників і в епіфізі, а також йодвмістні гормони щитовидної залози); 3) стероїдні гормони, що синтезуються в корі наднирників і в статевих залозах. По кількості вуглецевих атомів стероїди відрізняються один від одного: С21 − гормони кори наднирників і прогестерон; С19 − чоловічі статеві гормони – андрогени і тестостерон; С18 − жіночі статеві гормони − естрогени. Загальним для всіх стероїдів є наявність стеринового ядра –циклопентанпергідрофенантрену.
До пептидів належать багато біологічно активних речовин: глутатіон та деякі гормони (глюкагон, вазопресин, окситоцин та ін.).
Окислювальне фосфорилювання – це: а) гідроліз АТФ до АДФ і фосфорної кислоти б) перенесення залишку фосфорної кислоти від АТФ на іншу сполуку в) синтез АТФ із АДФ і фосфорної кислоти г) синтез АДФ із АТФ і фосфорної кислоти
Фосфорилювання – включення в молекулу залишку фосфатної кислоти. У живих клітинах здійснюється ферментами класу трансфераз (кіназами, фосфомутазами, фосфорилазами). Відіграє важливу роль в обмінних процесах, оскільки багаточисленні сполуки вступають у реакції обміну речовин лише у фосфорильованій (активованій) формі. Каталізоване протеїнкіназами Ф. білків (зокрема, ферментів) виконує регуляторну функцію. Важливе значення в енергетиці живої клітини має Ф. АДФ з утворенням АТФ, яке відбувається під впливом поліферментної системи за рахунок окиснення низькомолекулярних сполук киснем у дихальному ланцюзі (окиснювальне фосфорилювання) або в анаеробних умовах (наприклад, гліколітичне фосфорилювання). Енергія, акумульована у вигляді високоенергетичних зв’язків АТФ, використовується організмом для руху, синтезу необхідних речовин і т.п. У фотосинтезуючих організмів Ф. АДФ з утворенням АТФ може також відбуватися при фотосинтезі (фотофосфорилювання).
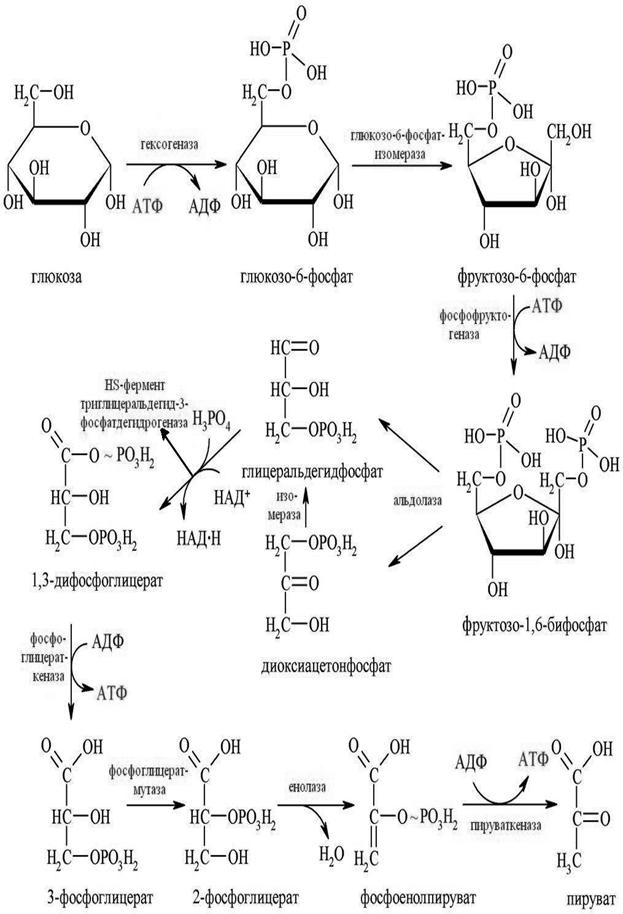
Який чистий вихід АТФ при гліколізі в анаеробних умовах на 1 молекулу глюкози? а) 1 моль б) 4 моль в) 3 моль г) 2 моль Гліколізшлях Ембдена-Мейергофа-Парнаса – ферментативний анаеробний процес негідролітичного розпаду вуглеводів (головним чином глюкози) до молочної кислоти.
Рисунок 3 - Схема глiколiзу
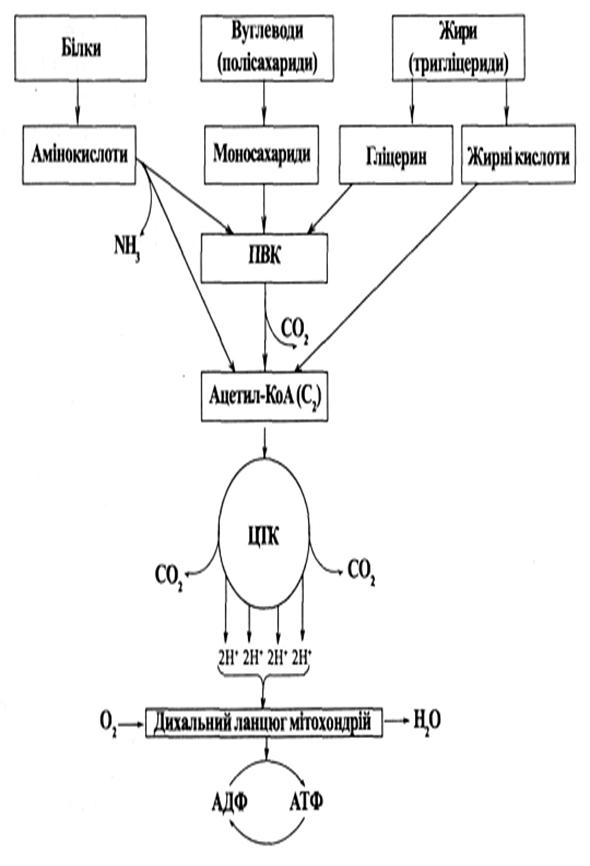
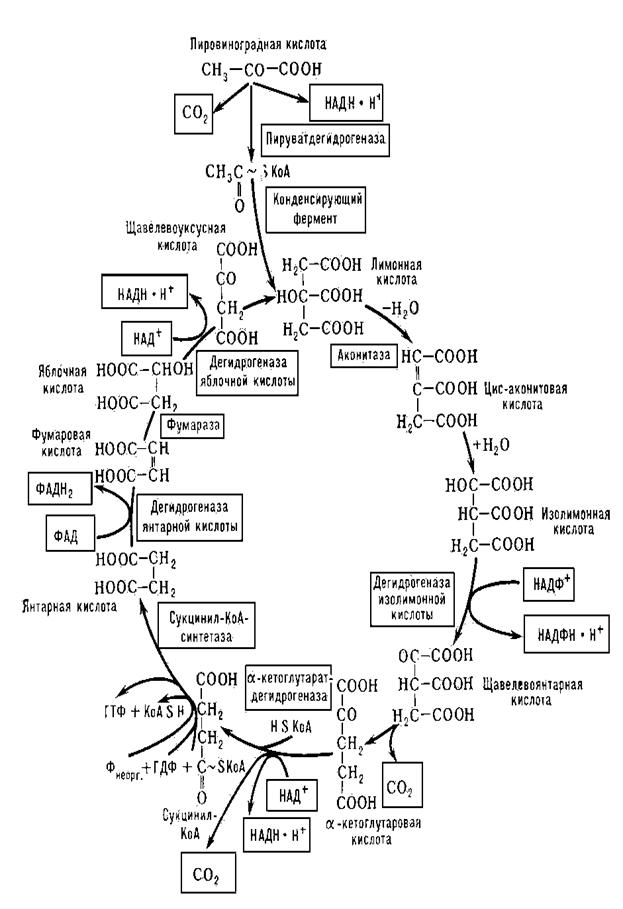
Ключова проміжна сполука, яка утворюється при окисненні вуглеводів, ліпідів та амінокислот? а) оксалоацетат б) ацетил-КоА в) фосфоенолпіруват г) малат
Рисунок 5 − Послідовність реакцій β-окислення жирних кислот (загальна схема)
Фермент хімотрипсин виділяється: а) підщлунковою залозою б) щитовидною залозою в) статевими залозами г) корою наднирників
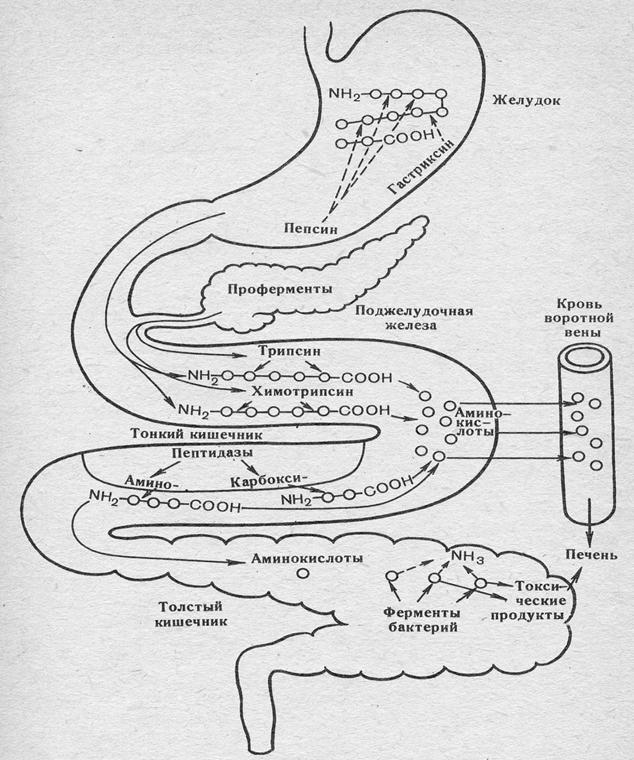
ПЕРЕТРАВЛЕННЯ І ОБМІН БІЛКІВ
Рисунок 1 − Перетравлення та всмоктування білків їжі у шлунково-кишковому тракті
Таблиця 1 − Протеолітичні ферменти шлунково-кишкового тракту
Таблиця 2 – Протеолітичні ферменти шлунково-кишкового тракту
Гідроліз ліпідів відбувається під дією: а) амілази б) пепсину в) трипсину г) ліпази
|
||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-05-10; просмотров: 445. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |