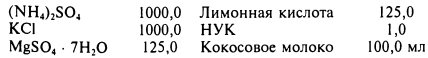Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Классификация питательных сред.Стр 1 из 2Следующая ⇒ Введение. Известно очень много питательных сред для культивирования микроорганизмов (более двух тысяч наименований было классифицировано Левином и Шенлейном еще в 1930 г.), но число ингредиентов, являющихся их неотъемлемыми компонентами, относительно невелико. Однако качественный диапазон этих сред весьма широк — от растворов неорганических солей, на которых могут расти автотрофы, до сложных питательных сред, приготавливаемых из мясных гидролизатов, обогащенных кровью или сывороткой; ими обычно пользуются для выделения патогенных микроорганизмов типа стрептококков, отличающихся высокой требовательностью к составу питательной среды. Различают два основных типа питательных сред: так называемые синтетические среды, главные составные части которых точно известны (например, глюкозо-солевая питательная среда), и эмпирически подобранные питательные среды природного происхождения, состав которых точно неизвестен (к ним относятся пептоны, приготавливаемые из частично гидролизованного белка).
Выбор питательной среды зависит в значительной степени от цели эксперимента. Герберт настойчиво высказывался за повсеместное использование синтетических питательных сред. Однако следует признать, что они обладают рядом практических неудобств. Микроорганизмы, выращенные на таких питательных средах, обычно фенотипически отличаются от выращенных на питательных средах естественного происхождения типа бульона (например, по составу и по скорости деления). Размножение микроорганизмов на таких средах обычно легче подавляется избыточной аэрацией или токсическими катионами; они также более чувствительны к нарушениям баланса между некоторыми составными частями питательной среды, особенно аминокислотами. Многие бактерии нуждаются в большом числе факторов роста, и для некоторых из них до сих пор не найдены искусственные среды, на которых они могли бы размножаться. Возможно, что все эти неудобства со временем будут преодолены, но пока среды неизвестного состава типа бульонов, приготовленных из перевара, используются весьма широко, хотя они и вносят в эксперимент неконтролируемые факторы. 
В литературе опубликованы результаты количественных анализов многих питательных сред природного происхождения, что является определенным шагом на пути к их стандартизации. Однако данными этих анализов следует пользоваться с осторожностью, поскольку результаты определений, проведенных независимо друг от друга, демонстрируют существенные различия состава различных партий одной и той же питательной среды. Более того, при проведении анализов обычно игнорируется наличие в питательных средах многих существенно важных составных частей, хотя ясно, что компоненты, требуемые в следовых количествах, например витамины и катионы, могут присутствовать в исключительно малой концентрации. При этом может оказаться, что размножение бактерий идет нормально, тогда как процессы типа споруляции или адсорбции фага ингибируются. В состав сред, применяемых для выращивания бактерий, входят необходимые для построения белков цитоплазмы элементы: азот, углерод, водород, кислород, неорганические соединения, содержащие фосфор, калий, серу, натрий, магний, железо, микроэлементы: кобальт, йод, марганец, бор, цинк, молибден, медь и др. Все перечисленные элементы должны находиться в питательной среде в удобоусвояемом для данного микроорганизма соединении, причем требования различных микробов в этом отношении неодинаковы. Потребность в кислороде и водороде бактерии удовлетворяют главным образом за счет поступающей в клетку воды. По характеру усвоения азота патогенные микроорганизмы делятся следующим образом: одни из них извлекают азот из простых аммонийных соединений, другие нуждаются в аминокислотах, третьи расщепляют высокомолекулярные вещества — пептоны, представляющие собой продукты неполного ферментативного переваривания белков. Строго паразитические виды бактерий размножаются только в присутствии нативного, т. е. неизмененного, белка. Источником углерода для патогенных бактерий являются, главным образом, различные углеводы: сахар, многоатомные спирты, органические кислоты и их соли.
Потребность бактерий в неорганических элементах удовлетворяется прибавляемыми к питательной среде солями: NaCI, KH2PO4, K2HPO4 и т. д. Микроэлементы, выполняющие роль катализаторов химических процессов, необходимы в ничтожно малых количествах и поступают в питательную среду с пептоном, неорганическими солями и водой. Наряду с перечисленными органическими и неорганическими элементами бактерии нуждаются в ростовых факторах, которые по своей роли соответствуют витаминам для животных. Источником факторов роста являются прибавляемые к питательной среде продукты растительного и животного происхождения, содержащие в своем составе никотиновую, пантотеновую, парабензойную кислоты, витамины А, В, С и др. Питательные вещества могут усваиваться микробами только при определенной реакции питательной среды, так как проницаемость оболочек микробных клеток изменяется в зависимости от рН среды. Потребность в питательных веществах и физических условиях у различных видов микробов неодинакова и этим исключается возможность создания универсальной питательной среды. По консистенции различают плотные и жидкие питательные среды. Плотные питательные среды готовят из жидких посредством прибавления к ним клеевых веществ - агара или желатина.
Исходные продукты для приготовления питательных сред. Для приготовления питательных сред используют: · Продукты животного происхождения (мясо, рыба, казеин, молоко, яйца, кровь и т. д.). · Продукты растительного происхождения (картофель и др.). · Органические и неорганические соединения определенного химического состава. Питательные среды, приготовленные из продуктов растительного и животного происхождения, несмотря на то, что они не могут быть стандартны и не имеют определенного химического состава, находят широкое применение в практике микробиологии. Синтетические питательные среды, составленные из химических соединений, используют преимущественно для изучения обмена веществ микробной клетки.
Требования, предъявляемые к питательным средам. Питательные среды должны: · Содержать необходимые для питания микроба питательные вещества. · Иметь реакцию рН, оптимальную для выращиваемого вида микроба. · Иметь достаточную влажность, так как микробы питаются по законам диффузии и осмоса. · Обладать изотоничностью. · Быть стерильными, обеспечивая тем самым возможность выращивания чистых культур микробов. Питательные среды подразделяются на среды общего назначения и специальные. К первой группе относятся мясопептонные: агар, бульон, питательный желатин. Среды общего назначения используют для выращивания многих патогенных микробов и применяют в качестве основы для приготовления специальных сред, добавляя к ним кровь, сахар, молоко, сыворотку и другие ингредиенты, необходимые для размножения того или иного вида микроба. К специальным питательным средам относятся элективные (избирательные) и дифференциально-днагностическне. Элективные (избирательные) среды. Принцип создания элективных питательных сред основан на удовлетворении основных биохимических и энергетических потребностей того вида микроба, для культивирования которого они предназначены. Определенный состав и концентрация питательных микроэлементов, ростовых факторов при строгом значении рН обеспечивают оптимальные условия для выращивания одного или нескольких видов микроорганизмов. При посеве на них материала, содержащего смесь различных микроорганизмов, раньше всего будет проявляться рост того вида, для которого данная среда будет элективной. Дифференциально-диагностические питательныесреды используют для определения видовой принадлежности исследуемого микроба, основываясь на особенностях его обмена веществ. По своему назначению дифференциально-диагностические питательные среды подразделяются следующим образом: · Среды для выявления протеолитической и гемолитической способности микробов, содержащие в своем составе белковые вещества: кровь, молоко, желатин, свернутую кровяную сыворотку и т. д. · Среды с индифферентными химическими веществами, которые служат источником питания для одних видов микробов и не усваиваются другими видами. · Среды с углеводами и многоатомными спиртами для обнаружения соответствующих ферментов. · Среды для определения редуцирующей способности микробов. В состав дифференциально-диагностических сред, предназначенных для выявления сахаролитических и окислительно-восстановительных ферментов, вводят индикаторы: нейтральный красный, метиленовый синий, лакмусовую настойку, кислый фуксин, бромтимоловый синий, водный голубой краситель и розоловую кислоту. Изменяя свою окраску при различных значениях рН, индикатор указывает на наличие или отсутствие расщепления, окисления или восстановления введенного в среду ингредиента. Однако индикатор не является обязательной составной частью сред, предназначенных для выявления ферментов. Так, наличие желатиназы и других протеолитических ферментов в культуре определяют по разжижению желатина, свернутого яичного или сывороточного белка.
Классификация питательных сред.
При составлении питательных сред для микроорганизмов необходимо учитывать их потребность в элементах питания. По составу питательные среды подразделяются на две группы: естественные (натуральные) и синтетические. Естественными обычно называют среды, которые состоят из продуктов животного или растительного происхождения, имеющих сложный неопределенный химический состав. Основой таких сред являются различные части зеленых растений, животные ткани, солод, дрожжи, овощи, навоз, почва, вода морей, озер и минеральных источников. Большинство из них используется в виде экстрактов или настоев. На естественных средах хорошо развиваются многие микроорганизмы, так как в этих средах имеются, обычно, все компоненты, необходимые для роста и развития. Однако среды с неопределенным составом малопригодны для изучения физиологии обмена веществ микроорганизмов, поскольку они не позволяют учесть потребление ряда компонентов среды, а с другой стороны, выяснить, какие вещества образуются по ходу развития микроорганизмов. Это связано с тем, что состав естественных сред очень сложен; кроме того, он не является постоянным, так как существенно колеблется в зависимости от сырья и способа приготовления сред. Это заметно влияет на рост микроорганизмов. Естественные среды неопределенного состава используются главным образом для поддержания культур микроорганизмов, накопления их биомассы и для диагностических целей. К числу сред неопределенного состава относят и так называемые полусинтетические среды. В их состав наряду с соединениями известной химической природы входят вещества неопределенного состава. Синтетические среды — это такие среды, в состав которых входят только определенные, химически чистые соединения, взятые в точно указанных концентрациях. Синтетические среды следует готовить на дистиллированной воде. Для разработки синтетических сред, обеспечивающих нормальный рост изучаемого микроорганизма или максимальный биосинтез какого-либо продукта его жизнедеятельности, необходимо знать особенности обмена веществ данного организма и его потребности в источниках питания. В настоящее время в распоряжении микробиологов имеется достаточное количество синтетических сред, не уступающих по своим качествам сложным средам неизвестного состава. Синтетические среды могут иметь относительно большой набор компонентов, но могут быть и довольно простыми по составу. Синтетические среды наиболее удобны для исследования обмена веществ микроорганизмов. Зная точный состав и количество входящих в среду компонентов, можно изучить их потребление и превращение в соответствующие продукты обмена. С. Н. Виноградским в практику микробиологии введены элективные (избирательные) среды для определенных групп микроорганизмов. Эти среды обеспечивают преимущественное развитие одного вида или группы родственных микроорганизмов и менее пригодны или совсем не пригодны для развития других. Зная физиологические особенности соответствующей группы микробов, можно подобрать такие условия культивирования (состав среды, ее активную кислотность, условия аэрации, температуру и др.), при которых будут развиваться лишь микроорганизмы этой группы. Это позволяет вести различные биологические процессы в лаборатории и в производстве без предварительной стерилизации среды. Такие среды применяются главным образом для выделения микроорганизмов из мест их естественного обитания, для получения накопительных культур. Понятие «элективные среды» входит в более широкое понятие «элективные условия». Питательные среды применяют различной консистенции: жидкие, плотные, полужидкие. Плотные питательные среды используют для учета количества бактерий, выделения их в чистую культуру и других целей. Такие среды готовят из жидких, добавляя 1,5—2,5% агар-агара или 10—15% желатины. При приготовлении полужидких сред вносят агар-агар в количестве 0,1—0,2%. По назначению среды подразделяют на: элективные и дифференциально-диагностические. Элективные среды обеспечивают преимущественное развитие одного или целой физиологической группы микроорганизмов. Например, для преимущественного выделения грамотрицательных бактерий бывает достаточным добавления в питательную среду трифенилметановых красителей (кристаллический фиолетовый, малахитовый зеленый и т. д.). Для выделения стафилоккоков в среду может быть добавлен хлористый натрий в концентрации 7,5 %. При этой концентрации рост других бактерий подавляется. Элективные среды применяются на первом этапе выделения чистой культуры бактерий, т. е. при получении накопительной культуры. Дифференциально-диагностические среды применяются для быстрой идентификации близкородственных видов микроорганизмов, для определения видовой принадлежности, в клинической бактериологии и др. Принцип построения дифференциально-диагностических сред основан на том, что разные виды бактерий различаются между собой по биохимической активности и имеют неодинаковый набор ферментов, расщепляющих субстраты, входящие в состав питательной среды. В состав дифференциально-диагностической среды входят: а) основная питательная среда, обеспечивающая размножение бактерий; б) определенный химический субстрат, отношение к которому является диагностическим признаком для данного микроорганизма; в) цветной индикатор, изменение окраски которого свидетельствует о биохимической реакции и наличии данной ферментной системы у исследуемого микроорганизма. Например, среда Эндо позволяет отличить клоны, сбраживающие лактозу от клонов, не обладающих этим свойством. Основными компонентами этой среды являются питательный (пептонный) агар, углевод и основной фусин, обесцвеченный сульфитом (реактив Шиффа). Исходная питательная среда окрашена в розовый цвет. Микроорганизмы, не сбраживающие лактозу, образуют бесцветные колонии. При сбраживании лактозы до ацетальдегида последний реагирует с сульфитом и развививается красная окраска соответствующих колоний. Среда с эозином и метиленовым синим (среда Левина) в качестве индикаторов содержит эозин и метиленовый синий и исходно окрашена в черно-синий цвет. Клетки, осуществляющие брожение, образуют колонии, окрашенные в черный с металлическим блеском цвет, а колонии, не обладающие этим свойством, бесцветны. Подобные изменения окраски происходят потому, что красители присутствуют в среде не в виде самостоятельных соединений, а в виде комплексов с веществами питательной среды. При низких значениях рН эти комплексы выпадают в осадок, исходные же красители в этих условиях растворимы, при больших рН комплексы красителей бесцветны, тогда как метиленовый синий приобретает синюю окраску. Данная среда позволяет дифференцировать бактерии рода Escherichia от бактерий рода Proteus.
Состав питательных сред.
Это растительный коллоид, получаемый из некоторых морских водорослей. В его состав входят главным образом полисахариды с ничтожным содержанием азотистых веществ. Желатина — кислый азотсодержащий продукт, добываемый путем выварки костей и хрящей. В качестве плотных питательных сред широко применяют также гелевые пластины, введенные в микробиологическую практику С. Н. Виноградским. Для выращивания микроорганизмов, использующих органические формы азота, часто употребляют мясопептонные среды: мясопептонный бульон, мясопептонный агар и мясопептонную желатину. Мясопептонный бульон (МПБ). Для приготовления мясо-пептонных сред используют мясной бульон, который получают так: 500 г мелко изрубленного свежего мяса без костей, жира и сухожилии заливают в эмалированной кастрюле 1 л водопроводной воды, нагретой до 50°С, и оставляют настаиваться 12 ч при комнатной температуре или 1 ч при 50—55°С. Мясо отжимают, экстракт процеживают через марлю со слоем ваты, кипятят в течение 30 мин для свертывания коллоидных белков и фильтруют дважды (первый раз через марлю с ватой, второй — через бумажный фильтр). Фильтр доливают водой до 1 л, разливают в колбы, закрываю! ватными пробками и стерилизуют при 120°С 20 мин (пробки колб закрывают сверху колпачками из бумаги). Ватные пробки должны быть плотными, так как они являются фильтром, препятствующим проникновению бактерий из воздуха после стерилизации. Мясной бульон может быть использован в любое время для приготовления соответствующих сред. Если их готовят сразу, то предварительная стерилизация излишня. Нередко в лабораторных условиях мясной настой кипятят вместе с мясом, а затем мясо отжимают. Бульон получается хорошего качества. Если желательно иметь мясной бульон особо высокой питательности, во время настаивания мяса с водой добавляют немного пепсина и подкисляют бульон соляной кислотой. Пепсин дополнительно гидролизует белковые соединения мяса, и количество усвояемых бактериями питательных веществ возрастает. Мясо можно заменить мясным экстрактом, беря его по 5 г на 1 л среды. Для приготовления мясопептонного бульона к 1 л мясного бульона добавляют 5—10 г пептона (пептон — первый продукт гидролиза белка с высокой молекулярной массой) для повышения калорийности среды и 5 г поваренной соли с целью создания осмотической активности. Среду нагревают до растворения пептона, постоянно помешивая. Затем устанавливают нейтральную или слабощелочную реакцию среды, приливая 20%-ный раствор NagCOa (до посинения влажной красной лакмусовой бумажки; при этом фенолфталеин еще не показывает щелочную реакцию — при добавлении его к среде в фарфоровой чашке розовая окраска не выявляется). Удобно использовать индикатор бромтимолблау. 1—2 капли его вносят стеклянной палочкой в фарфоровую чашку и добавляют каплю бульона. В нейтральной среде бромтимолблаубутылочно-зеленый, в кислой — желтый, в щелочной — синий. После установления реакции среду снова кипятят 5—10 мин и белки, свернувшиеся от изменения реакции, отфильтровывают через бумажный фильтр без осветления бульона или осветлив его белком. Прозрачный Мясо-пептонный бульон разливают в пробирки, закрывают ватными пробками и стерилизуют при 120°С в течение 20 мин. Мясо-пептонныйагар (МПА). К 1 л мясо-пептонного бульона добавляют 15—20 г мелко нарезанного агар-агара. Среду нагревают до растворения агара (температура плавления его 100°С, застывания —40°С),устанавливают слабощелочную реакцию среды 20%-ным раствором Na2COa и через воронки разливают в пробирки (но 10 мл для разливок в чашки — агар столбиком и по 5 мл для получения скошенного, наклонного агара). При разливе агара необходимо следить затем, чтобы края пробирки были сухими, иначе пробки прилипают к стеклу. Пробирки со средой стерилизуют в автоклаве при 120°С в течение 20 мин. Мясо-пептонная желатина (МПЖ). В 1 л мясопептонного бульона помешают 100—150 г желатины. Температура плавления зависит от процентного содержания в среде. 10%-ная желатина плавится при 24°С, 15%-пая — при 25°. В летнее время среды готовят, добавляя 15% желатины. После растворения желатины при осторожном нагревании в среде устанавливают слабощелочную реакцию (как и для МПБ и МПА), кипятят в течение 5мин, затем охлаждают -до 40—50°С. Одновременно яичный белок взбивают с небольшим количеством воды, вливают его в охлажденную желатиновую среду, хорошо взбалтывают и снова нагревают. Среда после выпадения белков становится прозрачной. Ее фильтруют через горячую воронку, разливают в пробирки и стерилизуют в кипятильнике Коха текучим паром, прогревая среду по 30 мин через 24 ч 3 раза.
200 г очищенного и промытого водой картофеля нарезают ломтиками, заливают 1 л водопроводной воды, варят 30 мин. Отвар фильтруют через вату и доводят до первоначального объема. К полученной жидкости прибавляют 2% агара, кипятят до его растворения и устанавливают нейтральную реакцию среды (рп 7,0). Среду стерилизуют при 1атм в течение 20 мин. Пивное сусло. Зерна ячменя замачивают в холодной воде и проращивают при 35°С. После того как ростки будут вдвое больше длины зерна, последнее высушивают до воздушно-сухого состояния (можно при слабом подогревании) и получают солод. Для приготовления сусла солод крупно размалывают и 250 г его берут на 1 л воды. Смесь подогревают при 57°С (для лучшего выделения фермента амилазы) до исчезновения реакции на крахмал (синее окрашивание с йодом). Пробы на осахаривание крахмала проводят в фарфоровой чашке в капле жидкости. Сусло процеживают через вату, затем фильтруют через бумажный фильтр. Такое сусло содержит 10— 20% сахара. Определив его содержание по плотности раствора с помощью сахариметра, сусло разбавляют водой до концентрации сахара 6—8%, стерилизуют при 115°С (давление 0,5 атм) в течение 30 мин. Готовое сусло можно получить на пивоваренном заводе. Сусло-агар. К приготовленному суслу добавляют 2,5—3% агара, кипятят до его расплавления, фильтруют через вату и стерилизуют таким же способом, как пивное. Обезжиренное молоко. Для приготовления питательных сред употребляют снятое молоко, так называемый обрат (жир в молоке неблагоприятно влияет на рост некоторых микроорганизмов). Обрат получают сепарированием молока, нагретого до 34°С. Жир можно удалять и при отстаивании молока. При стерилизации молока следует учитывать, что его нельзя длительное время выдерживать в автоклаве, так как лактоза (молочный сахар), содержащаяся в молоке, может карамелизоваться. Обезжиренное молоко разливают в стерильные пробирки и выдерживают при 115°С (давление 0,5 атм) 15 мин. Перед стерилизацией кислотность обрата не должна превышать 22° Тернера, иначе молоко свернется. После стерилизации его выдерживают трое суток в термостате при 30°С, чтобыпровоцировать развитие спорообразующих и других стойких к нагреванию форм. Через 3 дня каждую пробирку с молоком просматривают и пробирки, в которых развились микроорганизмы, выбраковывают. При стерилизации в автоклаве иногда наблюдается побурение молока вследствие карамелизации молочного сахара и пептонизации казеина. При длительной стерилизации на дно пробирки выпадает осадок казеина, который может частично пептонизироваться. Перегретое побуревшее молоко в качестве среды использовать нельзя.
Пептон Мартена. Свиные желудки (не промытые водой) с обильным слизистым слоем очищают от пленок, жира и пропускают через мясорубку. К фаршу прибавляют воду и соляную кислоту в следующем соотношении: фарш из свиных желудков 250 г, вода водопроводная, нагретая до 50°С, 1000 мл, соляная кислота (удельный вес 1,18) 10 мл. Смесь выдерживают в термостате при 50°С. Через 24 часа пептон прогревают в автоклаве при 100°С и фильтруют, фильтрат подщелачивают 10% раствором NaOH до щелочной реакции по лакмусу. После этого фильтрат разливают в колбы и стерилизуют при 115°С 30 минут. Для приготовления бульона пептон Мартена смешивают с равным объемом мясной воды, устанавливают необходимую реакцию, кипятят 30 минут, фильтруют и стерилизуют при 115°С 30 минут. Мясо можно переваривать с помощью трипсина — перевар Хоттингера, при этом более полно используют белки мяса, которые расщепляются до пептонов, полипептидов и свободных аминокислот. При триптическом переваривании мяса получают в 10 раз больше бульона, чем при обычном методе.
Мясной перевар Хоттингера. Мясо, освобожденное от жира и сухожилий, нарезают небольшими кусочками, помещают в кастрюлю с кипящей водопроводной водой (в полуторном объеме) и кипятят 15—20 минут, затем мясо извлекают из жидкости и пропускают через мясорубку. Установив рН охлажденной до 40—45°С жидкости, равный 8, заливают ею фарш. К полученной смеси добавляют сухой панкреатин в количестве 0,5—1% или поджелудочную железу из расчета 100 г железы на 1 л жидкости. Затем смесь снова подщелачивают до рН 8 и разливают ее в бутыль. Туда же добавляют 2—3% хлороформа и, закрыв бутыль резиновой пробкой, несколько раз встряхивают содержимое. Бутыль ставят на 7—14 суток при температуре 37°С. В результате переваривания мясной фарш превращается в гомогенный сероватый осадок, над которым находится совершенно прозрачная жидкость соломенно-желтого цвета. Перевар Хоттингера хорошего качества дает положительную реакцию на триптофан и содержит 560—860 мг% аминного азота. Для приготовления бульона к 1 части перевара прибавляют 6—7 частей воды. Триптические перевары. Приготовление бульона из переваров по Хоттингеру является более экономичным, чем применение мясопептонных сред; из одного и того же количества мяса получают бульона в 5—10 раз больше. Кроме того, можно использовать для переваривания заменители мяса. Наконец, присутствие в переварах значительного количества аминокислот создает буферность, а следовательно, и большую стабильность рН среды.
Перевар по Хоттингеру. 1кг мяса, очищенного от жира и сухожилий, нарезают кусками примерно 1—2 см. Мясо опускают небольшими порциями в кастрюлю с двойным количеством (по отношению к мясу) кипящей водопроводной воды; кипятят 15—20 минут, пока мясо не станет серым, что указывает на то, что белки свернулись. Мясо вынимают шумовкой и пропускают его через мясорубку. Устанавливают в жидкости рН 8,0. Опускают фарш в жидкость и охлаждают до 40° в открытой кастрюле, затем добавляют поджелудочную железу (очищенную от жира, соединительной ткани и дважды пропущенную через мясорубку) 1 в количестве 10% к взятой жидкости (на 1 л жидкости 100 г железы) или сухой панкреатин в количестве 0,5% и выше в зависимости от его активности. Хорошо размешивают, после чего снова подщелачивают смесь до рН 7,8—8,0 и повторяют такое подщелачивание через 30 минут. Отсутствие сдвига реакции смеси в сторону окисления указывает не недоброкачественность фермента. После установления рН смесь переливают в бутыль с плотной резиновой пробкой с таким расчетом, чтобы 1/3 бутыли оставалась свободной. Добавляют 1—3% хлороформа — 10—30 мл на 1 л жидкости (в холодное время года меньше, чем в теплое), закрывают бутыль пробкой и несколько раз встряхивают так, чтобы хлороформ перемещался от дна бутыли к пробке и обратно, после чего на минуту вынимают пробку для освобождения от избытка паров хлороформа. Через 1—2 часа после добавления фермента опять проверяют реакцию и устанавливают рН 7,4—7,6. При этой реакции оставляют смесь для переваривания на 7—10—16 дней при комнатной температуре. Первые 3—4 дня переваривания ежедневно проверяют и исправляют реакцию. В эти дни также встряхивают перевар не менее 3 раз в сутки. В дальнейшем проверку реакции производить нецелесообразно, а встряхивать можно реже; за 1—2 дня до окончания переваривания встряхивания совсем прекращают, чтобы перевар отстоялся.
Конец переваривания характеризуется следующими признаками: 1) на дне бутыли собирается пылевидный осадок; 2) жидкость над осадком просветляется и принимает соломенно-желтый цвет; 3) перевар легко фильтруется; 4) реакция на триптофан с бромной водой должна быть положительной (в пробирку наливают 3—4 мл фильтрованного перевара, добавляют 3-4 капли бромной воды; при наличии триптофана жидкость принимает розово-фиолетовый цвет (сравнивают с контрольной пробиркой, где к перевару не прибавлена бромная вода); 5) гидролизат перевара доведен до содержания в нем 1100—1200 мг% общего азота. По окончании гидролиза перевар фильтруют через полотняный или бумажный фильтр, разливают в бутыли и стерилизуют 30 минут при давлении 1 атм. (120°) для хранения впрок. Перед употреблением фильтруют.
А) Поджелудочную железу можно применять свежую, замороженную или соленую. Свежую поджелудочную железу можно консервировать впрок. Для этого ее очищают от жира, пропускают через мясорубку и закладывают в стерильную банку, куда добавляют столько глицерина, чтобы он покрыл поверхность. В таком виде ее можно хранить на холоду 2—3 месяца. Консервировать поджелудочную железу можно также поваренной солью. Прибавляют 15% соли по отношению к весу железы и тщательно перемешивают. В таком виде железа хранится до 6 месяцев. Если железа не свежая, а соленая, она удовлетворительно хранится и без глицерина.
Казеиновый перевар. Пищевой кислотный казеин в виде сухого желтоватого порошка является отходом молочной промышленности, характеризуется полноценным составом аминокислот и высокой питательностью. Водопроводную воду нагревают до 45°, подщелачивают в открытом сосуде до рН 8,2, прибавляют 7—10% сухого казеина, высыпая его постепенно при непрерывном помешивании. После прибавления казеина снова устанавливают прежнюю реакцию. Размешивание и подщелачивание производят несколько раз, каждые 30 минут, пока казеин не разбухнет. Тогда добавляют 7—10% фарша из поджелудочной железы или сухого панкреатина, хорошо размешивают и снова подщелачивают до прежней реакции. Через 30 минут опять устанавливают реакцию и переливают смесь в бутыль. В дальнейшем поступают так же, как при изготовлении перевара из мяса. Переваривание казеина при комнатной температуре продолжают 16—20 дней.
Перевар из кровяных сгустков. Среды из кровяных сгустков характеризуются высокой питательностью и значительной буферностью. Кровяные сгустки промывают на решетке водой и дают воде стечь. Сгустки взвешивают. Наливают в кастрюлю тройное по весу сгустков количество водопроводной воды и доводят ее до кипения. В кипящую воду постепенно опускают сгустки и кипятят 20—30 минут до просветления жидкости; образующуюся пену снимают шумовкой. После кипячения сгустки вынимают из жидкости и нарезают ножом на мелкие кусочки. Заливают в открытом сосуде отваром из расчета на 1 кг сгустков 3 л отвара, подщелачивают до рН 8,0—8,2. Выкипевшее количество жидкости доливают дистиллированной водой. Смесь охлаждают до 37—40°. В дальнейшем поступают, как указано для мясного перевара. Среды из трипсиновых переваров, особенно из казеина, обладают достаточной буферностью и реакцию после стерилизации не меняют.
Дрожжевые среды. Дрожжевая вода. 50—100 г сухих дрожжей размешивают в 1 л воды, кипятят 10 мин, фильтруют через бумажный фильтр и стерилизуют текучим паром по полчаса в течение трех дней ежедневно. Дрожжевой автолизат. 200 г прессованных дрожжей разводят в 1 л воды, добавляют 2 г Na2HPO4, 1 н. раствор NaOH (до рН 6,1) и 5 мл хлороформа, выдерживают при 37°С двое суток, доводят до рН 7,4, кипятят 30 мин, фильтруют через бумажный фильтр, разливают в посуду и стерилизуют при 115°С полчаса. Дрожжевой экстракт. 1 кг прессованных дрожжей разводят в 1 л воды, смесь кипятят 1 ч, трижды отфильтровывают через бумажный фильтр и стерилизуют при 115°С 30 мин. Бобовый отвар. 50 г фасоли (лучше белой) заливают 1 л водопроводной воды и варят до готовности так, чтобы бобы не разварились. Полученный отвар фильтруют через вату, добавляют к нему 10 г сахара и доводят до первоначального объема. Устанавливают слабощелочную реакцию среды, разливают в колбы и стерилизуют в автоклаве при давлении пара 1,5 атм в течение 30 мин.
Ниже приведены самые известные и употребляемые составы питательных сред для размножения декоративных растений. Концентрация веществ указана в миллиграммах на 1 л среды (мг/л).
Состав питательной среды Бургеффа
Состав питательной среды Вацина-Вента
Состав питательной среды Вимбера
Состав питательной среды Кнопа
Состав питательной среды Линсмайера-Скуга
Состав питательной среды Линдемана
Состав питательной среды Мореля
Состав питательной среды Мурашиге-Скуга
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 777. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |

 Агар-агар.
Агар-агар.
 Картофельный агар.
Картофельный агар.