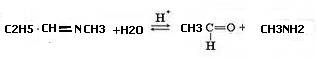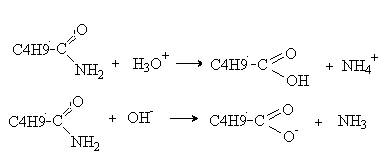Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Карбоновые кислоты и их функциональные производныеОтвет
2.Механизм этой реакции –нуклеофильное присоединение с последующим отщеплением молекулы воды
3. Роль кислотного катализатора – протонирование на стадии а) 4. В присутствии разбавленных кислот имины гидролизуются водой с образованием карбонильных соединений и аминов, эта реакция обратна реакции синтеза иминов:
В присутствии щелочи гидролиз не идет
Карбоновые кислоты и их функциональные производные 37. Напишите схему получения пропилбензоата из кислоты и спирта. Опишите механизм этой реакции. Сравните ацилирующую способность бензойной и уксусной кислот. Укажите роль кислотного катализатора. Объясните возможность гидролиза пропилбензоата в кислой и щелочной среде. Подтвердите Ваше предположение соответствующими уравнениями. . Ответ
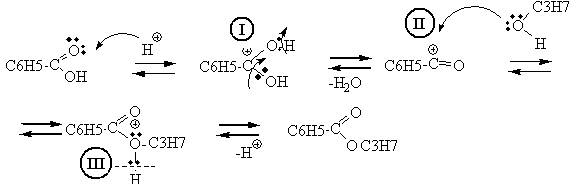
2.Механизм реакции этерификации – нуклеофильное замещение SN : замещение ОН-группы на алкоксигруппу (ОС3Н7).
Роль катализаторов в реакции этерификации играют ионы водорода. Кислород карбоксильной группы, захватывая протон, образует карбониевый ион I. Соединение I присоединяет молекулу спирта за счет неподеленных электронов кислородного атома с образованием промежуточного комплекса II, Этот комплекс способен обратимо распадаться с отщеплением воды и образованием нового карбониевого катиона сложного эфира III, который при диссоциации образует сложный эфир, причем освобождается катализатор – протон. 3. Электронодонорные заместителиуменьшают электрофильность карбонильного атома углерода и, следовательно, понижают реакционную способность оксосоединения. Фенильный радикал С6Н5 в бензойной кислоте обладает более выраженными донорными свойствами, чем метильный радикал в уксусной кислоте. Как следствие, реакция этерификации с участием бензойной кислоты протекает медленнее, чем в случае алифатических. Таким образом, ацилирующая способность бензойной кислоты ниже, чем уксусной.
 4. Роль кислотного катализатора – участие в образовании промежуточного карбониевого иона I . 5. Гидролиз пропилбензоата в кислой среде протекает с образованием пропилового спирта и бензойной кислоты (реакция а), в щелочной среде – пропилового спирта и бензоата (реакция б):
38. Напишите схему реакции получения амида валериановой (пентановой) кислоты из ее хлорангидрида. Опишите механизм этой реакции. Объясните возможность её протекания без участия катализатора. Обоснуйте необходимость применения кислотного или щелочного катализатора при гидролизе полученного амида.
Ответ
2. Механизм этой реакции –нуклеофильное замещение, протекает по бимолекулярному (SN2) механизму
На первом этапе молекула аммиака, имеющая неподеленную электронную пару, атакует атом углерода, связанный с кислородом и хлором. Вследствие разности электроотрицательностей на этом атоме углерода будет недостаток электронной плотности. Образуется промежуточное соединение I. На втором этапе происходит отщепление молекулы хлороводорода с образованием амида. 3. Данная реакция может протекать без участия катализатора, так как галоген в галогенанангидридах обладает большой реакционной способностью 4. В жестких условиях под действием водных растворов кислот или щелочей амиды гидролизуются: Механизмы реакций аналогичны гидролизу сложных эфиров. Однако, в отличие от гидролиза эфиров, кислотный и щелочной гидролиз амидов протекают необратимо.
Омыляемые липиды
39. Напишите уравнение реакции образования фосфатидилэтаноламина (кефалина) в состав которого входят олеиновая и линолевая кислоты. Изобразите конформационную формулу олеиновой кислоты. Укажите полярную и неполярную части ее молекулы. Ответ
2. Конформационная формула олеиновой кислоты
3.
40. Напишите уравнение реакции образования фосфатидилхолина (лецитина), в состав которого входят стеариновая и линолевая кислоты. Изобразите конформационную формулу линоленовой кислоты. Укажите полярную и неполярную части ее молекулы.
2. Конформационная формула линолевой кислоты
41. Напишите уравнение реакции взаимодействия 1-пальмитоил-2-олеоил-3-линоленоилглицерина с йодом. Классифицируйте исходный субстрат по химическому составу. Изобразите конформационную формулу олеиновой кислоты. Укажите полярную и неполярную части ее молекулы. Сформулируйте определение понятия “йодное число”. Объясните назначение этого показателя.
Ответ
2. Исходный субстрат является сложным эфиром трехатомного спирта глицерина и трех высокомолекулярных карбоновых кислот: пальмитиновой С15Н31СООН (предельная кислота), олеиновой С17Н33СООН (непредельная кислота, содержит одну двойную связь), линоленовой С17Н29СООН (непредельная кислота, содержит три двойных связи). При взаимодействии с иодом к остатку олеиновой кислоты присоединится 1 молекула I2, к остатку линоленовой кислоты – 3 молекулы I2. 3. Конформационная формула олеиновой кислоты
4. “йодное число” -масса иода (в г), присоединяющегося к 100 г органического вещества 5.Назначение показателя: Иодное число, которое характеризует содержание двойных связей в ненасыщенном соединении, определяют при исследовании жиров, а также при анализе жирных кислот и установлении содержания реагирующих с иодом примесей в ароматических углеводородах. Иодное число определяет общую ненасыщенность жиров. Чем выше иодное число, тем больше ненасыщенных кислот содержится в жире, то есть тем больше иода вещество может присоединить.
42. Напишите уравнение реакции гидрогенизации 1-стеароил-2,3-линолеоилглицерина. Классифицируйте исходный субстрат по химическому составу. Изобразите конформационную формулу линолевой кислоты. Укажите полярную и неполярную части ее молекулы. Назовите практическое применение этой реакции. Укажите преимущества и недостатки полученного продукта, используемого в пищевых целях.
Ответ
2. Исходный субстрат является сложным эфиром трехатомного спирта глицерина и двух высокомолекулярных карбоновых кислот: стеариновой С17Н35СООН (предельная кислота), линолевой С17Н31СООН (непредельная кислота, содержит 2 двойных связи). При гидрогенизации к одному остатку линолевой кислоты присоединится 2 молекулы Н2
3. Конформационная формула линолевой кислоты
4. Практическое применение реакции гидрогенизациисложных эфиров глицерина и непредельных карбоновых кислот используется для превращения жидких растительных жиров в твердые (маргарин). При этом повышается энергетическая ценность продуктов. Недостатки: продукт гидрогенизации может содержать побочные продукты и следы катализатора. Помимо этого, в продукте содержатся соединения транс-жирных кислот (ТЖК), являющихся ксенобиотиками.
43. Напишите уравнение реакции омыления (щелочного гидролиза) фосфатидилсерина, содержащего пальмитиновую и арахидоновую кислоты. Изобразите конформационную формулу арахидоновой кислоты. Укажите полярную и неполярную части ее молекулы. Ответ
2. Конформационная формула арахидоновой кислоты
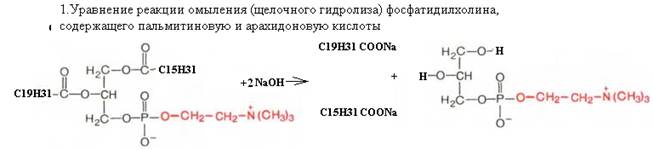
44. Напишите уравнение реакции омыления (щелочного гидролиза) фосфатидилхолина, содержащего пальмитиновую и арахидоновую кислоты. Изобразите конформационную формулу арахидоновой кислоты. Укажите полярную и неполярную части ее молекулы.
2. Конформационная формула арахидоновой кислоты
45. Напишите уравнение реакции кислотного гидролиза кефалина, содержащего стеариновую и линолевую кислоты. Изобразите конформационную формулу линолевой кислоты. Укажите полярную и неполярную части ее молекулы. Ответ
2. Конформационная формула линолевой кислоты
Моносахариды
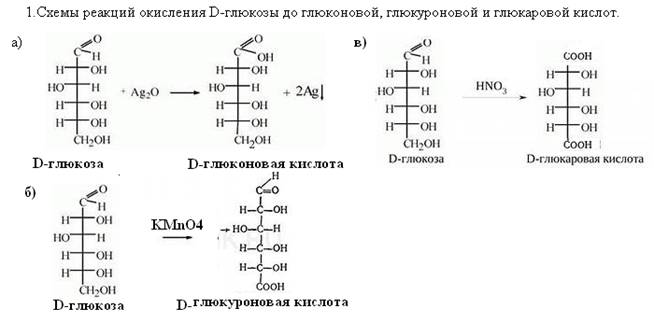
46. Напишите схемы реакций окисления D-глюкозы до глюконовой, глюкуроновой и глюкаровой кислот. Укажите условия протекания реакций.
Ответ
2.Условия проведения: окисления до глюконовой кислоты протекает под воздействием мягкодействующих окислителей:оксида серебра, хлорноватистой или бромноватистой кислоты. Окисление до глюкуроновой кислоты протекает в более жестких условиях, например, под воздействием перманганата калия или дихромата калия в присутствии серной кислоты. Получение глюкаровой кислоты происходит при обработке глюкозы концентрированной азотной кислотой.
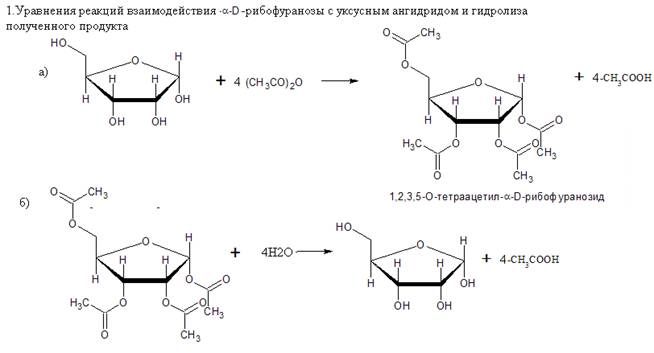
47. Напишите уравнения реакций взаимодействия a,D-рибофуранозы с уксусным ангидридом и гидролиза полученного продукта. Назовите продукты первой реакции. Ответ
48. Напишите уравнения реакций образования глюкозо-1-фосфата, глюкозо-6-фосфата, фруктозо-1,6-дифосфата. Объясните значение полученных продуктов в процессах жизнедеятельности.
Ответ
1. Уравнения реакций образования глюкозо-1-фосфата, глюкозо-6-фосфата, фруктозо-1,6-дифосфата.
2.Значение полученных продуктов в процессах жизнедеятельности: А)глюкозо-6-фосфат образуется на первой стадии гликолиза при фосфорилировании молекулы глюкозы. Фосфорилирование глюкозы преследует две цели: во-первых, из-за того что плазматическая мембрана, проницаемая для нейтральной молекулы глюкозы, не пропускает отрицательно заряженные молекулы глюкозо-6-фосфата, фосфорилированная глюкоза оказывается запертой внутри клетки. Во-вторых, при фосфорилировании глюкоза переводится в активную форму, способную участвовать в биохимических реакциях и включаться в метаболические циклы., происходящее при участии тканеспецифичного фермента гексокиназы . Б) Образование фруктозо-1,6-дифосфата - это вторая ключевая реакция гликолиза, её регуляция определяет интенсивность гликолиза в целом. В) После изомеризации глюкозо-6-фосфата в глюкозо-1-фосфат протекает дополнительная активация глюкозного фрагмента, что важно для синтеза гликогена в печени.
49.Напишите уравнения реакций взаимодействия D-маннозы с СН3I и СН3ОН и гидролиза полученных продуктов. Объясните отличие в протекании этих реакций. Укажите роль среды в реакции гидролиза. Ответ 1. Уравнения реакций взаимодействия D-маннозы с СН3I и СН3ОН и гидролиза полученных продуктов.
2. Отличие в протекании этих реакций: при действии на маннозу СН3I и Ag2O можно получить пентаметилманнозу, при действии СН3ОН и HCl реагирует только один гидроксил. Причина этого в том, что полуацетальный гидроксил по своим реакционным свойствам отличается от четырех других. В результате алкилирования манноза теряет свои альдегидные свойства. Частичный гидролиз пентаметилманнозы в кислой среде приводит к тетраметилманнозе (гидролизуется только эфир, образованный с участием полуацетального гидроксила). Освобождение полуацетального гидроксила способствует восстановлению альдегидных свойств моносахарида. Дальнейший гидролиз приводит к получению маннозы. 3.Роль среды в реакции гидролиза –поскольку в гидролиз вступают простые эфиры маннозы и метанола, гидролиз идет только в кислой среде.
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 1221. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |