
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
В) увеличить концентрации исходных веществ в 2 раза.Стр 1 из 2Следующая ⇒ Часть III. Задачи по общей химии
Химическая термодинамика. Термохимия
1. Рассчитайте стандартную энтальпию реакции 2AgNO3(т) → 2Ag(т) + 2NO2(г) + О2(г), если DНообр(AgNO3) = -124 кДж/моль; DНообр(NO2) = +33 кДж/моль. Классифицируйте реакцию по знаку теплового эффекта. Решение. 1.В соответствии со следствием закона Гесса рассчитаем значение
.2. Так как
2. РассчитайтеDS процесса 2N2(г) + O2(г) = 2N2O(г), если Sо (N2,г) = 200 Дж/моль·К; Sо (O2,г) = 205 Дж/моль·К; Sо(N2O,г) = 219,9 Дж/моль·К. Предскажите знак DSо процесса путём анализа уравнения химической реакции. Решение. 1.В соответствии со следствием закона Гесса рассчитаем значение
=2*219,9-(2*200+1*205)=-165,2дж/К 2.Согласно стехиометрии уравнения синтеза оксида азота(I) реакция протекает с уменьшением объема системы. Если в реакцию вступало три моля газов, то получено только два моля. Уменьшение объема системы всегда сопровождается уменьшением энтропии системы, что и показывают расчеты: 3. ОпределитеDGо298 реакции Fe3O4 + 4CO = 3Fe + 4CO2, если: DGо298 (Fe3O4) = -1014 кДж/моль, DGо298 (CO) = - 137,2 кДж/моль, DGо298 (CO2) = -394 кДж/моль. Установите возможность самопроизвольного протекания процесса в стандартных условиях. Решение. 1.В соответствии со следствием закона Гесса рассчитаем изменение изобарно-изотермического потенциала
2.Так как значение
Химическая кинетика. Химическое равновесие 
4. Напишите кинетические уравнения следующих реакций: а) С + О2 = СО2 б) 2NOCl(г) = 2NO(г) + Cl2(г) в) C12H22O11 + H2O = 2C6H12O6 г) 2NO + H2 = N2O + H2O. Объясните причину несовпадения молекулярности и порядка реакции. Решение. 1.Кинетические уравнения отражают взаимосвязь между концентрациями исходных веществ, находящихся в одной фазе, и скоростью реакции. Теоретической основой для написания кинетических уравнений является закон действующих масс (ЗДМ), согласно которому скорость реакции прямо пропорциональна произведению концентраций реагирующих веществ, в степенях, равных их стехиометрическим коэффициентам. В соответствии с ЗДМ кинетические уравнения рассматриваемых реакций выглядят следующим образом: А) С + О2 = СО2 V=k*C(O2), где V – скорость реакции, k – константа скорости реакции, C(O2) – концентрация кислорода, моль/л Б) 2NOCl(г) = 2NO(г) + Cl2(г) V=k*C(NOCl)2, где V – скорость реакции, k – константа скорости реакции, C(NOCl) – концентрация NOCl, моль/л В) C12H22O11 + H2O = 2C6H12O6 V=k*C(C12H22O11)*C(H2O), где V – скорость реакции, k – константа скорости гидролиза сахарозы C12H22O11, C(C12H22O11) – концентрация сахарозы в водном растворе ,моль/л, С (Н2О) –концентрация воды, моль/л. Г) 2NO + H2 = N2O + H2O. V=k*C(NO)2*C(H2), где V – скорость реакции, k – константа скорости, C(NO) – концентрацияNO,моль/л, С (Н2) –концентрация водорода, моль/л. 2.Причина несовпадения молекулярности и порядка реакции Молекулярность реакции определяется числом частиц реагентов, взаимодействующих друг с другом в одной элементарной (простой) реакции и превращающихся в продукты. Порядок реакции по данному веществу — показатель степени при концентрации этого вещества в кинетическом уравнении реакции. Основными причинами несовпадения молекулярности и порядка реакции могут являться: простое несовпадение ( поскольку молекулярность- характеризует механизм, а порядок - кинетику реакции), 5. Установите, как изменится скорость химической реакции 2NO + H2 = N2O + H2O, если: а) уменьшить объем реакционной смеси в 2 раза; б) уменьшить давление в 2 раза; в) увеличить концентрации исходных веществ в 2 раза. Решение. 1. Составим кинетическое уравнение реакции: V=k*C(NO)2*C(H2) 2.После уменьшения объема реакционной смеси в 2 раза концентрации реагентов увеличатся тоже в два раза. Тогда кинетическое уравнение примет вид: V/=k*(2C(NO))2*(2C(H2))=22*2 V=8 V. Как видно из расчетов, после уменьшения объема реакционной смеси в 2 раза скорость реакции возрастет в 8 раз. 3. Уменьшение давления в 2 раза приведет к соответствующему уменьшению концентраций реагентов. Кинетическое уравнение примет вид: V//=k*(1/2C(NO))2*(1/2C(H2))=(1/2)2*(1/2) V=1/8 V Из расчетов следует, что после уменьшения давления реакционной смеси в 2 раза скорость реакции уменьшится в 8 раз. 4.Увеличение концентраций исходных веществ в 2 раза приведет к эффекту, аналогичному при соответствующем уменьшении объема системы: V///=k*(2C(NO))2*(2C(H2))=22*2 V=8 V Т.о, после увеличения концентраций исходных веществ в 2 раза скорость реакции возрастет в 8 раз
6. Объясните, как влияет повышение температуры, давления и концентрации исходных веществ на экзотермическую реакцию синтеза аммиака из простых веществ. Решение. 1. Запишем уравнение реакции синтеза аммиака из простых веществ: N2 (г)+3H2(г)=2NH3(г) Данная реакция является обратимой, гомогенной (все реагенты – газы,), протекает с уменьшением объема (в реакцию вступает 4 объема исходных газов-реагентов, получается 2 объема газообразного продукта). 2. Повышение температуры, давления и концентрации исходных веществ будет влиять на рассматриваемую реакцию в соответствии с законом Ле-Шателье: Если на систему, находящуюся в химическом равновесии, подействовать извне, то равновесие сместится в сторону реакции, компенсирующей внешнее воздействие. 3. Повышение температуры будет смещать равновесие в сторону обратной эндотермической реакции, протекающей с поглощением тепла. 4. Повышение давления будет смещать равновесие в сторону прямой реакции, протекающей с уменьшением объема реакционной смеси, т.е., с уменьшением давления. 5. Повышение концентраций исходных веществ(азота и водорода) будет смещать равновесие в сторону прямой реакции, ведущей к уменьшению этих концентраций. 6.Таким образом, из рассмотренных факторов повышение давления и концентраций исходных веществ будет благоприятно влиять на экзотермическую реакцию синтеза аммиака из простых веществ, способствовать увеличению ее выхода. Напротив, повышение температуры будет способствовать уменьшению выхода прямой реакции. 7. В биологическом полимере (белке) имеет место следующее превращение: нативное состояние ↔ денатурированное состояние, |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 335. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
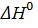 (реакции):
(реакции):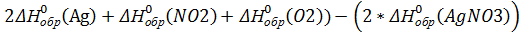 =(2*0+2*33)-2*(-124)=314 кДж
=(2*0+2*33)-2*(-124)=314 кДж (реакции):
(реакции): =
=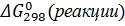
 (реакции)=(
(реакции)=(  =(3*0+4*(-394))-(1*(-1014)+4*(-137,2))=-13,2 кДж
=(3*0+4*(-394))-(1*(-1014)+4*(-137,2))=-13,2 кДж 0
0