
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Формирование исходных данныхСтр 1 из 4Следующая ⇒ Введение Взрыв – это освобождение большого количества энергии в ограниченном объеме за короткий промежуток времени. Он приводит к образованию сильно нагретого газа (плазмы) с очень высоким давлением, который при моментальном расширении оказывает механическое воздействие (давление, разрушение) на окружающие тела. Кроме того, высвободившаяся энергия проявляется в виде тепла, света, звука, хотя в ряде случаев могут наблюдаться не все указанные формы. Взрыв в твердой среде сопровождается ее разрушением и дроблением, в воздушной или водной – вызывает образования воздушной или гидравлической ударных волн, которые и оказывают разрушающее воздействие на помещенные в них объекты. Взрывы происходят за счет освобождения химической энергии, внутриядерной энергии (ядерный взрыв), электромагнитной энергии (искровой разряд, лазерная искра), механической энергии (при падении метеоритов на поверхность Земли и др.), энергии сжатых газов (при превышении давлением предела прочности сосуда – баллона, трубопровода и т.п.). Говоря о высвобождении химической энергии взрыв следует рассматривать как чрезвычайно быстрое горение с образованием сжатых газов, способных производить механические разрушения. Взрыв топливно-воздушных смесей относится к классу химических взрывов. Взрыв ТВС возникает при утечке газа либо испарении горючих жидкостей в ограниченных пространствах (помещениях), где быстро накапливается концентрация горючих элементов до предельной, при которой может произойти воспламенение облака. Взрывы ТВС могут происходить: - в помещениях вследствие утечки газов из бытовых приборов;  - Вёмкостях их хранения и транспортировки (спец. резервуарах, газгольдерах, цистернах, танках — грузовых отсеках танкеров); - в глубинных горных выработках; - в природной среде вследствие повреждений трубопроводов, труб буровых скважин, при интенсивных утечках сжиженных и горючих газов.
Характеристика горючего вещества
Окись этилена (этилен оксид, оксиран, 1,2-эпоксиэтан) — органическое химическое гетероциклическое вещество, химическая формула C2H4O. При нормальных условиях — бесцветный газ с характерным сладковатым запахом. Производное этилена и представляет собой простейший эпоксид — трёхчленный гетероцикл в кольцевой молекуле которого содержатся один атом кислорода и два атома углерода. Благодаря особенностям электронной структуры молекулы, окись этилена легко вступает в реакции присоединения с раскрытием гетероцикла, и, поэтому, легко подвергается полимеризации. Смесь паров вещества с воздухом является чрезвычайно огне- и взрывоопасной. Окись этилена обладает дезинфицирующими свойствами, то есть, является сильным ядом для большинства известных микроорганизмов и даже в газообразном виде, что используется для газовой стерилизации, например, одноразовых медицинских шприцов.Также является медленно действующим сильным ядом для теплокровных животных и человека, проявляя канцерогенное, мутагенное, раздражающее и наркотическое действие. Окись этилена является одним из важных веществ в основном органическом синтезе и широко используется для получения многих химических веществ и полупродуктов, в частности этиленгликолей, этаноламинов, простых и сложных гликолевых и полигликолевых эфиров и прочих соединений. В химической промышленности окись этилена получают прямым окислением этилена в присутствии серебряного катализатора. Физические свойства. Окись этилена — бесцветный газ (при 25 °C) или подвижная жидкость (при 0 °C) с характерным эфирным сладковатым запахом, ощутимым при концентрации в воздухе свыше 500 частей на миллион. Хорошо растворима в воде, спирте, эфире и многих других органических растворителях. Температура кипения: 10,7 °C; температура плавления: −111,3 °C; плотность жидкой окиси этилена при температуре 10 °C относительно воды при той же температуре: 0,8824. Благодаря особенностям молекулярной структуры, окись этилена является весьма реакционноспособным соединением и легко вступает в реакции с различными соединениями с разрывом C-O связи и раскрытием цикла. Для соединения наиболее характерны реакции с нуклеофилами, проходящие по механизму SN2 как в кислой (слабые нуклеофилы: вода, спирты), так и щелочной среде (сильные нуклеофилы: OH−, RO−, NH3, RNH2, RR’NH и пр.).
Формирование исходных данных
Определение массы горючего газа, участвующего во взрыве проводится согласно Приложению 3 Федеральных норм и правил в области промышленной безопасности «Общие правила взрывобезопасности для взрывопожароопасных химических, нефтеперерабатывающих производств». В общем случае, для неорганизованных парогазовых облаков в незамкнутом пространстве с большой массой горючих веществ, доля участия во взрыве может приниматься равной 0,1. Таким образом, масса окиси этилена, содержащегося в облаке топливно-воздушной смеси (ТВС)равна: Mг =0.1*М=0.1*30=3(т).
Определение эффективногоэнергозапаса ТВС проводится по формуле:
или
где
1) Средняя концентрация горючего вещества в смеси может приниматься как концентрация соответствующая нижнему концентрационному пределу воспламенения горючего газа.
2) Теплота сгорания горючего газа qг в ТВС берется из справочных данных или оценивается по формуле:
где
Справочная удельная теплота сгорания для окиси этилена Для расчета принимаем 3) Стехиометрическая концентрация вещества в смеси с воздухом:
где
Так как
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 339. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 , (1)
, (1) (2)
(2) ,
,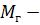 масса горючего вещества, кг;
масса горючего вещества, кг; удельная теплота сгорания горючего газа,
удельная теплота сгорания горючего газа, 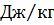 ;
; концентрация горючего в смеси,
концентрация горючего в смеси,  ;
; Стехиометрическая концентрация вещества в смеси с воздухом,кг⁄м3;
Стехиометрическая концентрация вещества в смеси с воздухом,кг⁄м3; .
. , (3)
, (3) корректировочный параметр,характеризующий фугасные свойства ТВС.
корректировочный параметр,характеризующий фугасные свойства ТВС. ;
; .
. [2].
[2]. , (4)
, (4)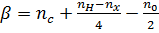 , (5)
, (5) число атомов углерода, водорода, галогена и кислорода в молекуле вещества;
число атомов углерода, водорода, галогена и кислорода в молекуле вещества; ,
, .
.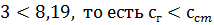 , то эффективный энергозапас горючей смеси определяем по формуле:
, то эффективный энергозапас горючей смеси определяем по формуле:
 .
.