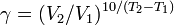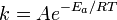Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Зависимость скорости реакции от температуры. Температурный коэффициент реакции и его особенности для биохимических процессов. уравнение Аррениуса.Стр 1 из 11Следующая ⇒ Зависимость скорости химической реакции от концентрации реагентов. Кинетические уравнения реакция первого, второго и нулевого порядков. Скорость гомогенной хим. реакции определяется изменением концентрации реагирующих веществ (или продуктов реакции) в единицу времени. Скорость прямой реакции уменьшается по мере расходования исходных веществ, а скорость обратной реакции увеличивается по мере накопления продуктов реакции. Когда скорости прямой и обратной реакции сравняются, система перейдет в состояние химического равновесия. Истинная скорость в любой момент времени является только положительной величиной и определяется первой производной концентрации по времени V= - Средняя скорость : Vср = Зависимость скорости хим.реакции от концентрации описывается кинетическим уравнением. Порядок реакции показывает, каким образом скорость реакции зависит от концентрации реагентов. Порядок кинетического уравнения может принимать значения 0,1,2 и 3; он может быть также дробным. Уравнения нулевого порядка:
С0 – с1= kt ;
C0-0.5 C0=kt0.5 ;
T0.5=
Где с0 – начальная концентрация реагента; с1 – концентрация реагента в момент времени t; k – константа скорости реакции; T0.5 – период полураспада. Уравнения первого порядка:
ln=
T0.5=
Где ct=0.5 c0 Уравнения второго порядка:
T0.5= Закон действующий масс(Закон Гульберта и Вааге): скорость химической реакции пропорциональна произведению концентраций реагирующих веществ в степени их стехиометрических коэффициентов. Т.е. чем больше концентрация, тем больше скорость хим.реакции. 
Зависимость скорости реакции от температуры. Температурный коэффициент реакции и его особенности для биохимических процессов. уравнение Аррениуса. Правило Вант-Гоффа: при повышении температуры на 10 градусов скорость гомогенной хим.реакции увеличивается в 2-4 раза.
где V2 — скорость реакции при температуре Т2, V1— скорость реакции при температуре Т1, Из уравнения Вант-Гоффа температурный коэффициент вычисляется по формуле:
Теория активных соударений обобщает закономерности зависимости скорости хим.р-и от температуры: 1.Реагировать могут не все молекулы, а только находящиеся в особом активном состоянии 2.Активация молекулы происходит в результате биомолекулярного столкновения. 3.При столкновении частиц с примерно одинаковым запасом энергии происходит её перераспределение, в результате чего энергия одной из молекул достигает значения, соответствующего энергии активации. 4.Влияние температуры на скорость реакции: смещение равновесия между обычными и активными молекулами в сторону увеличения концентрации первых.
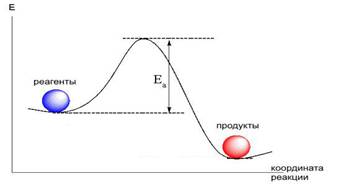
Энергетический профиль реакции (график зависимости потенциальной энергии от координаты реакции)
Энергия активации Еа – минимальная дополнительная энергия, которую необходимо сообщить молекуле сверх среднего её значения для того, чтобы стало возможным хим. взаимодействие. Уравнение Аррениуса устанавливает зависимость константы скорости химической реакции k от температуры Т.
Здесь А характеризует частоту столкновений реагирующих молекул, R — универсальная газовая постоянная. |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 344. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
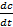 . Если измерение истинной скорости проводят по изменению концентрации исходных веществ, то перед производной ставят знак минус:
. Если измерение истинной скорости проводят по изменению концентрации исходных веществ, то перед производной ставят знак минус: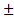
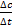
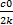 ;
;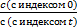 = - kt ;
= - kt ;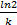 =
= 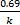 ;
;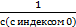 -
- 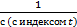 = kt;
= kt;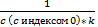 ;
;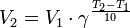
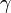 — температурный коэффициент реакции (если он равен 2, например, то скорость реакции будет увеличиваться в 2 раза при повышении температуры на 10 градусов).
— температурный коэффициент реакции (если он равен 2, например, то скорость реакции будет увеличиваться в 2 раза при повышении температуры на 10 градусов).