Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
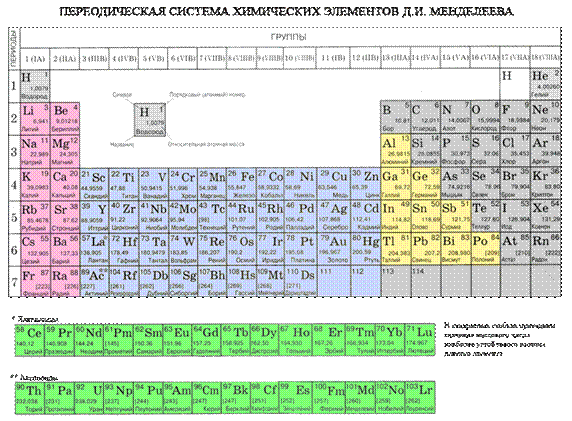
Положение металлов в Периодической системе элементов Д.И. МенделееваВ Периодической системе химических элементов Д.И. Менделеева металлы располагаются ниже диагонали бериллий – астат. Элементы, расположенные вблизи диагонали, например, бериллий, алюминий, титан, германий, сурьма обладают двойственным характером и относятся к металлоидам. Металлы располагаются в начале периодов, к ним относятся s-элементы 1 и 2 групп, р-элементы 13 группы, все, кроме бора, 14 группы: германий, олово, свинец, 15 группы: сурьма, висмут, а также все d- и f- элементы.
64вопрос Полумета́ллы (металлоиды) — химические элементы, расположенные в периодической системе на границе между металлами и неметаллами. Для них характерно наличие ковалентной кристаллической решётки и металлической проводимости. В физике твёрдого тела полуметаллами называются различные вещества, занимающие по электрическим свойствам промежуточное положение между металлами и полупроводниками. К полуметаллам относят кремний, бор, германий, мышьяк, сурьму, теллур, иногда — висмут, полоний[1][2] и астат, а также олово, имеющее полупроводниковую форму, и аллотропные модификации углерода — графит и фосфора — металлический фосфор. Вероятно, теннессин также является полуметаллом[3]. По своим химическим свойствам элементы бор, кремний, мышьяк и теллур являются неметаллами, но германий и сурьма наряду с неметаллическими свойствами обладают и металлическими (например, реагируют с кислотами с образованием солей). По типу проводимости бор, кремний, германий и теллур относятся к полупроводникам, а мышьяк и сурьма обладают металлической проводимостью. Расплавы германия и кремния так же обладают металлической проводимостью. По своим внешним характеристикам ярко выраженными признаками металлов (характерный блеск, цвет) обладают германий, сурьма и теллур, у бора, кремния и мышьяка они выражены гораздо слабее. Для всех простых веществ данных элементов характерно кристаллическое строение, высокая твёрдость и хрупкость.  В отличие от полупроводников полуметаллы обладают электрической проводимостью вблизи абсолютного нуля температуры, в то время как полупроводники (тем более диэлектрики) в этих условиях — изоляторы[4]. Характерной особенностью полуметаллов является слабое перекрытие валентной зоны и зоны проводимости, что приводит, с одной стороны, к тому, что полуметаллы остаются проводниками электрического тока вплоть до абсолютного нуля температуры, а с другой стороны — с повышением температуры число носителей тока (электронов и дырок) возрастает, но всё-таки остаётся небольшим, достигая концентрации 1018—1020 см−3, или 10−3 на атом. Носители тока в полуметаллах отличаются большой подвижностью и малой эффективной массой. Благодаря этому полуметаллы — наиболее подходящие объекты для наблюдения размерных эффектов, фазовых переходов полуметалл — диэлектрик в сильных магнитных полях и ряда других явлений.
Немета́ллы — химические элементы с типично неметаллическими свойствами, которые занимают правый верхний угол Периодической системы. Расположение их в главных подгруппах соответствующих периодов следующее:
Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов на внешнем энергетическом уровне их атомов. Это определяет их большую способность к присоединению дополнительных электронов, и проявлению более высокой окислительной активности, чем у металлов. Неметаллы имеют высокие значения сродства к электрону, большую электроотрицательность и высокий окислительно-восстановительный потенциал. Благодаря высоким значениям энергии ионизации неметаллов, их атомы могут образовывать ковалентные химические связи с атомами других неметаллов и амфотерных элементов. В отличие от преимущественно ионной природы строения соединений типичных металлов, простые неметаллические вещества, а также соединения неметаллов имеют ковалентную природу строения. В свободном виде могут быть газообразные неметаллические простые вещества — фтор, хлор, кислород, азот, водород, инертные газы, твёрдые — иод, астат, сера, селен, теллур, фосфор, мышьяк, углерод, кремний, бор, при комнатной температуре в жидком состоянии существует бром. У некоторых неметаллов наблюдается проявление аллотропии. Так, для газообразного кислорода характерны две аллотропных модификации — кислород (O2) и озон (O3), у твёрдого углеродамножество форм — алмаз, астралены, графен, графит, карбин, лонсдейлит, фуллерены, стеклоуглерод, диуглерод, углеродные наноструктуры (нанопена, наноконусы, нанотрубки, нановолокна) и аморфный углерод уже открыты, а ещё возможны и другие модификации, например, чаоит и металлический углерод. В молекулярной форме в виде простых веществ в природе встречаются азот, кислород и сера. Чаще неметаллы находятся в химически связанном виде: это вода, минералы, горные породы, различные силикаты, фосфаты, бораты. По распространённости в земной коре неметаллы существенно различаются. Наиболее распространёнными являются кислород, кремний, водород; наиболее редкими — мышьяк, селен, иод.
65 вопрос. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 397. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |