
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Идеальный газ и его свойстваЗАДАЧИ ПО ТЕХНИЧЕСКОЙ ТЕРМОДИНАМИКЕ Тема 1.1 Параметры состояния Задача 1 В сосуде объемом V= 1,4 м3 находитсяm = 2,4 кг воздуха.Определить его удельный объем о и плотность Решение Удельный объем воздуха составляет υ= Плотность воздуха равна
Ответ: υ = 0,583 м3/кг; Задача 2 Избыточное давление в паровом котле измеряется пружинным манометром и составляет ри = 9800 кПа. Барометрическое давление по ртутному барометру составляет рбар0 = 770 мм.рт.ст. при температуре 0°С. Определить абсолютное давление пара в котле р в кПа, Па, МПа, барах. Решение Барометрическое давление, выраженное в Па, составляет [1] Рбар0 = 770*133,322 = 102658 Па, или Рбар0=
Абсолютное давление пара в котле равно р =ри +рбар° = 9800 + 102,7 = 9902,7 кПа, или р = 9902,7*103 = 9902700 Па, или р = или р =
Ответ: 9902,7 кПа; 9902700 Па; 9,9 МПа; 99 бар.
Задача 3
Избыточное давление в сосуде, измеряемое пружинным манометром p = 1,0 МПа. Атмосферное давление но ртутному барометру при t= 20°Ссоставляет pбар° = 760 мм.рт.ст. Определить абсолютное давление в сосуде в МПа, Па, барах. Решение Приведем показания ртутного барометра к 0°С по формуле [1, с. 7] рбар°=Рбар20(1-0,000172t). Подставив численные значения, получим: рбар° = 760 (1 - 0,000172*20) = 757,4 мм.рт.ст. Барометрическое давление, выраженное в Па, составляет [1] рбар° = 757,4*133,322 = 100976 Па, или рбар°= Абсолютное давление в сосуде равно р = ри + рбар° = 1,0 + 0,101 = 1,101 МПа, или р= 1,101*106 Па, или р=
Ответ: 1,101 МПа; 1,101*106 Па; 11,01 бар. Задача 4 Ртутный вакуумметр, присоединенный к конденсатору паровой турбины, Показывает разрежение рв40= 300 мм.рт.ст. при температуре t1 = 40°С. Атмосферное давление по ртутному барометру pбар20 =750 мм.рт.ст. при t2 = 20°С.  Определить абсолютное давление р в конденсаторе в мм.рт.ст., Па, барах. Решение Приведем показания ртутных приборов к 0°С по формуле [1, с. 7] p0=pt(1 -0,000172t). Подставив численные значения, получим: -ртутный вакуумметр рв0 = 300* (1 - 0,000172*40) = 297,9 мм.рт.ст.; -ртутный барометр pбар0 = 750*(1 - 0,000172*20) = 747,4 мм.рт.ст. Абсолютное давление в конденсаторе равно p=pбар0 - рв0 = 747,4 - 297,9 = 449,5 мм.рт.ст., или р = 449,5*133,322 = 59928 Па, или р =
Ответ: 449,5 мм.рт.ст.; 59928 Па; 0,599 бар.
Закон сохранения энергии Задача 5 Сколько килограммов свинца mс можно нагреть от температуры t1 = 30°С до температуры плавления t2 = 327 °С посредством удара молотом массой mм = 250 кг при падении его с высоты hм = 3 м? Предполагается, что вся энергия падения молота превращается в теплоту, которая поглощается свинцом. Теплоемкость свинца ср = 0,1256 кДж/(кг*К). Решение Энергия падения молота составляет Э = mмghм = 250*9,81*3 = 7357,5 Дж. По условиям эта энергия полностью превращается в теплоту, т.е. Q = Э = 7357,5 Дж. Массу свинца, которую можно нагреть этим количеством теплоты, определим из уравнения теплового баланса mс= или mс = 197 г. Ответ: 197 г. Задача 6 Современная паротурбинная электростанция мощностью N = 600 МВт работает в году τ= 320 суток с КПД η = 0,34. Теплота сгорания топлива Определить су точный Всут и годовой Вг расходы топлива. Решение Суточный расход топлива составляет Всут = Годовой расход топлива равен Вг = Bсут = 16,43*320 = 5257,6 т/год. Ответ: 16,43 т/сут.; 5257,6 т/год. Задача 7 Определить годовой расход ядерного горючего на АЭС той же мощности, что и в предыдущей задаче, если 1 кг урана при расщеплении выделяет ( Решение Годовой расход ядерного горючего на АЭС составляет Всут =
Ответ: 1,85 кг/сут. Задача 8 При испытании двигателей для определения мощности необходимо их тормозить гидротормозом. При этом работа, произведенная двигателем, расходуется на преодоление сил трения и превращается в теплоту, часть которой (примерно 20 %) рассеивается в окружающей среде, а остальная часть отводится с охлаждающей тормоз водой Сколько воды необходимо подводить к тормозу Gвза 1 час, если крутящим момент на валу Мкр = 150Дж, частота вращения n= 2500 об/мин, адопустимое повышение температуры воды Δt = 45 К. Теплоемкость воды ср = 4,19 кДж/(кг*К) Решение Мощность на валу двигателя определим по формуле N= Количества тепла отводимого водой составляет Q=0,8*N=0,8*39270=31416 Вт Часовой расход воды на охлаждения тормоза определим из уравнениятеплового баланса Gв= или Gв = 3600*0,167 Ответ: 600 кг/ч. Идеальный газ и его свойства Задача 9 Определить среднюю изохорную теплоемкость сυдиоксида серы (SO2) в интервале температур t1= 150 °С и t2 = 900°С, пользуясь таблицами средних теплоемкостей. Решение Среднюю изохорную теплоемкость S02 в рабочем интервале температур, определим по формуле [2]
где интервалах температур от 0 до 150°С [2, табл. VI]; Подставив численные значения, получим.
Ответ: 0,67 кДж/(кг*К). Задача 10 Определить теплоту, подведенную к азоту (N2) при p = const, если его температура изменяется от t1 = 600oС доt2= 850°С а) Масса газаm = 1,6 кг б) Объем газа при температуре t1 = 600oС равен V1 = 3,5 м3. Решение Среднюю изобарную теплоемкость N2, в рабочем интервале температур определим по формуле [2], ср.ср= где Подставив численные значения, получим:
Теплоту, подводимую в изобарном процессе к N2по пункту а) определим по формуле [2] Q = mср.ср( Подставив численные значения, получим: Q= 1,6 *1,1664 (850-600) =466,6кДж. Для определения массы газа по пункту б) найдем: -объем газа V2 при температуре
-газовую постоянную для азота
где μ= 28 кг/кмоль - мольная масса газа; - давление водяного пара, используя выражения для работы расширения в изобарном процессе
- массу водяною пара в процессе из уравнения состояния идеального газа
Теплота, подводимая к N2 по пункту б), по формуле (1) составляет Q= 1,1664*(850-600) = 291,6кДж. Ответ: а) 466,6 кДж; б) 291,6 кДж.
Задача 11 Газовая смесь состоит из mN2 = 5 кг, азота, mсо2= 4 кг углекислого газа = 1 кг окиси углерода. Начальные параметры смеси р1 = 1 МПаиt1= 57 °С. В процессе T= const смесь расширяется до давления p2 = 0,5 МПа. Определить: -работу расширения смеси L; -количество подведенной теплоты Q; -объем в конце расширения V2; -парциальные давления газов в начальном состоянии; -изменение внутренней энергии -построить процесс в р-υи T-s диаграммах. Решение Объемную концентрацию компонентов газовой смеси определим обшей формуле [2]
где В нашем случае имеем:
Подставив численные значения, получим.
Проверка
58,5 + 29,8 + 11,7 = 100%.
Средняя молекулярная масса смеси составляет:
Газовая постоянная смеси равна [2]
Абсолютная температура изотермического процесса расширения газовойсмеси Т = T1 = Т2 = t1 + 273 = 57 + 273 = 330 К. Масса газовой смеси равна mсм = Работа изотермического расширения газовой смеси составляет L = mсмRсмТ1ln В процессе изотермического расширения газовой смеси количество подведенной теплоты в соответствии с первым законом термодинамики равно Q = L = 580,3 кДж. Объем газовой смеси в начале изотермического процесса расширения из уравнения состояния идеального газа составляет
Объем газовой смеси в конце изотермического процесса расширения по закону Бойля - Мариотта [2] равен
Парциальные давления составляющих газовой смеси в начальном состоянии определим по формуле [2] p1i=ripi Подставив численные значения, получим:
pN2= pCO2 = pCO =
Изменение внутренней энергии
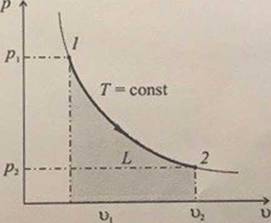
p-υ иT-s диаграммы процесса изотермического расширения газовой смеси приведены на рисунках 1 и 2
Рисунок 1- p-υ диаграмма расширения газа при T = const
Рисунок 2- T-sдиаграмма расширения газа при T = const
Задача 12 Сосуд вместимостью V1=400 л содержит кислород (О2) при абсолютном давлении р1= 1 МПа и температуре = 37°С. Определить: - массу газа; - конечную температуру, изменение энтропии и количество теплоты, которое необходимо подвести, чтобы повысить давление в процессе при постоянном объеме (υ = const) до p2 = 2 МПа; - изменение внутренней энергии и энтальпии газа; - построить процесс в p-υ иT-sдиаграммах. Удельную теплоемкость принять переменной. Решение Газовая постоянная кислорода равна [2]
где μ = 32 кг/кмоль - мольная масса кислорода. Абсолютная температура кислорода в начальный момент равна Т1 = t1 + 273 = 37 + 273 = 310 К. Масса кислорода в сосуде из уравнения состояния идеального газа составляет
Конечную температуру кислорода в процессе изохорного повышения давления до р2= 2 МПа определим по закону Шарля [2]
t2 = 620 - 273 = 347 °С.
Среднюю изохорную теплоемкостьO2 в рабочем интервале температур, определим по формуле [2]
где Средние изохорные теплоемкости O2 в интервалах температур от 0 до соответствующей рабочей температуре определим используя справочные данные [2, табл. VI] -интервал от 0 до 37°С
-интервал от 0 до 347°С
Подставив численные значения в формулу (1), получим:
Изменение энтропии в изохорическом процессе составляет
Количество теплоты, которое необходимо подвести, чтобы повысить давление в процессе при постоянном объеме (υ= const) до p2=2 МПа равно
Изменение внутренней энергии в изохорическом процессе в соответствии с Первым законом термодинамики равно количествуподведенной теплоты
Средняя изобарная теплоемкость O2 в рабочем интервале температур поформуле Майера составляет [2] cp=cυ + R = 0,7018 + 0,260 = 0,9618 кДж/(кг*К). Изменение энтальпии газа в изохорическом процессе равно
p-υ иT-s диаграммы процесса изохорного процесса повышения давления газа приведены на рисунках 3 и 4.
Рисунок 3 - p-υ диаграмма газа при υ=const
Рисунок 4- T-sдиаграмма газа при υ=const Задача 13 В цилиндре двигателя объемом V1=350 л находится газ со свойствами воздуха при абсолютном давлениир1= 2,5 МПа и температуре t1= 1500°С. От воздуха отводится теплота при постоянном давлении (р = const) до температуры t2= 400°С. Определить: - массу воздуха; - конечный объем; - изменение внутренней энергии; - количество отнятой теплоты; - изменение энтальпии; - работу сжатия; - изменение энтропии; - построить процесс в р-ь и T-s диаграммах. Теплоемкость считать переменной. Решение Газовая постоянная воздуха равна [2]
где μ = 29 кг/кмоль - мольная масса воздуха. Абсолютная температура воздуха T1 = t1 + 273 = 1500 + 273 = 1773 К, T2 = t2+ 273 = 400 + 273 = 673 К. Масса воздуха в цилиндре из уравнения состояния идеального газа составляет
Конечный объем воздуха в процессе изобарического отвода тепла определим по закону Гей-Люссака [2]
Среднюю изохорную теплоемкость воздуха в рабочем интервале температур, определим но формуле [2]
где Подставив численные значения в формулу (2), получим:
Изменение внутренней энергии в изобарическом процессе отвода тепла от воздуха в цилиндре двигателя составляет
Средняя изобарная теплоемкость воздуха в рабочем интервале температур по формуле Майера [2] равна
cp=cυ + R = 0,8814 + 0,287 = 1,16848 кДж/(кг*К). Количество отнятой теплоты в изобарном процессе составляет Q = Изменение энтальпии воздуха при изобарном отводе тепла в цилиндре двигателя равно
Работа сжатия в процессе изобарного отвода тепла составляет L = Проверим по первому закону термодинамики Q = -2210,3 =(-1667,6) + (-542,7). Изменение энтропии в процессе изобарического отвода тепла составляет
p-υ иT-s диаграммы изохорного процесса повышения давления газа приведены на рисунках 5 и6 Рисунок 5 - p-υ диаграмма газа при p =const
Рисунок 6 -T-sдиаграмма газа при p =const Задача 14 В компрессор ГTУ входит m = 6,5 кг воздуха с начальными параметрами р1 = 0,12 МПа и t1= 27 °С. Воздух сжимается адиабатно дор2= 1,2 МПа. Определить: - начальный и конечный объемы; - конечную температуру; - работу сжатия; - располагаемую работу сжатия; - изменение внутренней энергии, энтальпии и энтропии; - построить процесс в р-м и T-s диаграммах. Теплоемкость принять постоянной. Решение Газовая постоянная воздуха равна [2]
где μ = 29 кг/кмоль - мольная масса воздуха. Абсолютная температура воздуха T1 = t1 + 273 = 27 + 273 = 300 К. Начальный объем воздуха из уравнения состояния идеального газа составляет
Конечный объем воздуха определим из соотношения
где k= 1,4 - показатель адиабаты для воздуха, как двухатомного газа [2].
Решая (1), получим конечный объем воздуха.
Конечная температура воздуха из уравнения состояния идеального газасоставляет
Работа адиабатического сжатия воздуха в ГТУ составляет
L =
Изохорную теплоемкость воздуха определим по формуле [2] Cυ= Изменение внутренней энергии в адиабатном процессе равно
Проверим по первому закону термодинамики для адиабатного процесса(Q= 0) Q = 0 =1301 - 1301. Изобарную теплоемкость воздуха определим по формуле cp = Изменение энтальпии в адиабатном процессе составляет
Располагаемая работа сжатия для адиабатического процесса равна Lрасп= - Изменение энтропии для адиабатического процесса составляет
p-υ иT-s диаграммыадиабатного сжатия воздуха в ГТУ приведены рисунках 7 и 8.
Рисунок 7- p-υ диаграмма адиабатного сжатия в ГТУ (q= 0) Рисунок 8- T-sдиаграмма адиабатного сжатия в ГТУ (q=0) Задача 15 Определить теоретическую работу на привододноступенчатого и 4-ступенчатого с промежуточным охлаждениемкомпрессоровпри сжатии воздуха от давления р1 = 0,1 МПа до р2= 8, 1 МП, если начальная температура t1 = 17 °С Показатель политропы для всех ступеней принять равнымиn=1,22. Начальный объем таза V1 = 1000 м3 Сравнить величину работы одно- и 4-ступенчатото сжатия Определить температуры в конце сжатия. Построить процесс вp-υ иT-sдиаграммах. Решение Теоретическую работу на привод одноступенчатого компрессора при политропическом сжатии определим по формуле [2] L = Подставив численные значения, получим: L = Степень увеличения давления в каждой ступени 4-ступенчатого компрессора равна [2] x= Теоретическую работу на привод одной ступени 4-ступенчатого компрессора при политропическом сжатии определим по формуле [2] L1 =
Подставив численные значения, получим.
L =
Для 4-ступенчатого компрессора имеем L=4*L1=4*1,215*108=4,86*108Дж. Как видно, теоретическая работа на привод 4-ступенчатого компрессора меньше теоретической работы на привод одноступенчатого компрессора в
Абсолютная температура воздуха Т1= t1 + 273 = 17 + 273 = 290 К.
Температуру в конце политропического сжатия в одноступенчатом компрессоре определим из соотношения [2]
T2= Температура в конце политропического сжатия каждой ступени 4-ступенчатого компрессора составляет
T2=
p-υ иT-s диаграммыполитропического сжатия воздуха в ГТУ приведенрисунках 9 и 10 Рисунок 9- Одноступенчатое сжатие
Рисунок 10- 4-ступенчатое сжатие |
|||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 1494. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
 .
. =
=  = 0,583м3/кг
= 0,583м3/кг =
=  =
= 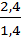 = 1,714 кг/м3.
= 1,714 кг/м3. = 1,714 кг/м3.
= 1,714 кг/м3.
 = 9,9 МПа,
= 9,9 МПа, = 99 бар,
= 99 бар, 0,101 МПа
0,101 МПа 11,01 бар
11,01 бар 0,599 бар.
0,599 бар. 0,197 кг,
0,197 кг, = 29000 кДж/кг.
= 29000 кДж/кг. =
=  = 16,43 т/сут
= 16,43 т/сут =
=  = 1,85 кг/сут.
= 1,85 кг/сут. = 39270 Вт
= 39270 Вт =
=  = 0,167 кг/с
= 0,167 кг/с 600 кг/ч.
600 кг/ч. =
= 
 = 0,520 кДж/(кг-К) - средняя изохорная теплоемкости SO2 в
= 0,520 кДж/(кг-К) - средняя изохорная теплоемкости SO2 в = 0,645 кДж/(кг*К) - средняя изохорная теплоемкость SO2 в интервалах температур от 0 до 900°С [2, табл. VI].
= 0,645 кДж/(кг*К) - средняя изохорная теплоемкость SO2 в интервалах температур от 0 до 900°С [2, табл. VI]. =
=  = 0,67 кДж/(кг*К)
= 0,67 кДж/(кг*К) =
=  = 1,1664 кДж/(кг-К).
= 1,1664 кДж/(кг-К).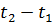 ). (1)
). (1) = 850°С по закону Гей-Люссака[2]
= 850°С по закону Гей-Люссака[2] =
=  , (2)
, (2) =
=  = 3,5*
= 3,5*  = 4,50 м3
= 4,50 м3 =
=  =
=  = 296,9 Дж/(кг*К)
= 296,9 Дж/(кг*К) =
=  =
=  = 74225 Па;
= 74225 Па; =
=  =
=  = 1 кг
= 1 кг U и энтальпии
U и энтальпии  =
= 
 - молекулярная масса компонента, кг/кмоль.
- молекулярная масса компонента, кг/кмоль. = 28 кг/кмоль;
= 28 кг/кмоль;  = 44 кг/кмоль;
= 44 кг/кмоль;  = 28 кг/кмоль.
= 28 кг/кмоль. =
=  *100= 58,5%,
*100= 58,5%, =
=  *100= 29,8%,
*100= 29,8%,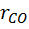 =
=  *100= 11,7%,
*100= 11,7%, = 100%,
= 100%, =
=  ,=
,=  = 32,8 кг/кмоль
= 32,8 кг/кмоль = 253,7Дж/(кг*К)
= 253,7Дж/(кг*К) = 5 + 4 +1 = 10 кг.
= 5 + 4 +1 = 10 кг. =
=  ln
ln  = 580,3 кДж.
= 580,3 кДж. =
=  =
= 
 ,
,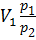 = 0,837*
= 0,837*  = 1,674м3
= 1,674м3




 = 260Дж/(кг*К)
= 260Дж/(кг*К) 4,96 кг.
4,96 кг. ,
, =
=  = 310*
= 310*  = 620 К,
= 620 К, 0,6579 кДж/(кг*К);
0,6579 кДж/(кг*К); 0,6971 кДж/(кг*К);
0,6971 кДж/(кг*К); 0,7018 кДж/(кг*К);
0,7018 кДж/(кг*К);
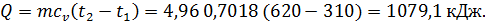
 = 1079,1 кДж.
= 1079,1 кДж. = 4,96*0,9618*(620-310)= 1478,9 кДж.
= 4,96*0,9618*(620-310)= 1478,9 кДж.

 = 287Дж/(кг*К)
= 287Дж/(кг*К) 1,72 кг.
1,72 кг. , (1)
, (1) = 0,35*
= 0,35*  = 0,1329м3
= 0,1329м3 =
=  (2)
(2) 0,8814 кДж/(кг*К);
0,8814 кДж/(кг*К); = 1,72*0,8814*(400-1500)= -1667,6 кДж.
= 1,72*0,8814*(400-1500)= -1667,6 кДж. = 2,5*106*(0,1329 - 0,35)/1000 = -542,7 кДж.
= 2,5*106*(0,1329 - 0,35)/1000 = -542,7 кДж.


 = 4,66м3
= 4,66м3 =
=  = 4,66*
= 4,66*  0,9 м3
0,9 м3 579 К
579 К =
=  = -1301 кДж.
= -1301 кДж.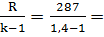 717,5 Дж/(кг*К).
717,5 Дж/(кг*К). = 6,5*0,7175*(579-300)= 1301 кДж.
= 6,5*0,7175*(579-300)= 1301 кДж. 1004.5 Дж/(кг*К).
1004.5 Дж/(кг*К). = 6,5*1,0045*(579-300)= 1822 кДж.
= 6,5*1,0045*(579-300)= 1822 кДж. H= -1822 кДж.
H= -1822 кДж. S = 0.
S = 0.

 (1)
(1) = 6,7*108Дж
= 6,7*108Дж
 (2)
(2) = 1,215*108Дж
= 1,215*108Дж 1,38 раза.
1,38 раза. , (3)
, (3) =641 K
=641 K =354 K
=354 K
