Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Задания для самостоятельной работыСтр 1 из 2Следующая ⇒ Модульная единица 1.2. «Химическая структура, биологическая роль важнейших молекул жизни. Принципы гормональной и нейромедиаторной регуляции» Занятие 1.2.8. Методические указания для студентов ТЕМА: Зачет ЦЕЛЬ: Повторить принципы самосборки важнейших биомолекул и формирования их надмолекулярных комплексов. ЗНАТЬ: Природу химических связей, определяющих вторичную и третичную структуру важнейших биополимеров и их надмолекулярных комплексов. УМЕТЬ:Прогнозировать возможность образования связей между различными фрагментами белков, белков, полиаминов и нуклеиновых кислот, липидов и антиоксидантов. ВЛАДЕТЬ: Навыками распознавания основных биологически значимых структур и фрагментов молекул, определяющих их активность. Значение изучения темы Липиды, белки, нуклеиновые кислоты существуют в организме в виде надмолекулярных комплексов (липопротеинов, нуклеопротеинов), представляющих собой по сути супрамолекулярные структуры. Особенности состава этих структур определяет их свойства. Важно иметь представление об известных супрамолекулярных структурах, возможности и принципах самоорганизации важнейших биомолекул и биополимеров. Исходный уровень 1. Вторичная структура амилозы, вторичная и третичная структура полипептидов и белков, нуклеиновых кислот. 2. Роль гидрофобных ковалентных и ионных взаимодействий фрагментов молекул липидов, белков, нуклеиновых кислот. Значение водородных связей в обеспечении третичной структуры белков, нуклеиновых кислот.
Теоретические вопросы для самостоятельного изучения темы: 
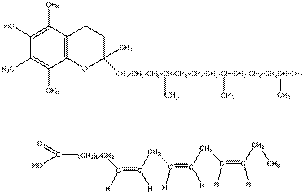
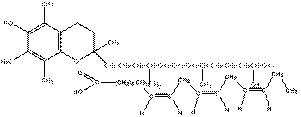
Задания для самостоятельной работы Задание 1.Вторичная структура белков обеспечивается, как правило, за счет водородной связи, образующейся между карбонильной (С=О)- группой и (N-Н)-группой амидного фрагмента, расположенных напротив друг друга в параллельных витках спирали. Изобразите схему образования водородной связи в белке, укажите группу, проявляющую основные и кислотные свойства. Задание 2.Изобразите водородные связи между комплементарными нуклеиновыми основаниями в структуре ДНК, обеспечивающие стабилизацию структуры. Задание 3.Изобразите ионизированное строение глутаминовой кислоты и лизина, проявляющих в водном растворе за счет дополнительной карбокси- и амино-групп свойства кислоты и основания. Как будут осуществляются ионные взаимодействия указанных аминокислот, включенных в белковые глобулы. Задание 4.Изобразите образование дисульфидных мостиков между SH-грппами цистеина, локализованных на поверхности белковых глобул. По такому типу связываются различные суъединицы сложных белков. Задание 5.В структуре биологических мембран высшие жирные кислоты, присутствующие в молекуле фосфолипидов в цис-форме, взаимодействуют с локализованными совместно с ними антиоксидантами, например, α-токоферолом, имеющим длинный боковой заместитель («хвост»), составленный из 3 остатков 2-метил-бутана (изопреноидное строение). Ниже приведена схема межмолекулярного связывания α-токоферола с молекулой линоленовой кислоты (индекс 18:3) по типу «пазла», когда метильная группа попадает в «карман», образованный жирной кислотой в цис-форме.
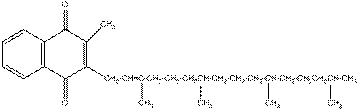
По аналогии изобразите гидрофобные взаимодействия между арахидоновой кислотой (20:4) и витамином К1
|
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 310. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |