
Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Массовая доля растворенного вещества (w)Массовая доля растворенного вещества – это отношение массы растворенного вещества (А) к массе раствора, выраженное в процентах:
mр-ра =m(A)+m(H2O) (2) Масса раствора равна сумме масс растворенного вещества и растворителя (воды). Масса раствора (г), его объем (мл) и плотность (г/мл) связаны между собой соотношением: mр-ра=ρ*Vр-ра (3) Пример 1: В 135 г воды растворено 15 г соли. Какова массовая доля соли в полученном растворе? wсоли=15*100/135+15=10%
Пример 2: Сколько граммов соли и воды потребуется для приготовления 500г раствора с массовой долей 18%
m(A)= w* mр-ра/100=18*500/100=90 г m(H2O)= mр-ра-m(A)=500-90=410 г Пример 3: 1200 г раствора соли с массовой долей 20% упарили до массы 800 г. Какова концентрация получившегося раствора? 1) Упаривание приводит к потере воды, содержание же растворенного вещества остается неизменным. Определим массу соли в растворе: m(A)= w* mр-ра/100=20*1200/100=240 г 2) Определим массовую долю соли в новом растворе: wсоли=240*100/800=30% Пример 4: Приготовить 500 г раствора KJ с массовой долей KJ 19%. Сколько соли необходимо добавить, чтобы получить 20 % раствор? 1) Определяем массу KJ в исходном растворе: m(A)= w* mр-ра/100=19*500/100=95 г 2)Обозначим массу прибавленного KJ за х, то масса раствора будет равна (500+х). Поставим эти величины в формулу (1): 20=95+х/500+х=240 х=6,25 г Молярная концентрация. Молярная концентрация – это отношение количества вещества v(A) к объему раствора V(р-ра). С(А)= v (A)/ V(р-ра) (моль/л) (4) Раствор с молярной концентрацией K2SO4C(K2SO4)=1моль/л может быть обозначен как 1 М K2SO4 – одно молярный раствор сульфата калия.  v (A)=m(A)/M(A) (5) объединяя (6) и (7) получаем: С(А)=m(A)/M(A)*V (6) Где m(A) – масса вещества (г), М(А) – молярная масса вещества (г/моль), V – объем раствора (л). Пример 5. Определить молярную концентрацию раствора KOH, в 50 мл которого содержится 5,6 г вещества. CKOH=m(KOH)/M(KOH)=5,6*1000/56*50=2 моль/л или 2 М KOH ОБЪЕКТ ИССЛЕДОВАНИЯ. При проведении лабораторной работы необходимо определить плотность приготовленного раствора. КОНТРОЛЬНЫЕ ВОПРОСЫ. 1.В 110г водного раствора содержится 56г КОН. Какова массовая доля КОН в растворе? 2.В 910г Н2О растворено 309г NaOH, плотность раствора ρ=1,3 г/мл. Найдите: а) массовую долю NaOH б) молярную концентрацию 3.Сколько кг растворителя нужно добавить к 1л раствора с молярной концентрацией См=4 моль/л, чтобы получить раствор См=0,2 моль/л. |
||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 323. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
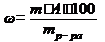 (1)
(1)