Студопедия КАТЕГОРИИ: АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция |
Расчет изменения энтропии реакцииСтр 1 из 3Следующая ⇒ Формулировка задания
Исследование 1 Для СВОЕЙ РЕАКЦИИ 1.1. Составить уравнение зависимости от температуры величины теплового эффекта ∆Н0т=f(T) и изменения энтропии ∆S0 T = f(T). 1.2. Вычислить величины ∆Ср, ∆Н0т, ∆S0т, ∆G0т и lnKp при нескольких температурах. Полученные значения используются при построении графиков в координатах ∆Ср – Т; ∆Н0т – Т; ∆S0т – Т; ∆G0т –Т; и lnKp – 1/Т. 1.3. Пользуясь графиком lnKp – 1/Т, вывести приближенное уравнение вида lnKp = А/Т + В, где А, В – постоянные. Исходные данные на примере реакции H2S(г) + CO2(г) = H2O(г) + COS(г) Исследование 1
3. Решение задания 3.1. Исследование 1 Для реакции H2S(г) + CO2(г) = H2O(г) + COS(г) Составить уравнение зависимости от температуры величины теплового эффекта ∆Н0т=f(T) и изменения энтропии ∆S0T = f(T). Вычислить величины ∆Ср, ∆Н0т, ∆S0т, ∆G0т и lnKp при нескольких температурах. Полученные значения используются при построении графиков в координатах ∆Ср – Т; ∆Н0т – Т; ∆S0т – Т; ∆G0т – Т; и lnKp – 1/Т. Для удобства последующих расчетов, составим таблицу исходных данных, используя справочный материал. Таблица 1.  Исходные данные для термодинамического исследования реакции H2S + CO2= H2O + COS
Расчет теплового эффекта реакции Зависимость теплового эффекта реакции от температуры определяется законом Кирхгофа: где: ∆Н0298 – стандартный тепловой эффект реакции при 298 К; ∆СР - изменение теплоемкости системы в результате протекания реакции. Последняя величина рассчитывается по уравнению: где Ср,i – мольная изобарная теплоемкость i-го вещества; ni – стехиометрический коэффициент i-го вещества в уравнении реакции (1). После подстановки зависимостей Ср,i в выражение (2), оно имеет вид ∆Ср,i = ∆а + ∆bТ + ∆сТ2 (3) где ∆b и ∆с рассчитываются аналогично. ∆а = а(н2о) + а(cos) – (а(н2s) + a(co2)) = 30,00+48,12-(44,14+29,31) = 78,12 – 73,51 = 4,61 Дж/моль∙К ∆b = b(н2о) + b(cos) – (b(н2s) + b(co2)) = 8,45∙10-3 +10,71∙10-3 – (9,04∙10-3 + 15,40∙10-3) = -5,28∙10-3 ∆сi = с(н2о) + с(cos) – с(co2) = -8,20∙105 + 0,33∙105 + 8,54∙105 = 0,67∙105 Значение ∆Н0298 определяется по стандартным теплотам образования ∆Н0298,i: Значения теплот образования соответствующих веществ приведены в табл. 1. После их подстановки в уравнение (5) имеем ∆Н0298 = -141,70 - 241,81 – (-393,51 – 20,60) =-383,51+417,11 = 33,6 кДж = = 33600 Дж В соответствии с заданием необходимо рассчитать тепловые эффекты в интервале температур 800 – 1700 К при шаге температуры 100 К. После подстановки значений ∆Ср из уравнения (3) в (1) получим тепловые эффекты: = 30600+((4,61Т - 2,64∙10-3 Т2 – 0,67∙105 Т-1)-(1373,78 - 243,44 – 224,83)) = =(30600 - 905,51) + 4,61Т – 0,67∙105 Т-1 – 2,64∙10-3Т2 ∆Н0т = 4,61Т – 0,67∙105Т-1 – 2,64∙10-3Т2 + 29694,49 ∆Н0800 = 4,61∙800 – 0,67∙105/800 – 2,64∙10-38002 + 29694,49 = 3688 – 83,75 – 1689,6 + 29694,49 = 31609,15 Дж ............................ ∆Н01700 = 4,61∙1700 – 0,67∙105/1700 – 2,64∙10-3∙17002 + 29694,49 = 29862,48Дж Значения тепловых эффектов приведем в табл. 2.
Таблица 2. Величина ∆Н0т при различных температурах для реакции H2S + CO2= H2O + COS
Зависимость ∆Н0т - Т, построенная по данным табл. 2 представлена на рис. 1 и позволяет найти на только значение теплового эффекта при любой температуре в заданном интервале, но и легко определить величину ∆СР. Например, требуется определить ∆СР рассматриваемого процесса при 1300 К. Из дифференциальной формы закона Кирхгофа: следует, что тангенс угла наклона касательной, проведенной к кривой при температуре 1300К дает величину ∆СР (см. рис. 1). Чтобы определить численное значение ∆СР возьмем на касательной две произвольные точки «а» и «b». Можно записать: Расчет ∆СР,1300 по уравнению (3) дает близкие к найденному графическим способом значения:
∆СР,1300 = 4,61 - 6,86 + 0,04 = -2,21 Дж/К Расчет изменения энтропии реакции Изменение Энтропии системы в результате протекания процесса определяется по уравнению: В этом уравнении ∆S0298 – стандартное изменение энтропии для реакции при 298 К, определяемое по мольным энтропиям веществ ∆S0i,298: Значение ∆S0298 для соответствующих веществ приведены в табл. 1, после их подстановки в уравнение (7) получим: ∆S0298 = ∆S0298(н2о) + ∆S0298(cos) – (∆S0298(н2s) + ∆S0298(co2)) = = 231,53 + 188,72 - (213,66+205,70) = 0,89 Дж/К
= 0,89 +(4,61∙ln│Т│- 5,28∙10-3∙Т –0,335∙105∙Т-2) – (26,3 – 1,57 – 0,38)= = 4,61∙ln│Т│- 5,28∙10-3∙Т –0,335∙105∙Т-2 – 23,46 Рассчитаем изменение энтропии в заданном интервале температур и полученные данные сведем в табл. 3. ∆S0800 = 4,61∙ln│800│-5,28∙10-3∙800 – 0,335∙105∙800-2 – 23,46 = 3,079 Дж/К ............................... ∆S01700 =4,61∙ln│1700│–5,28∙10-3∙1700–0,335∙105∙1700-2 – 23,46 = 1,843Дж/К Таблица 3. Значения изменения энтропии (∆S0т ) при различных Т,К
По данным табл. 3 построим график ∆S0т = f(Т) (см. рис. 2). |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2018-04-12; просмотров: 257. stydopedya.ru не претендует на авторское право материалов, которые вылажены, но предоставляет бесплатный доступ к ним. В случае нарушения авторского права или персональных данных напишите сюда... |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
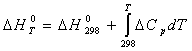 (1)
(1)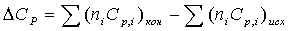 (2)
(2)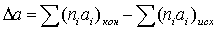 (4)
(4)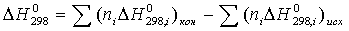 (5)
(5)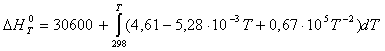
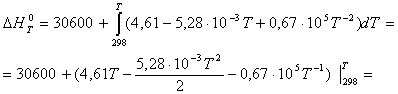
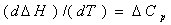
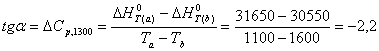 Дж/К
Дж/К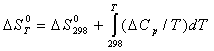 (6)
(6)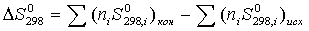 (7)
(7)